Clear Sky Science · fr
Base structurale de la reconnaissance des récepteurs de chauves-souris par le SARS-CoV-2 et les coronavirus apparentés de type SARS2 chez les chauves-souris
Pourquoi cette histoire chauve‑souris–virus compte toujours
La pandémie de COVID‑19 a commencé il y a plus de six ans, et les scientifiques cherchent encore à reconstituer comment le virus responsable, le SARS‑CoV‑2, est devenu si efficace pour infecter l’humain. Une énigme centrale porte sur la manière dont ce virus, et ses proches parents trouvés chez les chauves‑souris, s’attachent à une protéine appelée ACE2 à la surface des cellules — une première étape cruciale de l’infection. Comprendre ces interactions microscopiques de type serrure‑clé permet d’éclairer l’origine du virus, ses adaptations et ce qui pourrait se produire si des virus apparentés franchissaient à l’avenir la barrière d’espèce vers l’homme. 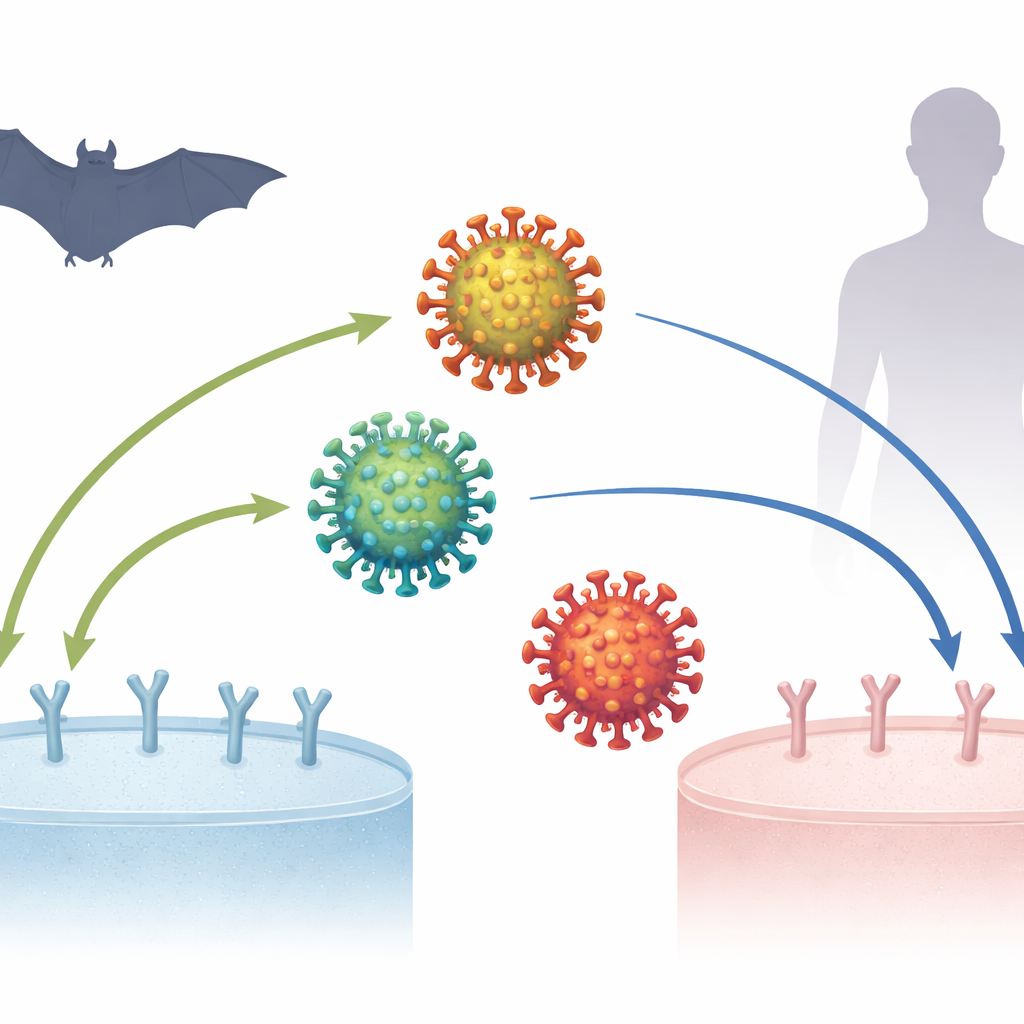
Observer la poignée virale
L’étude se concentre sur la protéine spike, la structure en forme de couronne à la surface du virus qui saisit ACE2. Une petite région de la spike, le domaine de liaison au récepteur (RBD), joue le rôle d’un bout du doigt qui agrippe la « poignée » ACE2. Des travaux antérieurs ont montré que lorsque des coronavirus sautent d’une espèce à une autre — par exemple des chauves‑souris aux civettes puis aux humains — le RBD accumule souvent des mutations qui améliorent son adhérence au ACE2 du nouvel hôte. Mais le SARS‑CoV‑2 posait une question : sa forme originelle se liait déjà très bien à l’ACE2 humain, même avant qu’un long temps d’adaptation n’ait pu s’écouler, et certains virus de chauves‑souris apparentés au SARS‑CoV‑2 semblaient se lier mieux à l’ACE2 humain qu’à l’ACE2 des chauves‑souris. Cela a amené certains à se demander si le SARS‑CoV‑2 constituait une exception aux règles évolutives usuelles.
Mettre à l’épreuve les récepteurs de chauve‑souris et humains
Pour explorer ce mystère, les chercheurs ont examiné deux coronavirus de chauves‑souris étroitement liés au SARS‑CoV‑2, appelés BANAL‑52 et BANAL‑236. Ils ont comparé la force d’attachement des RBD de ces virus et du SARS‑CoV‑2 à l’ACE2 humain et à l’ACE2 de plusieurs espèces de chauves‑souris. En utilisant des tests de liaison sur cellules, des mesures biosensorielles de haute précision et des essais d’infection avec des « pseudovirus » inoffensifs, ils ont identifié un schéma net. Le RBD de BANAL‑52 se liait le plus fortement à l’ACE2 d’une espèce de chauve‑souris, Rhinolophus sinicus, et un peu moins fortement à l’ACE2 humain. Le RBD du SARS‑CoV‑2, en revanche, présentait une préférence modeste pour l’ACE2 humain par rapport à l’ACE2 de chauve‑souris. Globalement, le RBD de BANAL‑52 liait plus fermement les récepteurs de chauve‑souris et humains que celui du SARS‑CoV‑2, mais il était le mieux ajusté à cet ACE2 de chauve‑souris en particulier. 
Comment une modification à l’échelle atomique fait basculer la balance
L’équipe s’est ensuite tournée vers la cristallographie aux rayons X, qui révèle des structures au niveau atomique, pour voir précisément comment le « doigt » viral et la « poignée » ACE2 se touchent. Ils se sont focalisés sur deux positions clés : une sur le RBD viral (appelée résidu 498) et une sur l’ACE2 (résidu 41). Dans BANAL‑52, à la fois le site viral et le site de l’ACE2 de la chauve‑souris utilisent le même élément constitutif, l’histidine, ce qui permet une interaction très ajustée et superposée — empilement comme deux pièces de monnaie — et forme aussi une liaison hydrogène. Dans l’ACE2 humain, la même position porte un élément apparenté mais légèrement différent, la tyrosine, qui s’empile encore bien avec l’histidine de BANAL‑52 mais manque la liaison hydrogène supplémentaire. Le SARS‑CoV‑2 utilise pour sa part une glutamine à cette position virale, qui ne peut pas s’empiler de la même manière, entraînant une liaison plus faible aux ACE2 de chauve‑souris et humains. En échangeant délibérément ces acides aminés dans l’ACE2 de chauve‑souris, les chercheurs ont confirmé que le renforcement ou l’affaiblissement de ce point de contact unique pouvait inverser la préférence pour un virus ou un hôte donné.
Pourquoi l’ACE2 humain est une porte si accueillante
Au‑delà de ce contact unique, les auteurs se sont demandé pourquoi l’ACE2 humain est en général une porte si efficace pour les coronavirus. En comparant côte à côte les ACE2 de chauves‑souris et d’humains, ils ont identifié plusieurs caractéristiques propres à l’humain qui améliorent la « poignée » virale. Deux positions sur l’ACE2 humain, portant les acides aminés histidine (au site 34) et méthionine (au site 82), créent des liaisons hydrogène plus fortes et des « zones » hydrophobes qui aident le RBD viral à s’ancrer plus solidement. Un autre résidu humain, la thréonine au site 27, rend en fait l’attachement un peu plus faible que dans la version de chauve‑souris, mais dans l’ensemble les contacts favorables supplémentaires l’emportent. Ces détails s’accordent avec des travaux antérieurs montrant que l’ACE2 humain comporte plusieurs « points chauds » qui en font naturellement un récepteur attractif pour une large gamme de coronavirus.
Reformuler l’histoire de l’origine
En regroupant toutes les données, l’étude soutient que le SARS‑CoV‑2 et ses proches bat‑virus suivent bien le scénario évolutif habituel. La spike de BANAL‑52 semble mieux adaptée à l’ACE2 de certaines chauves‑souris, tout en restant compatible avec l’ACE2 humain. La spike du SARS‑CoV‑2, quant à elle, est davantage ajustée à l’ACE2 humain qu’à celle des chauves‑souris, aidée par des points de contact particuliers sur le récepteur humain. De petites modifications à seulement quelques positions — en particulier au résidu viral 498 et aux sites voisins — peuvent déplacer l’avantage vers un hôte ou un autre. Pour le grand public, la conclusion est qu’il n’est pas nécessaire d’invoquer des explications exotiques : des principes structuraux simples et bien compris des interactions protéine–protéine suffisent à expliquer comment ces virus reconnaissent les cellules de chauves‑souris et d’humains, et ils soutiennent un lien évolutif étroit entre le SARS‑CoV‑2 et les coronavirus apparentés de chauves‑souris.
Citation: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Mots-clés: évolution du SARS-CoV-2, coronavirus de chauves-souris, récepteur ACE2, plage d’hôtes du virus, liaison de la protéine spike