Clear Sky Science · fr
La protéine codée par le virus de la peste porcine africaine MGF 505–3R compromet l’immunité innée via la dégradation de MyD88 médiée par l’ubiquitine
Pourquoi c’est important pour la santé animale et au-delà
La peste porcine africaine a dévasté des élevages de porcs dans le monde entier, menaçant les approvisionnements alimentaires et entraînant d’énormes pertes économiques. Le virus responsable est si létal en partie parce qu’il échappe aux systèmes d’alerte précoces de l’organisme. Cette étude révèle comment une protéine virale, nommée MGF 505–3R, sabote discrètement un interrupteur d’alarme clé à l’intérieur des cellules et montre qu’un très court fragment de cette protéine peut être transformé en un puissant agent anti-inflammatoire chez la souris.
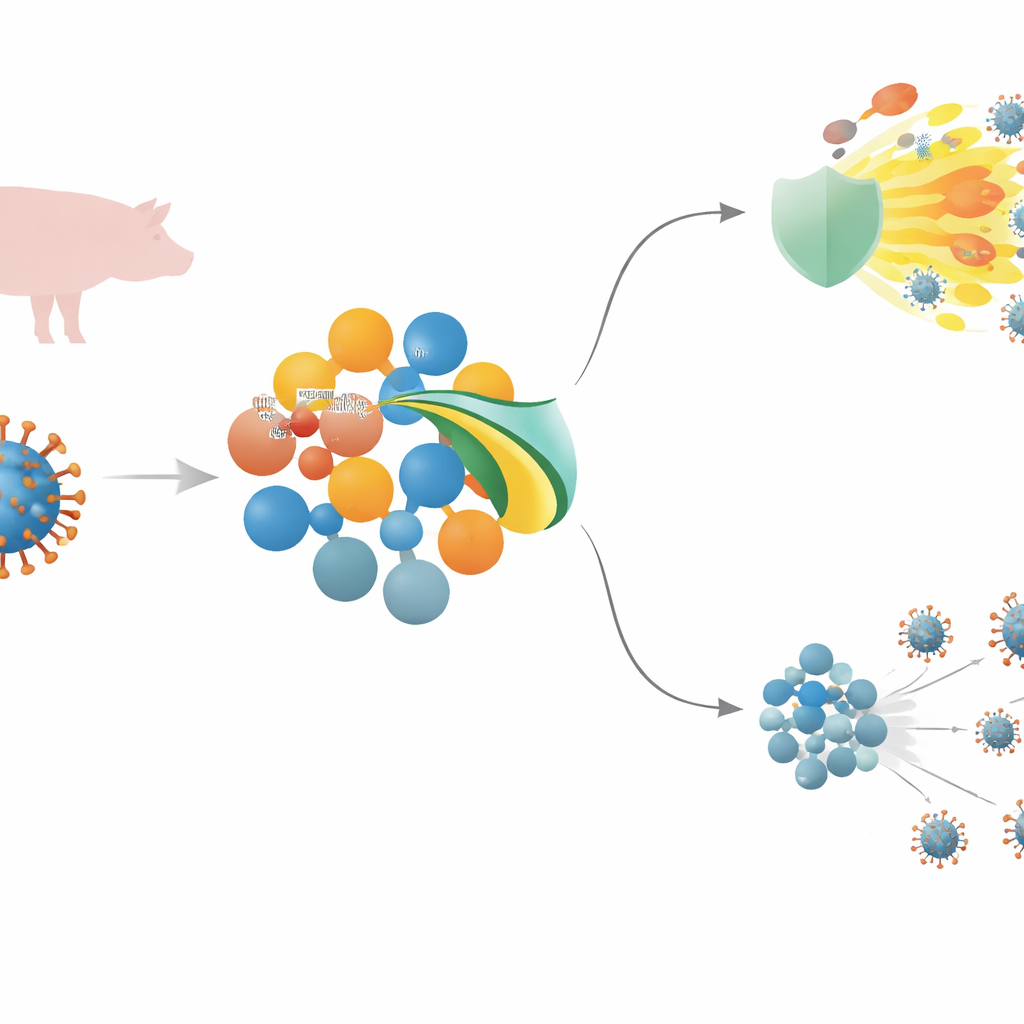
Un virus porcin mortel et la première ligne de défense de l’organisme
Le virus de la peste porcine africaine (VPPA) est un grand virus à ADN qui peut tuer presque tous les porcs infectés. Pour s’implanter, il doit déjouer l’immunité innée — la défense de première ligne, rapide, qui détecte les envahisseurs et déclenche inflammation et molécules antivirales. Au centre de cette réponse se trouve une chaîne de signalisation incluant des capteurs de surface, une protéine relais appelée MyD88, et un interrupteur maître connu sous le nom de NF–κB, qui ensemble stimulent la production de messagers inflammatoires et d’interférons antiviraux. Le VPPA porte de nombreux gènes supposés interférer avec ces signaux, mais pour plusieurs d’entre eux, y compris MGF 505–3R, leurs mécanismes précis restaient mal compris.
Comment le virus coupe les fils de l’alarme immunitaire
Les chercheurs ont testé les protéines du VPPA pour leur capacité à atténuer l’activité de NF–κB et ont découvert que MGF 505–3R était un inhibiteur particulièrement puissant. En présence de cette protéine virale, des cellules exposées à différents stimuli immunitaires produisaient beaucoup moins de cytokines inflammatoires et des niveaux nettement plus faibles d’interférons de type I et III. Une analyse plus fine a montré que MGF 505–3R agit directement sur MyD88, l’adaptateur central qui relie de nombreux capteurs immunitaires à NF–κB. MGF 505–3R se lie à MyD88 et le marque pour élimination via la machinerie de dégradation protéique de la cellule, en utilisant une forme d’étiquetage appelée ubiquitination liée en K48. À mesure que MyD88 est dégradé, NF–κB ne parvient plus à migrer vers le noyau et à activer les gènes protecteurs, laissant les cellules plus perméables à la réplication virale.
Zoom sur un petit fragment protéique mais puissant
Pour identifier la partie cruciale de MGF 505–3R, l’équipe a produit des versions tronquées de la protéine et testé leurs effets. Ils ont découvert que les acides aminés 89–277 étaient à la fois nécessaires et suffisants pour se lier à MyD88, favoriser son ubiquitination et bloquer l’activation de NF–κB. Guidés par des prédictions informatiques de structure protéique, ils ont isolé deux courts peptides issus de cette région. L’un d’eux, pep3R–1, s’est distingué : il réduisait fortement l’activité de NF–κB, empêchait la phosphorylation et la translocation nucléaire de la sous-unité p65 de NF–κB, et diminuait l’expression de cytokines inflammatoires et d’interférons dans des cellules immunitaires stimulées par divers signaux de danger. En culture cellulaire, à la fois la protéine MGF 505–3R complète et pep3R–1 ont non seulement atténué la signalisation antivirale mais ont aussi permis à un virus témoin de se répliquer plus efficacement, soulignant la puissance de cette voie pour contrôler les infections.
Transformer une ruse virale en médicament potentiel
L’équipe a ensuite cherché à savoir si le peptide pouvait être utilisé pour calmer une inflammation nocive plutôt que pour aider les virus. Dans un modèle murin de colite induite par un produit chimique appelé DSS, les animaux perdent normalement du poids, développent des diarrhées sanglantes et présentent de graves lésions et une infiltration de cellules immunitaires dans le côlon. Les souris traitées par pep3R–1 s’en sont beaucoup mieux sorties : les scores de maladie étaient plus bas, les côlons plus longs et en meilleur état, et l’examen microscopique a révélé une architecture tissulaire préservée avec beaucoup moins de cellules inflammatoires. Les niveaux de molécules inflammatoires clés telles que TNF–α, IL–1β, IL–6, et d’une enzyme liée à l’afflux des globules blancs étaient tous réduits dans les tissus coliques et le sang. Dans une expérience séparée, pep3R–1 a également atténué la réponse inflammatoire à une toxine bactérienne systémique, indiquant qu’il peut modérer à la fois les tempêtes inflammatoires locales et générales.
Ce que cela signifie pour les porcs, les humains et les traitements futurs
Ce travail montre que la protéine du VPPA MGF 505–3R aide le virus à prospérer en démantelant un relais immunitaire central, MyD88, fermant ainsi à la fois les défenses inflammatoires et les réponses à l’interféron. Parallèlement, un petit fragment de cette protéine virale, pep3R–1, peut être réutilisé pour atténuer en toute sécurité une inflammation excessive chez la souris, y compris dans un modèle de maladie intestinale. Bien qu’il reste beaucoup à faire — améliorer la stabilité, la délivrance et tester dans d’autres contextes pathologiques — l’étude révèle à la fois un point faible critique que les stratégies antivirales pourraient cibler et une feuille de route prometteuse pour concevoir de nouveaux médicaments anti-inflammatoires peptidiques inspirés par les mécanismes d’évasion immunitaire virale.
Citation: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Mots-clés: Peste porcine africaine, immunité innée, NF-kappaB, MyD88, peptide anti-inflammatoire