Clear Sky Science · fr
Une homéostasie du fer anormale entraîne l’altération des cellules ciliées cochléaires et la perte auditive chez des souris déficientes en Gprasp2
Pourquoi c’est important pour l’audition au quotidien
On pense souvent que la perte auditive relève d’un simple « usure », mais pour de nombreuses personnes elle est provoquée par des défauts génétiques cachés. Cette étude révèle comment un gène peu étudié, GPRASP2, contribue à protéger les cellules sensibles au son de l’oreille interne contre des dommages induits par le fer. En montrant précisément ce qui se passe quand ce gène manque, ce travail ouvre la voie à des diagnostics plus précis et à de futures thérapies pour des troubles auditifs héréditaires et, possiblement, certains troubles de l’humeur associés.
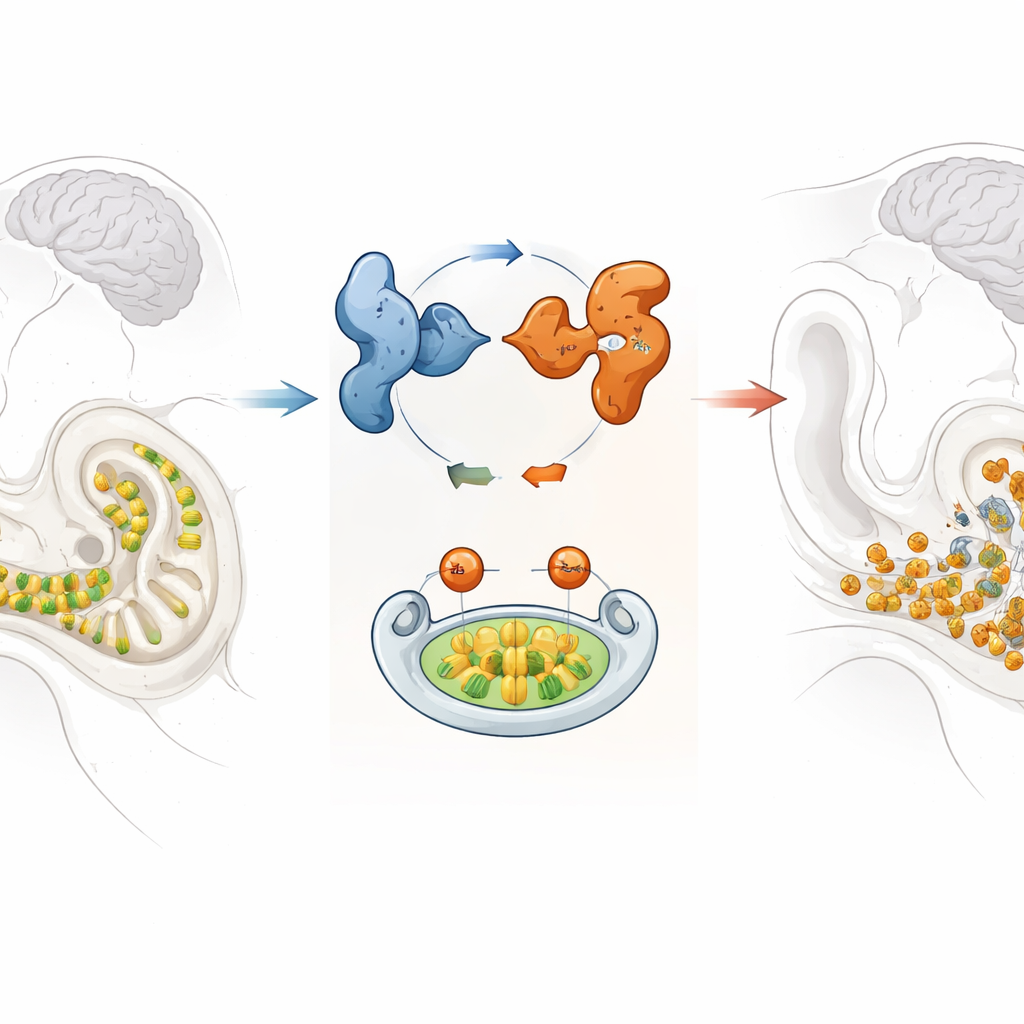
Un capteur sonore fragile dans l’oreille interne
Dans la cochlée enroulée de l’oreille interne se trouvent des rangées de cellules ciliées qui transforment de minuscules vibrations en signaux électriques compréhensibles par le cerveau. Une fois perdues, ces cellules ne repoussent pas, d’où l’importance de les préserver pour conserver l’audition toute la vie. Les chercheurs se sont intéressés à GPRASP2, un gène précédemment identifié comme muté dans une famille présentant une perte auditive syndromique liée à l’X, ce qui signifie que l’affection touche principalement les hommes et peut s’accompagner de symptômes supplémentaires. Bien que GPRASP2 fût connu pour être actif dans le cerveau et l’oreille interne, son rôle exact dans l’audition restait flou.
Que se passe-t-il quand le gène manque
Pour reproduire la situation humaine, l’équipe a utilisé l’édition génomique CRISPR pour créer des souris dépourvues d’une copie fonctionnelle du gène Gprasp2. Ces animaux présentaient une perte auditive nette sur une large gamme de fréquences, mesurée par des enregistrements électriques sensibles du nerf auditif. Leurs réponses aux sons brusques et forts étaient atténuées, tandis que leur équilibre et leurs capacités motrices restaient en grande partie normales, ce qui indique un problème spécifique à l’audition plutôt qu’un trouble moteur général. Fait intéressant, les souris montraient aussi des comportements de type dépressif dans plusieurs tests standards, suggérant que ce gène relie audition et humeur par ses actions à la fois dans l’oreille et le cerveau.
Dommages à l’intérieur de la cochlée
En examinant les oreilles internes des souris déficientes en Gprasp2, les scientifiques ont constaté que de nombreuses cellules ciliées externes étaient absentes ou déplacées, et que les cellules restantes présentaient souvent des faisceaux de stéréocils déformés qui jouent normalement un rôle d’accordage. Ils ont aussi observé des altérations de la strie vasculaire, un tissu très actif qui maintient le milieu liquide et électrique spécial nécessaire à l’audition. Au niveau microscopique, des marqueurs de mort cellulaire et de stress oxydatif étaient élevés dans les cellules ciliées externes et les neurones auditifs voisins, indiquant que ces structures subissaient une forte attaque par des molécules réactives et étaient plus susceptibles de mourir.
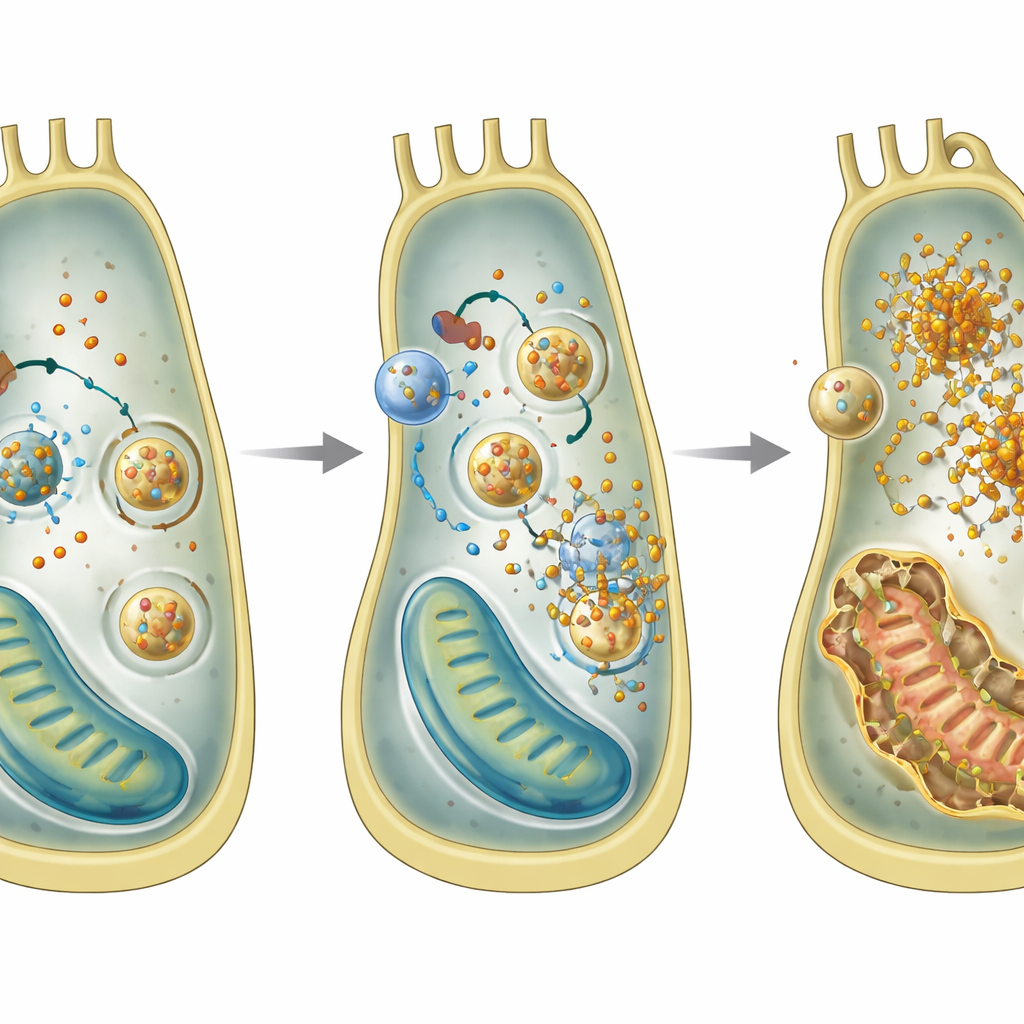
Surcharge en fer et recyclage excessif
Pour approfondir, l’équipe a utilisé une lignée cellulaire de l’oreille interne pour explorer ce qui dysfonctionne à l’intérieur des cellules individuelles privées de GPRASP2. Ils ont identifié un schéma caractéristique d’une forme de mort cellulaire appelée ferroptose, nourrie par le fer et la peroxydation lipidique. Les cellules dépourvues de Gprasp2 accumulaient davantage de fer ferreux, produisaient plus d’espèces réactives de l’oxygène, avaient des niveaux réduits du glutathion antioxydant et présentaient des mitochondries endommagées. Les analyses géniques et protéiques indiquaient une augmentation de la ferritinophagie, un processus où les particules de stockage du fer sont livrées aux compartiments de recyclage puis dégradées, libérant ainsi du fer supplémentaire dans la cellule. Le blocage de cette étape de recyclage a réduit l’accumulation de fer, soutenant l’idée qu’une ferritinophagie excessive est au cœur des dommages.
Un partenaire protéique clé qui régule le fer
Les chercheurs ont ensuite cherché à savoir comment GPRASP2 contrôle cette machinerie de gestion du fer. En cartographiant les protéines interagissant avec GPRASP2, ils ont identifié NCAM1, une molécule d’adhésion cellulaire surtout connue pour ses rôles dans l’apprentissage, la mémoire et l’humeur. Ils ont montré que GPRASP2 se lie physiquement à NCAM1, et que la perte de GPRASP2 entraîne une diminution des niveaux de NCAM1 dans les cellules ciliées et dans des cellules auditives en culture. Un faible niveau de NCAM1 était associé à une augmentation de la ferritinophagie et à une surcharge en fer. Restaurer NCAM1 dans des cellules déficientes en Gprasp2 a réduit les niveaux de fer et atténué des régulateurs clés de la ferritinophagie, même si l’autophagie générale restait active. Cela suggère que GPRASP2 module finement une voie spécifique de recyclage du fer via NCAM1, plutôt que d’activer ou d’éteindre l’ensemble du système de recyclage.
Ce que cela signifie pour l’audition et au-delà
En termes simples, ce travail montre que GPRASP2 agit comme un gestionnaire de sécurité du fer à l’intérieur des cellules ciliées cochléaires. Lorsque GPRASP2 est présent, il coopère avec NCAM1 pour empêcher qu’une trop grande quantité de fer stocké ne soit déversée dans la cellule, limitant ainsi les dommages oxydatifs. Lorsque le gène est perturbé, la gestion du fer se déséquilibre, les cellules s’oxydent de l’intérieur et les cellules ciliées cruciales meurent, entraînant une perte auditive. Comme GPRASP2 et NCAM1 fonctionnent aussi dans le cerveau, la même voie pourrait contribuer aux changements d’humeur observés chez certains patients. Comprendre ce mode de défaillance lié au fer offre une cible claire pour de futurs médicaments ou thérapies géniques visant à préserver l’audition chez les personnes atteintes de troubles génétiques liés à GPRASP2 ou similaires.
Citation: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Mots-clés: perte auditive héréditaire, cellules ciliées cochléaires, homéostasie du fer, ferroptose, GPRASP2