Clear Sky Science · fr
La protéine d’enveloppe du ZIKV bloque fortement la différenciation directionnelle précoce dans la lignée neuronale
Pourquoi cela compte pour les cerveaux en croissance
Le virus Zika a d’abord fait la une en raison d’un lien avec des nouveau-nés présentant des têtes anormalement petites et des lésions cérébrales graves. Mais comment une infection chez la mère perturbe-t-elle si puissamment les toutes premières étapes de la construction du cerveau chez l’embryon ? Cette étude se concentre sur un seul composant viral — la protéine d’enveloppe qui recouvre les particules du Zika — et examine si cette protéine seule peut perturber la formation des cellules nerveuses. En recréant en laboratoire le développement cérébral précoce avec des cellules souches de souris, les chercheurs montrent comment cette protéine virale bloque discrètement mais fortement la construction normale des circuits neuronaux.
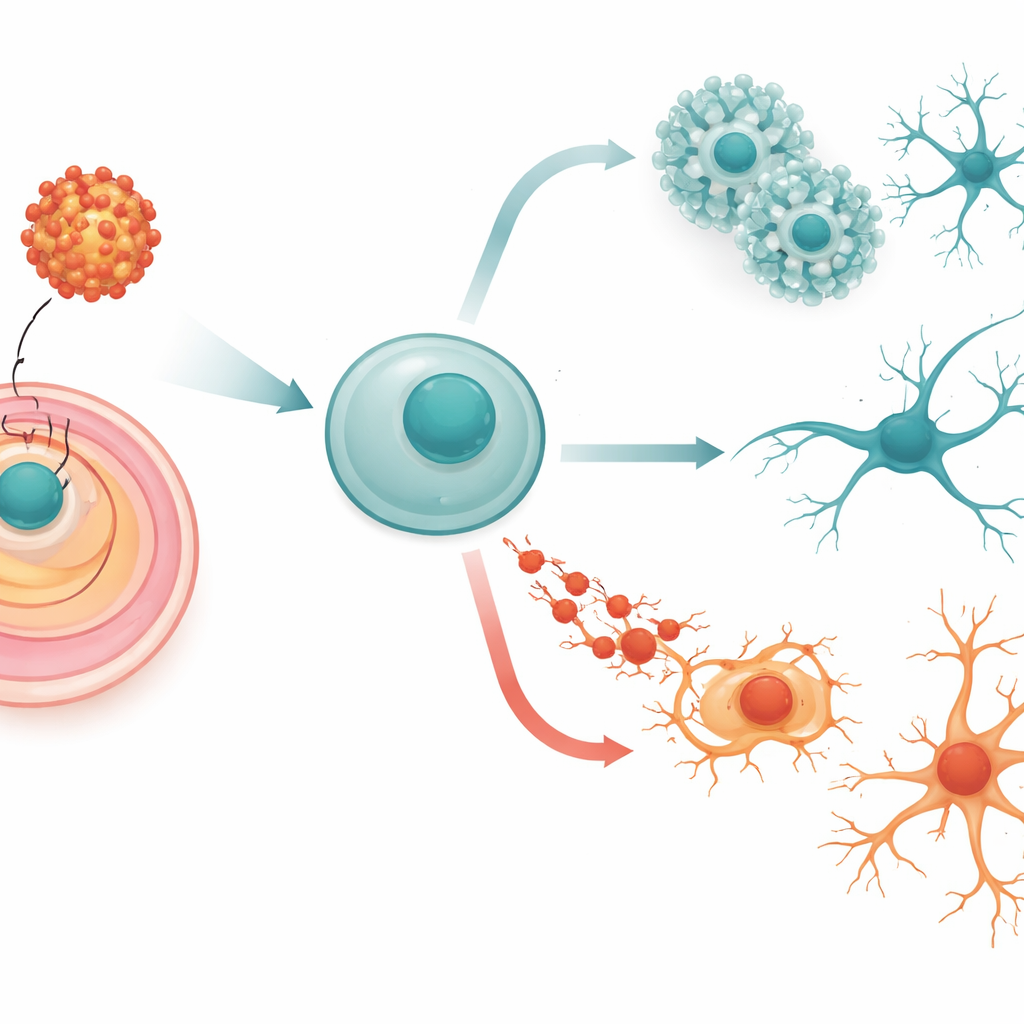
Des cellules souches flexibles aux futures cellules nerveuses
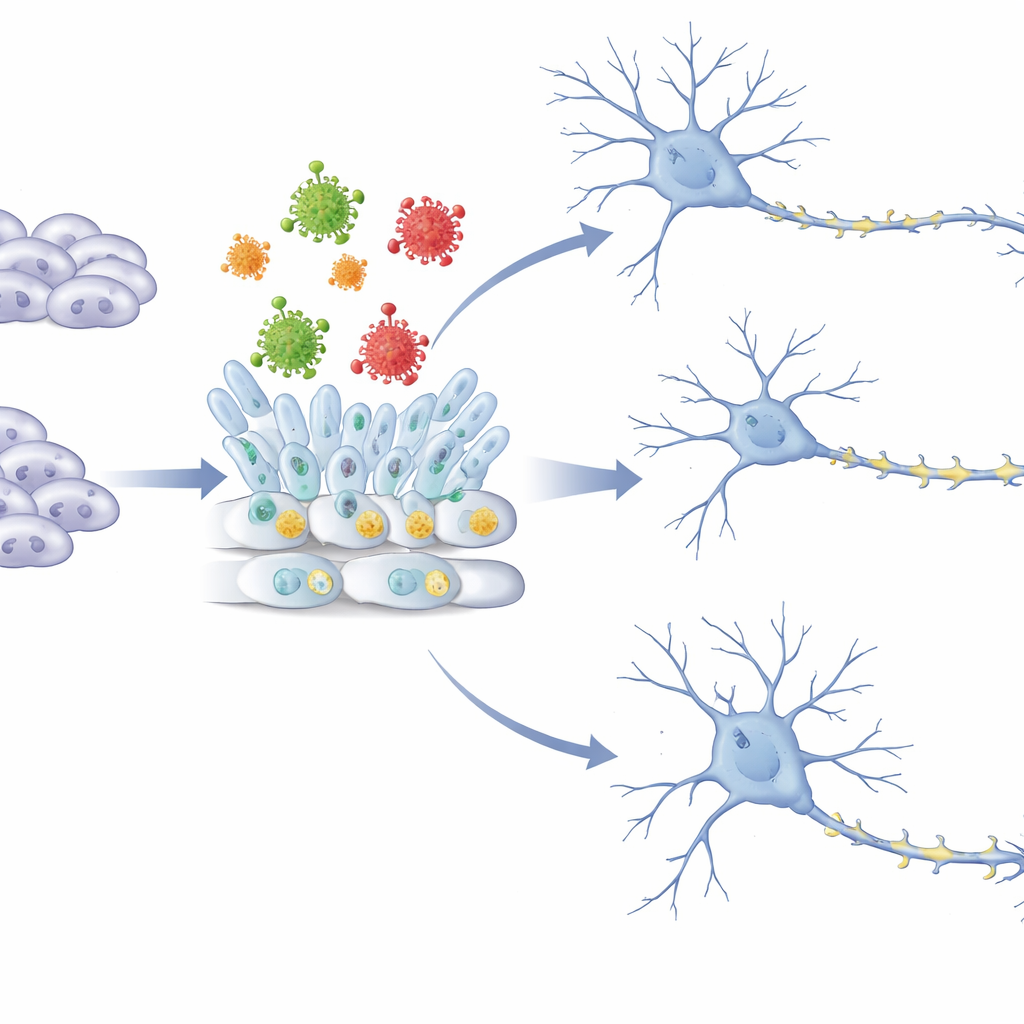
Nos cerveaux commencent sous la forme de cellules simples et très flexibles appelées cellules souches embryonnaires. Ces cellules peuvent devenir n’importe quel tissu du corps, mais, dans des conditions appropriées, elles suivent un trajet soigneusement ordonné vers la formation de cellules nerveuses. D’abord elles s’engagent sur la voie « neuronale », puis forment des structures en rosette rappelant le système nerveux primitif, et finalement mûrissent en neurones qui se connectent via de longs prolongements ramifiés. L’équipe a utilisé des cellules souches embryonnaires de souris comme modèle de ces stades précoces et les a modifiées pour produire la protéine d’enveloppe du Zika, avec ou sans un petit changement à un site clé d’attachement de sucre connu pour moduler la virulence du virus.
La protéine de l’enveloppe fige les premières étapes de la construction cérébrale
Lorsque les cellules souches produisaient la protéine d’enveloppe du Zika, elles semblaient toujours saines et conservaient leur potentiel large de différenciation. Cependant, lorsqu’elles étaient laissées à se différencier librement, leur capacité à former des agrégats 3D complexes représentant les trois feuillets embryonnaires était fortement réduite, et les marqueurs de ces trois couches chutaient. Cela suggère que la protéine virale ne tue pas directement les cellules souches, mais interfère subtilement avec leur aptitude à emprunter les trajectoires développementales normales. Une version mutante de la protéine, dépourvue d’un attachement sucré spécifique, modifiait ce profil de façon plus inégale, laissant penser que la décoration chimique fine de la protéine module la façon dont elle nuit au développement.
Bloquer la route de la cellule souche au neurone
Les chercheurs se sont ensuite concentrés sur le trajet de la cellule souche au neurone précoce en utilisant deux modèles établis : une culture en « monocouche » plate et une culture 3D en « neurosphère » qui imite le tissu cérébral précoce. Dans les deux systèmes, les cellules témoins augmentaient progressivement l’expression des marqueurs de cellules souches neurales et de neurones sur plusieurs jours, formant des rosettes organisées et de nombreux jeunes neurones. En revanche, les cellules produisant la protéine d’enveloppe généraient beaucoup moins de cellules souches neurales, moins de rosettes et bien moins de neurones précoces, comme le montraient des niveaux réduits de gènes et de protéines clés liés à l’identité neuronale. La forme mutante sans sucre provoquait généralement un blocage encore plus marqué au niveau génique et activait des voies inflammatoires de mort cellulaire supplémentaires, suggérant un mécanisme conduisant à des lésions plus sévères.
Étouffer la communication dans les jeunes réseaux nerveux
Pour comprendre ce qui dysfonctionnait à l’intérieur des cellules, l’équipe a comparé l’activité génique globale entre cellules normales et cellules produisant l’enveloppe à des stades critiques de différenciation. Ils ont observé que de nombreux gènes liés à la croissance neuronale, à la formation de synapses et aux petites épines dendritiques qui stockent la mémoire étaient réprimés. Les voies impliquées dans le chargement et la libération des neurotransmetteurs, le guidage des axones vers leurs cibles et l’assemblage des synapses étaient toutes atténuées. Parallèlement, des voies de signalisation associées au calcium et à certains récepteurs de surface cellulaire étaient activées, ce qui pourrait rendre les cellules excessivement excitable ou mal signalées. Ces changements profonds sont apparus aussi bien dans les cultures plates que dans les cultures 3D, montrant que la protéine d’enveloppe détourne de façon répétée les cellules neurales en développement de la construction de réseaux robustes et bien connectés.
Ce que cela signifie pour les malformations liées au Zika
Pour les non-spécialistes, le message clé est que le virus Zika n’a pas besoin de se multiplier activement ou de tuer les cellules pour nuire au cerveau en développement. Ce travail montre que sa protéine d’enveloppe seule peut détourner les cellules souches précoces du chemin normal vers la différenciation neuronale et affaiblir les programmes génétiques nécessaires à la formation de synapses et d’épines dendritiques saines. De telles perturbations précoces et silencieuses aident à expliquer comment une exposition in utero peut conduire à des troubles comme la microcéphalie et à des déficits cognitifs à long terme. Les résultats soulignent aussi que les vaccins ou thérapies impliquant des protéines d’enveloppe virales doivent être évalués avec précaution pour leurs effets potentiels sur le développement cérébral, même en l’absence de virus vivant.
Citation: Ma, ZH., Wang, Y., Hassaan, N.A. et al. ZIKV envelope protein is a strong blocker of early directional differentiation in the neural lineage. Commun Biol 9, 395 (2026). https://doi.org/10.1038/s42003-026-09672-1
Mots-clés: virus Zika, développement cérébral, cellules souches neurales, protéine d’enveloppe virale, microcéphalie