Clear Sky Science · fr
Le facteur de transcription horloge centrale TOC1 se lie directement aux promoteurs de gènes de défense régulant l’immunité chez Arabidopsis
Les plantes sur un calendrier de défense quotidien
Les plantes ne peuvent pas fuir les agents pathogènes, elles dépendent donc de systèmes de défense finement réglés. Cette étude révèle qu’une composante de l’horloge interne quotidienne de la plante, une protéine appelée TOC1, fait plus que donner l’heure. Elle décide aussi quand les plantes sont les plus vulnérables ou les plus résistantes à un champignon de la pourriture grise courant, contribuant ainsi à expliquer pourquoi l’heure de la journée peut modifier l’issue d’une infection.
Pourquoi l’heure de la journée modifie le risque d’infection
Les chercheurs ont travaillé avec Arabidopsis, une petite crucifère largement utilisée comme organisme modèle, et le champignon Botrytis cinerea, qui attaque de nombreuses cultures. Des travaux antérieurs montraient que les plantes sont généralement plus résistantes à ce champignon à l’aube et plus susceptibles la nuit. Dans cette étude, l’équipe s’est concentrée sur TOC1, une protéine clé de l’horloge qui atteint normalement son pic en soirée, pour vérifier si elle contrôle directement cette oscillation jour–nuit de la résistance aux maladies.
Une protéine de l’horloge qui affaiblit les défenses végétales
En utilisant des plantes modifiées pour surexprimer TOC1 et des mutants dépourvus de TOC1, les auteurs ont infecté des feuilles soit à l’aube subjective, soit la nuit, en conditions de lumière constante ou de cycles lumière–obscurité normaux. Chez les plantes normales, la taille des lésions — tissus nécrosés causés par le champignon — dépendait fortement du moment de l’infection. En revanche, les plantes surexprimant TOC1 et celles dépourvues de TOC1 ont perdu cette variation quotidienne. Les plantes avec un excès de TOC1 restaient dans un état très susceptible, tandis que les plantes sans TOC1 se comportaient comme si elles étaient verrouillées dans leur état le plus résistant. Ce schéma montre que TOC1 agit comme un frein de l’immunité : plus il y a de TOC1, plus la défense est affaiblie, en particulier lorsqu’il est normalement élevé en soirée.
Des gènes de défense déjà prêts avant l’attaque
Pour comprendre ce que faisait TOC1 à l’intérieur de la cellule, l’équipe a comparé l’activité de milliers de gènes chez les plantes normales et chez les mutantes dépourvues de TOC1, avec et sans infection. Avant même l’arrivée du champignon, le mutant sans TOC1 présentait déjà une mauvaise régulation de centaines de gènes liés au stress et à la défense. Nombre de ces gènes portaient de courts motifs d’ADN que TOC1 reconnaît, ce qui suggère qu’il est normalement positionné sur leurs régions de contrôle pour les maintenir réprimés. Des régulateurs clés des voies hormonales impliquées dans la défense, en particulier celles gouvernées par l’acide jasmonique et l’éthylène, étaient plus actifs en l’absence de TOC1, fournissant une explication moléculaire à la résistance accrue du mutant.
Comment TOC1 et MYC2 partagent les mêmes interrupteurs
L’histoire devient plus complexe au niveau des interrupteurs de défense individuels dans le génome. Les auteurs se sont intéressés de près à plusieurs facteurs de transcription liés à la défense — ERF4, ORA47, ORA59 et WRKY33 — dont les promoteurs contiennent un motif d’ADN commun appelé G-box. Ce même motif est reconnu par une autre protéine, MYC2, acteur central de la signalisation à l’acide jasmonique. Par immunoprécipitation de la chromatine, ils ont montré que TOC1 occupe physiquement ces régions de G-box chez les plantes saines, ce qui concorde avec son rôle de maintien des gènes de défense sous contrôle. Après l’infection fongique, l’occupation de ces promoteurs par TOC1 disparaît en grande partie, tandis que MYC2 reste lié. Lorsque MYC2 est éliminé génétiquement, la liaison de TOC1 chez les plantes saines diminue et, fait crucial, TOC1 n’est plus libéré après l’infection. Parallèlement, l’expression des régulateurs de défense en aval chute. Ensemble, ces résultats indiquent que MYC2 aide à recruter puis à évincer TOC1 des gènes de défense de manière dépendante de l’infection.
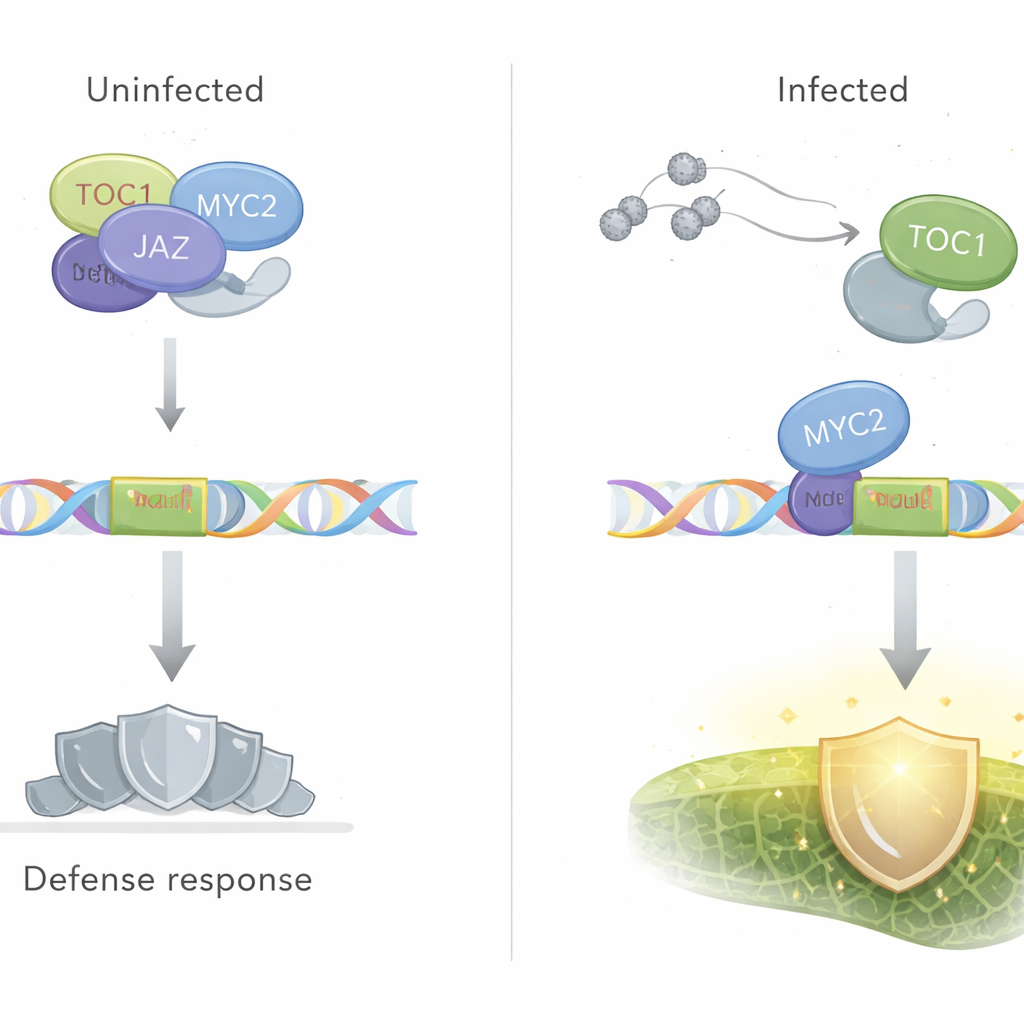
Une immunité régulée par l’horloge au quotidien
En assemblant ces éléments, les auteurs proposent que l’horloge de la plante et la signalisation hormonale forment un panneau de contrôle partagé pour l’immunité. Sur un cycle de 24 heures, les niveaux de TOC1 augmentent vers la soirée et, avec l’aide de MYC2, TOC1 se positionne sur les motifs G-box des gènes de défense et en atténue l’activité, créant une « porte » quotidienne qui rétrécit la fenêtre d’une défense forte. Lorsqu’un pathogène est détecté et que les niveaux d’acide jasmonique augmentent, MYC2 modifie son comportement, TOC1 est libéré de ces sites d’ADN et le frein sur la défense est levé afin que la plante puisse monter une réponse aiguë, indépendamment de l’heure de la journée. Pour le lecteur non spécialiste, le message clé est que la vigueur du système immunitaire des plantes n’est pas constante : elle est programmée par l’horloge interne, et TOC1 est un élément central qui commute directement les interrupteurs de gènes de défense importants.
Citation: Sparks, SL., Roden, L.C. & Ingle, R.A. The core clock transcription factor TOC1 binds directly to defence gene promoters regulating immunity in Arabidopsis. Commun Biol 9, 402 (2026). https://doi.org/10.1038/s42003-026-09667-y
Mots-clés: horloge circadienne des plantes, immunité d’Arabidopsis, Botrytis cinerea, signalisation au jasmonate, facteurs de transcription