Clear Sky Science · fr
La transcriptomique unicellulaire révèle les mécanismes de la différenciation du muscle squelettique au cours du développement embryonnaire du canard
Pourquoi le développement musculaire du canard importe
Le muscle squelettique permet aux animaux de se déplacer, de voler et, pour les espèces d’élevage, détermine aussi la texture et la saveur de la viande. Cette étude se concentre sur la formation du muscle pectoral du canard de Pékin avant l’éclosion, en utilisant des outils unicellulaires puissants pour observer des dizaines de milliers de cellules individuelles au fur et à mesure qu’elles croissent et se spécialisent. En suivant le parcours de chaque cellule, d’un état précoce proche de la cellule souche jusqu’à une fibre musculaire pleinement formée, les chercheurs dévoilent comment apparaissent différents types de fibres musculaires, comment elles peuvent changer d’identité et quelles règles sont partagées entre oiseaux et mammifères.
Construire le muscle à partir des premières cellules
Le muscle du canard commence comme un mélange de cellules très plastiques de type souche dès les premiers stades embryonnaires. L’équipe a créé un « atlas cellulaire » détaillé en séquençant l’ARN de près de 77 000 cellules individuelles issues d’embryons de canard à dix moments différents, du très jeune développement jusqu’à l’éclosion. Ils ont identifié deux réservoirs principaux de cellules souches qui dominent les stades précoces et donnent progressivement naissance à de nombreux types cellulaires de soutien et formateurs de muscle. Parmi eux, un sous-ensemble de cellules souches mésenchymateuses marqué par une molécule appelée MYL9 semble constituer la principale source des futurs progéniteurs musculaires. Au fil du temps, ces progéniteurs deviennent des myoblastes qui fusionnent en structures plus grandes, aboutissant aux longues fibres multinucléées qui composent le muscle fonctionnel.
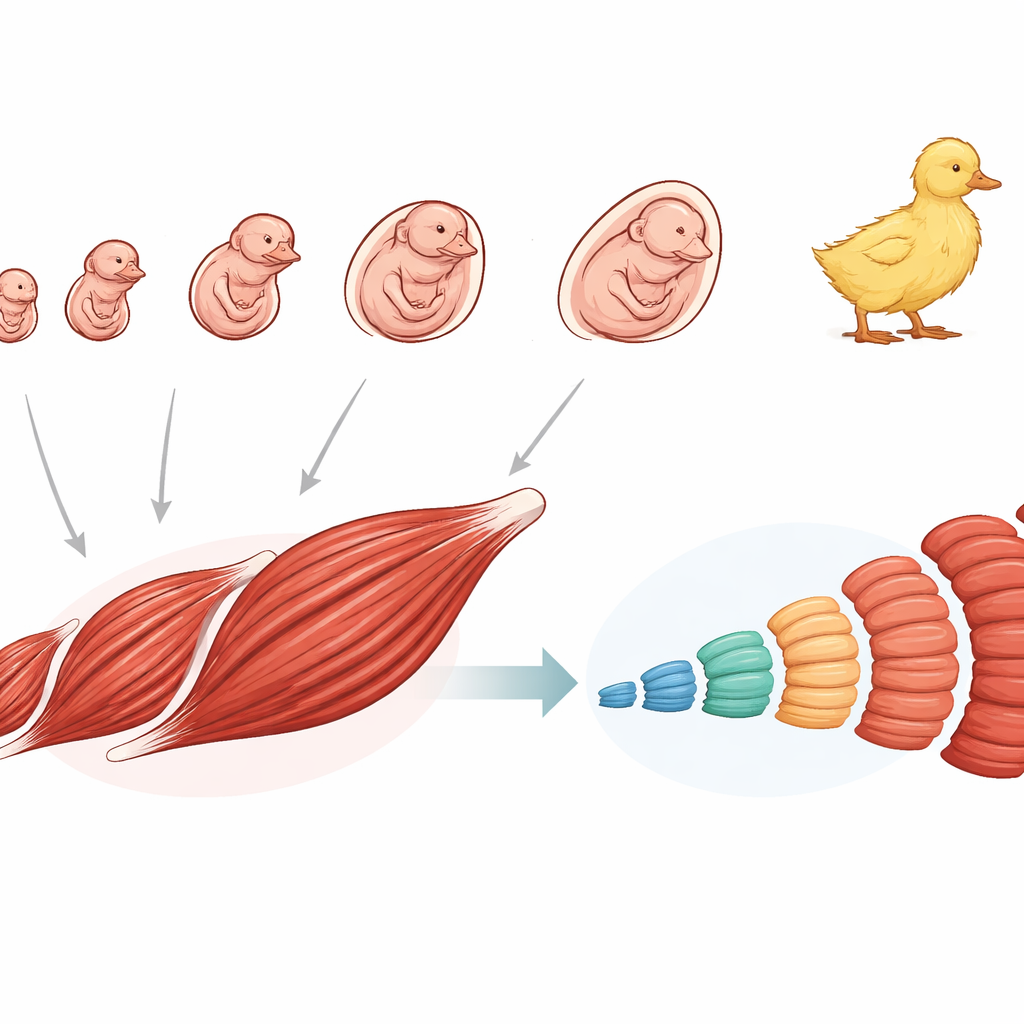
Deux branches clés : des fibres pour le travail et des cellules pour la réparation
Lorsque les chercheurs ont suivi les cellules de la lignée musculaire au « pseudotemps » du développement, ils ont observé que les progéniteurs précoces se scindent en deux branches majeures. Une branche produit les fibres musculaires matures nécessaires à la contraction. L’autre forme les cellules satellites, « l’équipe de réparation » à longue durée de vie qui reste majoritairement inactive jusqu’à ce qu’elles soient sollicitées pour la croissance ou la régénération plus tard dans la vie. Le long de la branche des cellules satellites, des gènes spécifiques s’activent et se désactivent de manière coordonnée, faisant passer les cellules d’un état de repos à un état actif et prolifératif. L’analyse met en évidence une poignée de gènes régulateurs qui agissent vraisemblablement comme des interrupteurs de ce processus d’activation. Dans la branche de formation des fibres, l’étude souligne des processus cellulaires tels que le trafic membranaire et l’adhésion cellule–cellule, cruciaux pour que les myoblastes fusionnent et construisent des fibres musculaires robustes.
Comment les fibres lentes deviennent des fibres rapides
Une des découvertes les plus marquantes est que les fibres musculaires ne se forment pas simplement dès le départ comme « lentes » ou « rapides ». Au début du développement du canard, les fibres à contraction lente — meilleures pour un travail soutenu et endurant — sont fréquentes, tandis que les fibres à contraction rapide, responsables de mouvements brefs et puissants, sont rares. À mesure que l’embryon mûrit, l’équilibre s’inverse. En suivant l’activité génique dans des fibres individuelles, les chercheurs ont découvert une transition « lente-vers-rapide » par étapes. Les fibres lentes traversent un état intermédiaire, incluant un sous-type nouvellement décrit marqué par le facteur LEF1, puis acquièrent des caractéristiques de fibres rapides. En cours de route, certaines fibres présentent brièvement une identité hybride, affichant des traits des deux types, ce qui suggère une fenêtre de plasticité où leur destin peut encore changer.
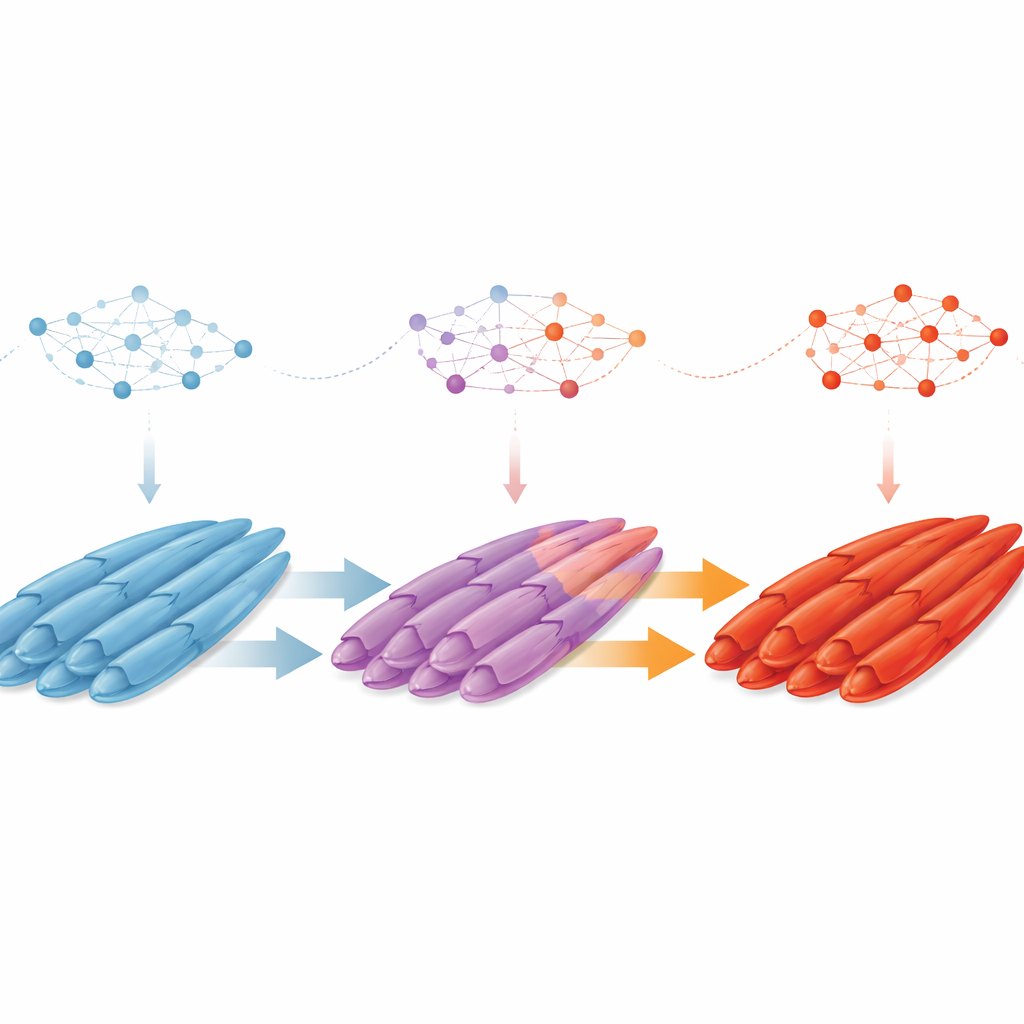
Gènes de contrôle et règles partagées entre espèces
L’équipe a ensuite cherché à savoir ce qui régule ce changement d’identité des fibres. En reconstruisant des réseaux géniques, ils ont identifié 13 facteurs de transcription clés — des régulateurs maîtres qui coordonnent des groupes de gènes — guidant les cellules depuis les progéniteurs précoces jusqu’aux myoblastes, aux fibres en maturation et aux cellules satellites. Deux facteurs, TBX15 et PBX3, se dégagent comme de solides candidats pour orienter les fibres vers un comportement rapide, agissant via des voies bien connues de croissance et de survie telles que PI3K–Akt et les voies des récepteurs tyrosine kinases. Enfin, en comparant les données du canard avec des cartes unicellulaires de porc, de poulet et de souris, les auteurs montrent que de nombreux types cellulaires, gènes marqueurs et même le schéma global de transition lente-vers-rapide sont conservés chez les oiseaux et les mammifères. Cela suggère que des programmes génétiques profonds et partagés façonnent la spécialisation des muscles chez les vertébrés.
Ce que cela signifie pour la biologie et au-delà
Pour un public non spécialisé, la conclusion principale est que les fibres musculaires ne sont pas figées à la naissance : chez le canard, et probablement chez de nombreux vertébrés, les fibres lentes précoces peuvent se transformer en fibres rapides via une séquence organisée d’états intermédiaires contrôlés par des gènes et des voies de signalisation spécifiques. Comprendre cette feuille de route aide à expliquer comment les animaux ajustent finement leurs muscles pour le vol, la course ou d’autres tâches, et pourquoi la composition en fibres influence la qualité de la viande. À plus long terme, ces mêmes principes pourraient éclairer des stratégies pour améliorer les caractères musculaires du bétail ou pour concevoir des thérapies régénératives qui reconstruisent ou reconfigurent le muscle humain après blessure ou maladie.
Citation: Sun, Y., Li, Z., Jie, Y. et al. Single-cell transcriptomics reveal mechanisms of skeletal muscle differentiation across duck embryonic development. Commun Biol 9, 404 (2026). https://doi.org/10.1038/s42003-026-09665-0
Mots-clés: développement du muscle squelettique, types de fibres musculaires, transcriptomique unicellulaire, embryogenèse du canard, transition fibres lentes-vers-rapides