Clear Sky Science · fr
Activation du récepteur couplé aux protéines G codé par le cytomégalovirus UL33 par un peptide N‑terminal inné
Comment un virus courant reconfigure nos cellules
Le cytomégalovirus humain (CMV) infecte silencieusement la plupart des personnes sur Terre et passe le plus souvent inaperçu. Pourtant, chez les nouveau‑nés, les patients transplantés et d’autres sujets immunodéprimés, il peut provoquer des maladies graves. Cette étude révèle, au niveau moléculaire, comment une protéine virale appelée UL33 agit comme un interrupteur interne qui pousse en permanence les cellules infectées à favoriser le virus. Comprendre cet interrupteur caché aide à expliquer comment le CMV persiste à vie et ouvre la voie à de nouvelles stratégies pour le neutraliser sans perturber la signalisation cellulaire normale.
Un interrupteur viral furtif à la surface cellulaire
Le CMV transporte ses propres versions de récepteurs de surface — des protéines qui, normalement, détectent des hormones ou des signaux immunitaires. UL33 est l’un de ces récepteurs viraux. Contrairement aux récepteurs typiques, qui attendent un signal externe, UL33 est « constamment actif ». Une fois inséré dans la membrane externe d’une cellule infectée, il peut se brancher simultanément sur plusieurs des principales voies de communication de la cellule. Ces voies contrôlent des processus tels que l’activité des gènes, le métabolisme et la décision de rester en latence ou de produire davantage de virus. Pendant des années, les scientifiques savaient qu’UL33 était actif mais ignoraient ce qui l’activait, d’autant plus qu’aucune molécule externe activatrice (ligand) n’avait jamais été identifiée.
Un démarreur autonome : le récepteur qui apporte sa propre clé
À l’aide de la cryo‑microscopie électronique avancée, les auteurs ont capturé des instantanés tridimensionnels d’UL33 lié à l’un des partenaires de signalisation cellulaire, une protéine G appelée Gs. Les images montrent que le tout début de la protéine UL33 — sa courte queue N‑terminale — se replie dans une poche du récepteur lui‑même, à la manière d’une clé laissée en permanence dans une serrure. Cette queue « enchaînée » s’insère dans une petite poche latérale qui, dans des récepteurs humains apparentés, recevrait normalement une portion d’une protéine de signalisation immunitaire appelée chimiokine. En occupant cette poche dès le départ, UL33 empêche les chimiokines externes de se lier, ce qui explique pourquoi il se comporte comme un récepteur « orphelin » qui ne répond pas aux messagers normaux de l’hôte.
Atomes cruciaux de l’interrupteur viral
Pour confirmer que cette queue intégrée est bien le déclencheur, l’équipe a modifié systématiquement des éléments individuels d’UL33 dans des cellules humaines. Ils se sont concentrés sur les premiers acides aminés de la queue et sur les points correspondants à l’intérieur de la poche qui la retiennent. Lorsqu’ils ont remplacé ces résidus clés par des plus neutres ou supprimé l’un d’eux, la capacité d’UL33 à signaler est tombée quasiment à zéro — bien que les récepteurs modifiés atteignaient toujours la surface cellulaire en quantités normales. Autrement dit, la protéine était présente mais muette. Cela montre que la queue n’est pas une simple ornementation structurale ; c’est la pièce auto‑activatrice essentielle qui maintient UL33 en position « on ».
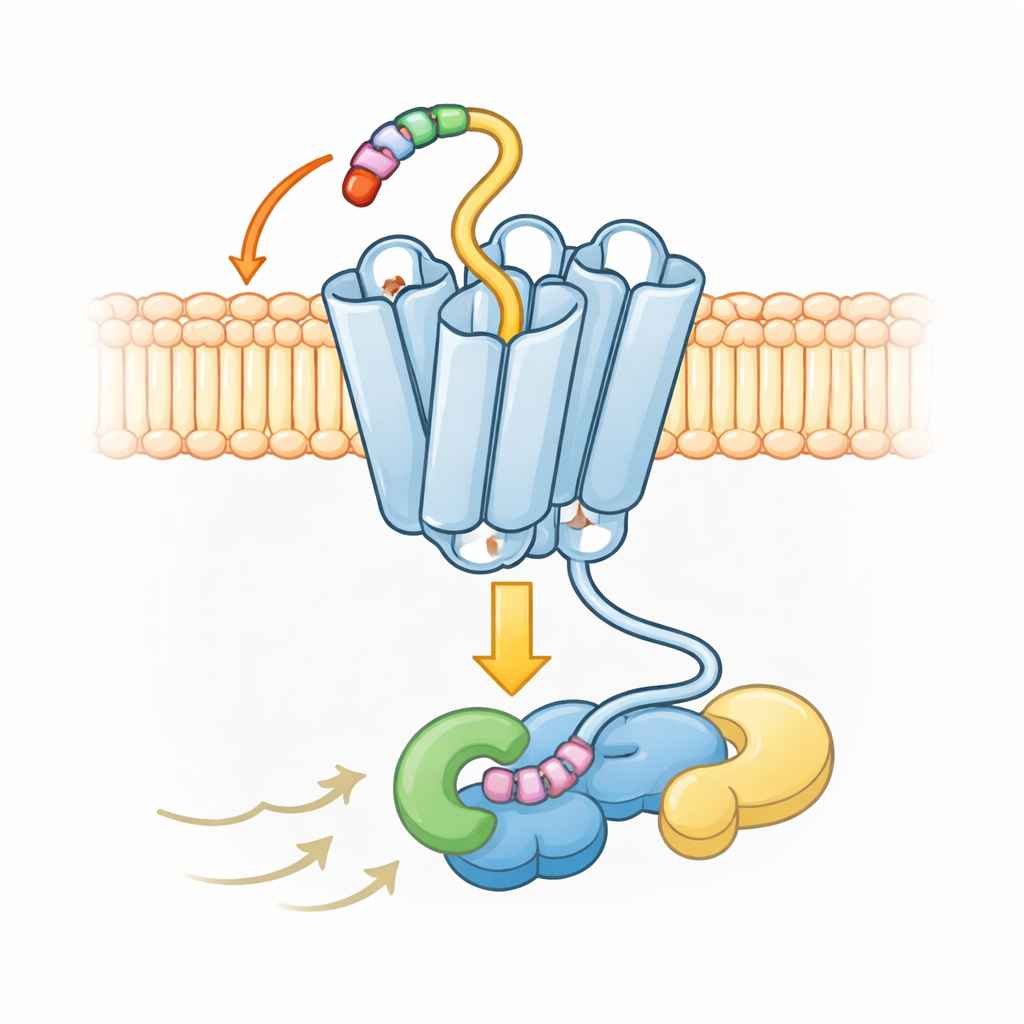
Une conformation inhabituelle pour une signalisation large mais contrôlée
Les cartes structurales révèlent aussi qu’UL33 adopte une forme active légèrement différente de celle des récepteurs humains typiques. Dans la plupart des récepteurs de cette famille, l’un des sept hélices proches de l’intérieur cellulaire se déplace fortement vers l’extérieur lors de l’activation, ouvrant une grande cavité pour que les protéines G s’y fixent. Chez UL33, cette hélice reste beaucoup plus proche du centre, créant un ajustement plus serré. Malgré cela, UL33 peut encore engager plusieurs types de protéines G — Gs, Gq et Gi — en établissant des contacts précis avec l’extrémité de la protéine G qui s’insère dans le récepteur. Ces contacts favorisent certains G et en excluent d’autres, comme le groupe G12/13, permettant au virus d’orienter les réponses cellulaires sans déclencher une signalisation incontrôlée.
Nouvelles vulnérabilités pour un vieux virus
En combinant imagerie structurale et tests fonctionnels, l’étude dresse un portrait clair : UL33 est un récepteur viral auto‑démarrant dont la propre queue joue le rôle d’activateur attaché en permanence. Ce dispositif permet au CMV d’ajuster doucement mais de façon persistante la signalisation de l’hôte pour favoriser la réplication et la réactivation virales, notamment en renforçant des voies qui activent les gènes viraux. Parallèlement, le travail met au jour des points faibles exploitables par des médicaments, comme un tunnel étroit menant à la poche où la queue se loge. Des molécules conçues pour s’immiscer dans cette région ou déloger la queue pourraient calmer l’activité d’UL33 et réduire les dommages viraux, tout en épargnant les récepteurs normaux de l’organisme. Pour les patients à risque lié au CMV, cibler cet « interrupteur maître » viral pourrait offrir un jour une manière plus précise de maintenir le virus sous contrôle.
Citation: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Mots-clés: cytomégalovirus, récepteur viral RCPG, signalisation cellulaire, structure cryo‑EM, ciblage médicamenteux