Clear Sky Science · fr
La privation de sommeil perturbe l’homéostasie des glandes lacrymales via l’axe hypothalamo-hypophyso-surrénalien et la dysbiose intestinale chez la souris
Pourquoi le manque de sommeil peut donner une sensation de grains dans les yeux
La plupart des gens savent qu’un sommeil insuffisant peut provoquer fatigue et brouillard cognitif le lendemain. Moins nombreux sont ceux qui se rendent compte que la perte chronique de sommeil peut aussi endommager en silence les glandes qui maintiennent nos yeux confortables et protégés. Cette étude chez la souris examine comment une privation de sommeil prolongée assèche la surface de l’œil en dérangeant les hormones du stress et les microbes intestinaux, et elle indique des pistes possibles pour préserver notre vision dans un monde privé de sommeil. 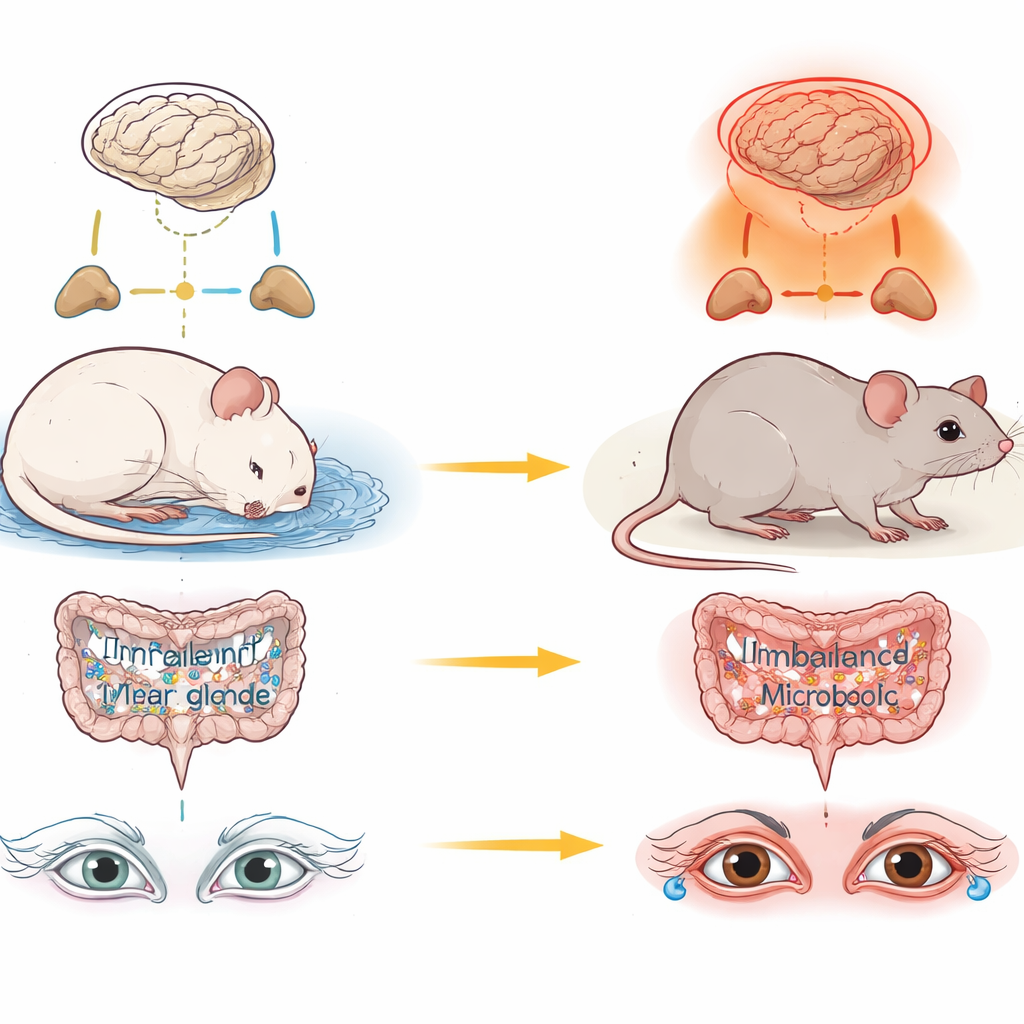
Une chaîne cachée du cerveau à l’intestin puis à l’œil
Les chercheurs se sont intéressés aux glandes lacrymales, petites structures proches des yeux qui produisent la couche aqueuse de nos larmes. Lorsque l’équipe a maintenu les souris éveillées pendant des semaines à l’aide d’un système automatisé et doux, les animaux ont produit moins de larmes et leurs glandes lacrymales ont diminué de volume et perdu leur organisation cellulaire normale. Parallèlement, l’activité génétique dans ces glandes a fortement basculé vers des programmes immunitaires et inflammatoires, incluant une voie puissante portée par une molécule appelée IL-17. En termes simples, les glandes qui devraient baigner l’œil de larmes sont devenues semblables à des tissus irrités et enflammés.
Les hormones du stress montent en puissance
La perte de sommeil est un déclencheur bien connu du principal circuit du stress de l’organisme, l’axe hypothalamo‑hypophyso‑surrénalien, qui aboutit à la libération d’hormones de stress par les surrénales. Chez les souris privées de sommeil, les niveaux du stéroïde corticostérone ont augmenté, et les glandes surrénales elles‑mêmes présentaient des signes d’activation immunitaire. Lorsque les scientifiques ont administré un médicament appelé métapirone pour bloquer la production de ces hormones de stress, une grande partie des lésions a été atténuée : les glandes lacrymales ont conservé une taille et une structure plus normales, la production de larmes s’est améliorée et les cellules immunitaires inflammatoires étaient moins abondantes. Cela suggère que la suractivation du signal de stress n’est pas qu’un effet secondaire du manque de sommeil, mais un moteur clé des lésions des glandes oculaires.
Les microbes intestinaux déséquilibrés
L’équipe s’est ensuite tournée vers l’intestin, où des trillions de microbes aident à digérer les aliments et à éduquer le système immunitaire. La privation chronique de sommeil a rendu la paroi intestinale plus perméable et a modifié de façon marquée la composition des bactéries intestinales. Les niveaux d’acides gras à chaîne courte — de petites molécules produites par des microbes bénéfiques qui contribuent à contenir l’inflammation — ont chuté dans l’intestin et dans le sang. Quand les chercheurs ont éliminé les bactéries intestinales avec des antibiotiques, les lésions des glandes lacrymales se sont aggravées, laissant entendre qu’une communauté microbienne saine protège normalement l’œil. 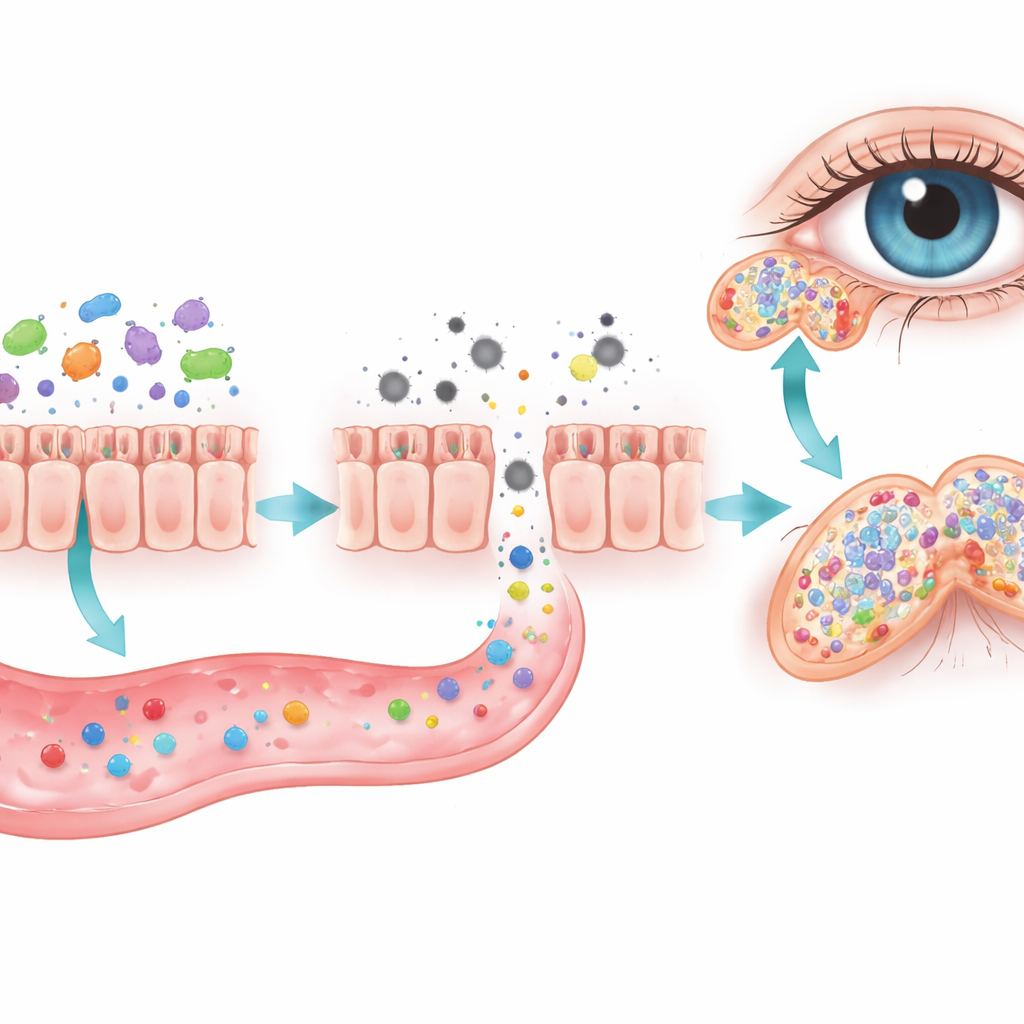
Restaurer les microbes et leurs métabolites utiles
Pour vérifier si corriger l’intestin pouvait sauver les yeux, les scientifiques ont testé deux stratégies. Dans l’une, ils ont transplanté les microbes intestinaux de souris saines dans des animaux privés de sommeil. Dans l’autre, ils ont ajouté un cocktail d’acides gras à chaîne courte dans l’eau de boisson. Les deux approches ont partiellement restauré des communautés intestinales normales, augmenté ces métabolites bénéfiques et atténué les lésions des glandes lacrymales. La production de larmes a augmenté, la structure des glandes s’est améliorée et les cellules immunitaires envahissantes ont diminué. Surtout, les trois interventions — blocage des hormones du stress, transplantation microbienne et supplémentation en acides gras à chaîne courte — ont convergé pour réduire l’inflammation liée à l’IL‑17 dans les glandes.
Ce que cela signifie pour des yeux fatigués
Au total, ce travail décrit un « axe » reliant le stress d’origine cérébrale, les microbes intestinaux et les glandes lacrymales. Dans ce modèle, la privation de sommeil chronique suractive les hormones du stress, perturbe l’écosystème intestinal, appauvrit les produits microbiaux apaisants et fragilise la barrière intestinale. Des signaux fuyant de l’intestin contribuent alors à déclencher une inflammation centrée sur l’IL‑17 dans les glandes lacrymales, qui se rétrécissent et réduisent la production de larmes. Bien que l’étude ait été réalisée chez des souris mâles, ces résultats laissent envisager que mieux dormir, contrôler le stress et, à l’avenir, des thérapies basées sur le microbiome pourraient aider à protéger les personnes souffrant de sécheresse oculaire et d’autres troubles oculaires liés au sommeil.
Citation: Huang, S., Yu, S., Zhang, W. et al. Sleep deprivation disrupts lacrimal gland homeostasis via hypothalamic-pituitary-adrenal axis and gut dysbiosis in mice. Commun Biol 9, 367 (2026). https://doi.org/10.1038/s42003-026-09657-0
Mots-clés: privation de sommeil, sécheresse oculaire, microbiome intestinal, hormones du stress, acides gras à chaîne courte