Clear Sky Science · fr
Étude des réponses en biofilm de Salmonella au traitement antibiotique par spectroscopie optique photothermique infrarouge
Pourquoi les cités collantes de microbes comptent
De nombreuses bactéries pathogènes préfèrent vivre en communautés denses appelées biofilms, où les cellules adhèrent les unes aux autres et aux surfaces à l’intérieur du corps ou sur des dispositifs médicaux. Dans ces « cités » visqueuses, les microbes peuvent résister à des antibiotiques qui les tueraient normalement. Cette étude présente une nouvelle façon d’examiner les biofilms en détail, révélant quelles cellules sont en croissance active et comment elles réagissent lorsque des médicaments puissants sont ajoutés. Comprendre ces motifs d’activité invisibles pourrait aider les cliniciens à concevoir des traitements capables de briser enfin les défenses tenaces des biofilms.
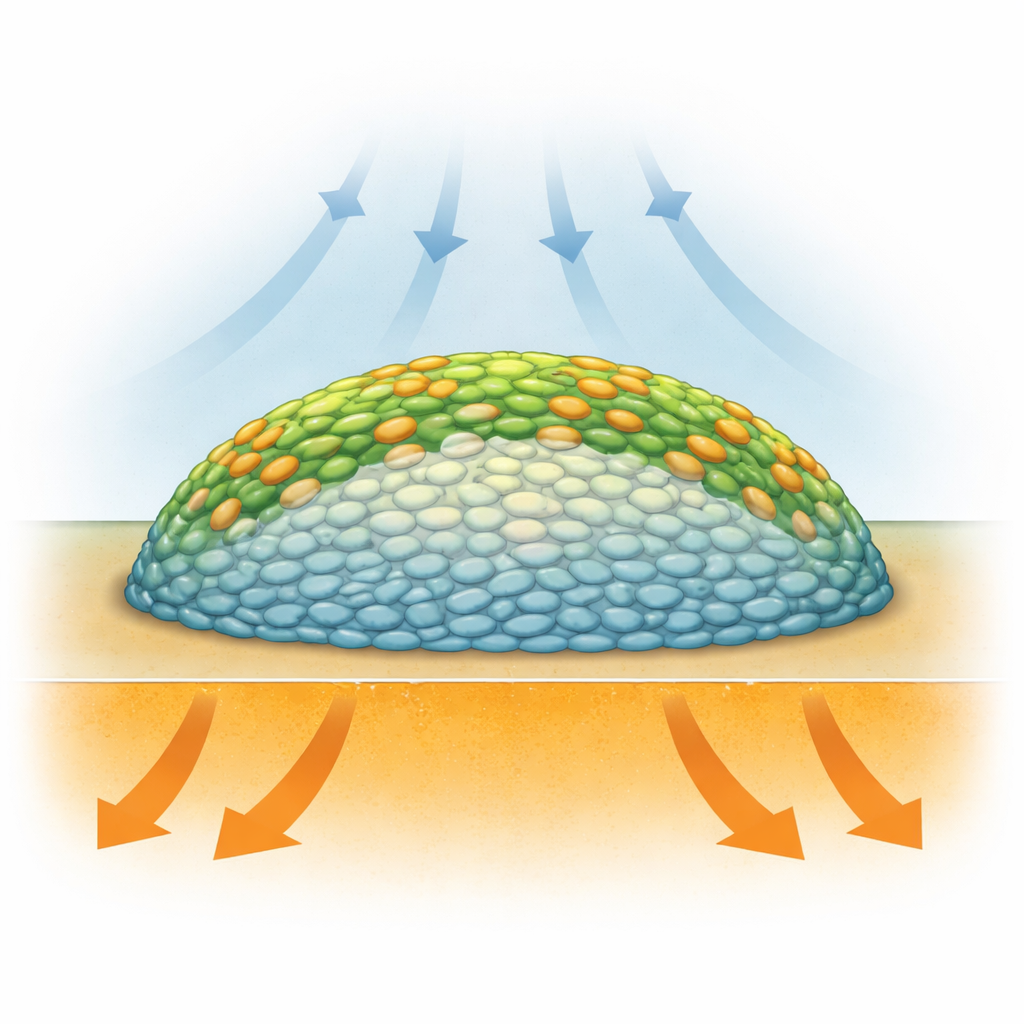
Vie cachée à l’intérieur des cités bactériennes
Les biofilms ne sont pas de simples amas aléatoires de microbes : ce sont des structures stratifiées où les bactéries vivent dans des conditions très différentes selon leur position. Les cellules externes ont un meilleur accès à l’oxygène de l’air, tandis que celles enfouies au centre sont privées d’oxygène et peuvent ralentir ou entrer en dormance. Les méthodes précédentes, comme la microscopie à fluorescence, permettaient de montrer la structure, mais exigeaient souvent des colorants ou des marqueurs génétiques qui pouvaient perturber la biologie, et elles ne mesuraient pas directement l’activité chimique des cellules. Les chercheurs avaient besoin d’un moyen de « voir » la chimie des biofilms vivants, couche par couche, sans les déchirer ni les altérer fortement.
Voir la chimie avec la lumière invisible
L’équipe s’est tournée vers une technique appelée spectroscopie optique photothermique infrarouge (O-PTIR), qui utilise des impulsions de lumière infrarouge invisible et un laser visible pour détecter de petites vibrations dans les molécules. Ces vibrations servent d’empreintes pour des composants cellulaires clés, comme les protéines, les lipides et l’ADN. Pour suivre le métabolisme — l’utilisation active des nutriments — ils ont alimenté des biofilms de Salmonella Typhimurium avec une forme spéciale de sucre dont les atomes de carbone étaient légèrement plus lourds que d’habitude (un isotope stable connu sous le nom de carbone-13). Lorsque les cellules sont en pleine croissance et synthétisent de nouvelles protéines, elles incorporent ces atomes plus lourds dans leurs propres structures, ce qui provoque des décalages subtils mais détectables dans le signal infrarouge. En réalisant des cryofractures du biofilm et en scannant des coupes transversales fines, les chercheurs ont produit des cartes chimiques montrant où dans le biofilm ce carbone lourd avait été incorporé.
Anneaux d’activité et cœurs silencieux
L’imagerie infrarouge des biofilms de Salmonella non traités a révélé un motif frappant : les régions externes et les couches de surface montraient une forte incorporation du carbone lourd, tandis qu’un large noyau central affichait très peu d’incorporation. Autrement dit, le biofilm se comportait comme un anneau de cellules actives entourant un intérieur calme. L’analyse statistique des spectres infrarouges a confirmé que les signaux liés aux vibrations des protéines étaient plus décalés dans les couches externes que dans le centre, indiquant une production protéique plus élevée en périphérie. Ces résultats soutiennent l’idée que la disponibilité en oxygène, maximale à la surface, est le principal moteur des « zones chaudes » métaboliques dans ce modèle de colonie, même si les nutriments arrivent par le dessous. L’étude a fourni l’une des vues les plus claires et les plus résolues à ce jour de la stratification du métabolisme à l’intérieur d’un biofilm.
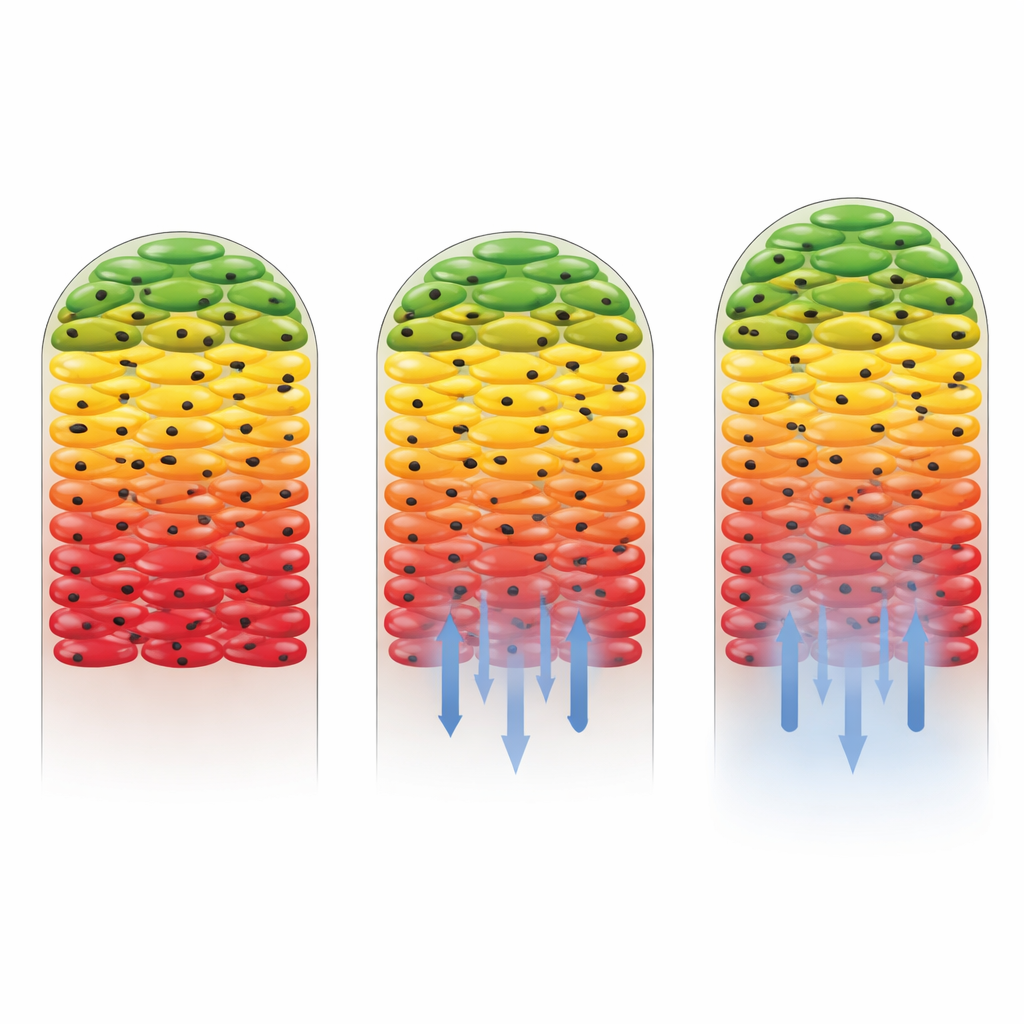
Comment différents antibiotiques remodèlent l’activité du biofilm
Les chercheurs ont ensuite examiné ce qui se passe lorsque des antibiotiques sont introduits. Ils ont utilisé deux médicaments : la kanamycine, à laquelle la souche de Salmonella est sensible, et la gentamicine, à laquelle la souche avait été rendue en grande partie non sensible. En présence de gentamicine, le schéma général d’un extérieur actif et d’un noyau calme a à peine changé, montrant que des cellules résistantes continuaient de croître et d’incorporer le carbone lourd dans une grande partie du biofilm. En revanche, la kanamycine a réduit de manière spectaculaire l’activité métabolique, en particulier près du bas du biofilm où la concentration du médicament était la plus élevée. Seule une mince bande de cellules la plus éloignée de la source d’antibiotique montrait encore des signes d’absorption du carbone. Cela a révélé non seulement que le médicament était efficace, mais aussi que la structure du biofilm elle-même contribuait à protéger certaines cellules en affaiblissant le médicament au fur et à mesure de sa diffusion vers l’intérieur.
Nouvelles fenêtres pour traiter les infections tenaces
Pour un lecteur non spécialiste, le message clé est que ce travail propose un « microscope chimique » puissant pour observer comment les communautés bactériennes vivent et survivent aux traitements en trois dimensions. En combinant une méthode d’imagerie infrarouge non destructive avec une forme sûre de carbone lourd, les chercheurs ont pu localiser précisément où les bactéries croissaient activement et comment cette activité changeait sous différents antibiotiques. Leurs résultats confirment que les biofilms abritent un mélange de cellules actives et quasiment dormantes, et que les médicaments efficaces peuvent néanmoins être contrecarrés par la barrière physique du biofilm. À l’avenir, cette approche pourrait servir à tester de nouvelles thérapies, explorer comment différentes espèces coopèrent ou partagent la résistance dans des biofilms mixtes, et ultimement aider à concevoir des stratégies plus intelligentes pour éliminer les infections persistantes.
Citation: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Mots-clés: biofilms, Salmonella, résistance aux antibiotiques, imagerie infrarouge, sondage par isotope stable