Clear Sky Science · fr
Le dinactine d’origine naturelle cible la protéine cpsA et tue Mycobacterium tuberculosis en perturbant la force motrice protonique
Un nouvel espoir contre un tueur pulmonaire tenace
La tuberculose reste l’une des maladies infectieuses les plus meurtrières au monde, et des souches résistantes à plusieurs antibiotiques se propagent. Cette étude présente un composé naturel appelé dinactine, produit par des bactéries du sol, capable de tuer Mycobacterium tuberculosis, y compris des formes résistantes aux médicaments et des formes dormantes particulièrement difficiles à éliminer. En sondant le mode d’action de la dinactine et sa coopération avec des médicaments existants, les chercheurs esquissent une stratégie prometteuse pour raccourcir et renforcer le traitement de la tuberculose.
Trouver une arme cachée dans la nature
Pour chercher de nouveaux antibiotiques contre la tuberculose, l’équipe a criblé plus de 6 000 extraits naturels de plantes et de micro-organismes, testant leur capacité à arrêter la croissance des bactéries de la tuberculose dans des cellules entières plutôt que sur des enzymes isolées. Parmi les nombreux candidats, la dinactine s’est distinguée. Elle appartient à une famille de molécules cycliques appelées macrotétrolides et a montré une forte activité contre des souches de laboratoire standard à des doses très faibles, sans endommager les globules rouges. En comparant la dinactine à des molécules proches, elle s’est avérée à la fois plus puissante et plus sélective, ce qui en a fait la meilleure candidate pour une investigation approfondie. 
Une action puissante sur des bactéries difficiles d’accès
Les bactéries responsables de la tuberculose peuvent se cacher dans plusieurs états difficiles à traiter : se divisant activement dans les poumons, en dormance avec un métabolisme ralenti, ou abritées à l’intérieur des cellules immunitaires. La dinactine les a attaquées dans ces trois conditions. Elle a tué les bacilles en croissance active avec une chute marquée du nombre de bactéries viables et a également été efficace contre des cellules non réplicatives appauvries en nutriments qui survivent souvent aux thérapies standards. Dans un modèle de macrophage humain, la dinactine a pénétré les cellules hôtes et réduit d’environ cent fois le nombre de bacilles internalisés. Dans des larves de ver de cire infectées, modèle in vivo, la dinactine seule a amélioré la survie et réduit la charge bactérienne, et ses bénéfices ont été encore plus importants lorsqu’elle a été associée aux médicaments antituberculeux existants.
Associer la dinactine aux médicaments existants
Comme le traitement de la tuberculose repose sur des combinaisons médicamenteuses, les chercheurs ont testé l’interaction de la dinactine avec des antibiotiques courants tels que la rifampicine, l’isoniazide, la bédaquiline et d’autres. À l’aide d’essais en damier (checkerboard), ils ont constaté que la dinactine renforçait fortement l’effet de la plupart de ces médicaments, en particulier de la rifampicine et de l’isoniazide : l’ajout de dinactine a permis à des doses beaucoup plus faibles de ces standards d’être efficaces. Notamment, appliquée à des isolats cliniques multirésistants, la dinactine a restauré une grande partie de leur sensibilité à la rifampicine et à l’isoniazide. Dans des cultures en phase stationnaire qui reproduisent l’infection persistante, des combinaisons de dinactine avec la rifampicine ou l’isoniazide ont tué bien plus de bactéries que chaque médicament seul, suggérant que des cocktails à base de dinactine pourraient aider à éradiquer plus rapidement les infections tenaces.
Comment la dinactine sape l’énergie bactérienne
Pour comprendre comment la dinactine tue les bacilles tuberculeux, l’équipe a examiné ses effets sur l’enveloppe cellulaire et les systèmes énergétiques. La dinactine agit comme un transporteur d’ions, faisant passer le potassium et le sodium à travers la membrane bactérienne. Ce flux ionique supplémentaire rend la membrane plus poreuse et plus fluide, ridant visiblement la surface bactérienne et permettant aux colorants de pénétrer plus facilement. En déplaçant les ions, la dinactine effondre la force motrice protonique — le gradient électrique et chimique que les bactéries utilisent comme une petite batterie pour alimenter la production d’ATP. Les mesures ont montré que les deux composantes de ce gradient, la tension à travers la membrane et la différence de protons, disparaissaient après traitement par la dinactine. En conséquence, les niveaux d’ATP à l’intérieur des cellules ont chuté, bien que leur machinerie de consommation d’oxygène continue de fonctionner, indiquant que la production d’énergie avait été découplée de la respiration. La dinactine a aussi perturbé l’équilibre entre les formes réduites et oxydées d’un cofacteur métabolique clé (NADH/NAD+) et déclenché une rafale d’espèces réactives de l’oxygène à l’intérieur des bactéries, endommageant davantage les composants cellulaires. 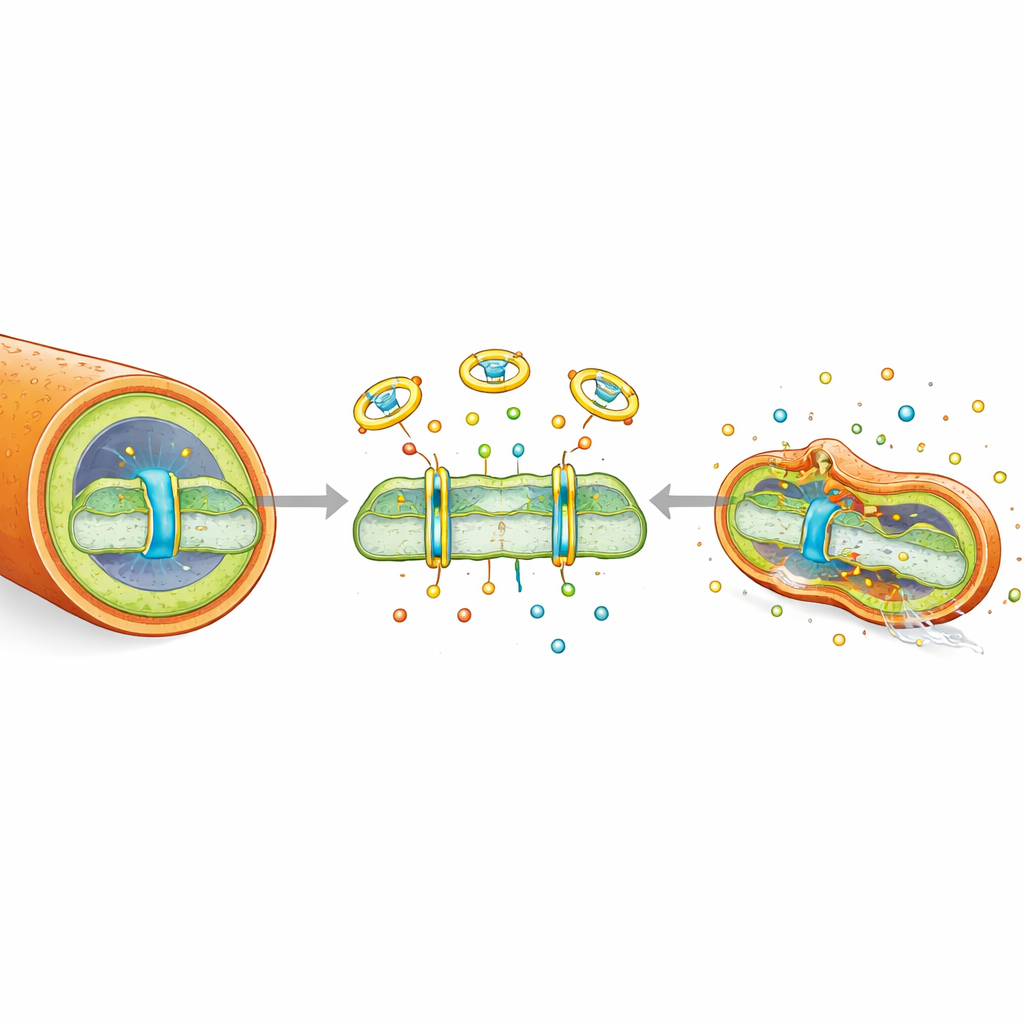
Cibler un élément clé de la construction de la paroi
Pour identifier une cible moléculaire spécifique, les chercheurs ont isolé de rares apparentés du bacille tuberculeux qui avaient spontanément perdu en sensibilité à la dinactine et ont séquencé leurs génomes. La plupart de ces mutants portaient le même changement dans un gène appelé cpsA, qui code pour un membre de la famille de protéines LytR‑Cps2A‑Psr (LCP) impliquées dans l’attachement des composants majeurs de la paroi cellulaire. Lorsque cpsA ou sa protéine partenaire était surexprimé, les bactéries devenaient plus tolérantes à la dinactine ; la suppression de cpsA rendait les cellules plus résistantes sur gélose, mais mettait aussi en évidence que la dinactine a probablement des cibles supplémentaires. À l’aide de modélisation structurale et d’expériences de liaison, l’équipe a montré que la dinactine se lie fortement à la protéine cpsA en un site spécifique, et que la mutation associée à la résistance affaiblit grandement cette interaction. Comme les protéines LCP sont répandues chez les bactéries à Gram positif et absentes de la plupart des espèces à Gram négatif, cette cible contribue à expliquer pourquoi la dinactine attaque préférentiellement le bacille tuberculeux et des organismes apparentés.
Ce que cela pourrait signifier pour le traitement futur de la tuberculose
Pour les non‑spécialistes, le message central est que la dinactine est un composé naturel qui frappe les bacilles tuberculeux à leur point faible : leur approvisionnement en énergie et l’assemblage de leur paroi. Elle agit comme une petite navette d’ions qui décharge la « batterie » bactérienne, prive les cellules d’ATP, perturbe leur chimie interne et interfère avec une protéine cruciale de construction de la paroi. Parallèlement, elle fonctionne de concert avec les médicaments de première ligne, les rendant plus efficaces contre des bactéries résistantes et dormantes. Bien que beaucoup de travail reste à faire — notamment des tests de sécurité et des essais sur des modèles mammifères — cette étude positionne la dinactine et des molécules apparentées comme des éléments prometteurs pour la prochaine génération de thérapies anti‑tuberculeuses.
Citation: Wang, G., Dong, W., Bai, Y. et al. Naturally occurring dinactin targets cpsA protein and kills Mycobacterium tuberculosis by disrupting the proton motive force. Commun Biol 9, 417 (2026). https://doi.org/10.1038/s42003-026-09654-3
Mots-clés: tuberculose, dinactine, résistance aux antibiotiques, métabolisme énergétique bactérien, protéines de la paroi cellulaire