Clear Sky Science · fr
Modélisation à base d’agents des dynamiques cellulaires en thérapie cellulaire adoptive
Pourquoi les cellules « créées par ordinateur » comptent pour la prise en charge du cancer
Les thérapies contre le cancer qui utilisent des cellules immunitaires vivantes transforment la médecine, mais tester chaque nouvelle idée chez l’animal puis chez l’humain est lent, coûteux et parfois risqué. Cette étude présente ABMACT, un laboratoire virtuel qui construit des cellules cancéreuses et immunitaires « numériques » et les fait interagir à l’écran. En rejouant et en prolongeant des expériences réelles, ABMACT aide les chercheurs à voir quelles caractéristiques des thérapies par cellules NK (natural killer) sont les plus déterminantes, et comment ajuster les calendriers de traitement bien avant d’entrer en clinique. 
Transformer les cellules en acteurs numériques
ABMACT repose sur la modélisation à base d’agents, une technique où chaque cellule devient un petit agent logiciel capable de se déplacer, se diviser, mourir ou attaquer ses voisines selon des règles simples. Les auteurs ont conçu quatre acteurs principaux : les cellules tumorales, les NK agressifs capables de tuer les tumeurs, les NK épuisés ayant perdu leur efficacité, et les NK « vigilants » qui restent discrets mais peuvent se réactiver. Les règles décrivant la croissance, l’épuisement, la migration et les transitions d’état de ces cellules sont tirées d’études en laboratoire et sur modèles animaux, puis codées dans la simulation pour que des milliers de cellules virtuelles puissent jouer un court parcours thérapeutique.
Ajouter le câblage interne de la cellule
Le séquençage monocellulaire moderne révèle quels gènes sont actifs dans chaque cellule NK, mais ce niveau moléculaire est difficile à traduire en comportement à l’échelle de l’organisme. ABMACT aborde ce problème en reliant les profils d’activité génique à des traits pratiques, comme la probabilité qu’une cellule NK tue une cellule tumorale ou le nombre de cibles qu’elle peut éliminer avant épuisement. L’équipe a utilisé des données de gènes et de voies issues de modèles murins de lymphome et de tumeur cérébrale pour estimer comment des gènes spécifiques orientent les NK vers un contrôle tumoral plus fort ou plus faible. Ces effets basés sur les gènes sont attribués aléatoirement à des NK virtuels individuels, créant une population numérique qui reflète le mélange naturel d’assassins puissants et plus faibles observé en expérimentation réelle.
Rejouer et prolonger des expériences animales
Les chercheurs ont confronté ABMACT à plusieurs expériences où des NK modifiés étaient utilisés pour traiter des hémopathies et des glioblastomes chez la souris. Dans les modèles de lymphome, le simulateur a correctement reproduit le meilleur contrôle tumoral des NK ingénierés pour exprimer à la fois un récepteur reconnaissant la tumeur et le signal de croissance IL‑15, par rapport à des produits plus simples ou à des cellules non modifiées. Il a non seulement égalé les tailles tumorales mesurées à quelques instants, mais a aussi restitué jour après jour la montée et la décroissance de la charge tumorale, l’expansion des NK, leur épuisement et l’émergence de cellules vigilantes. Dans les modèles de glioblastome, ABMACT a de nouveau suivi le contrôle tumoral observé et a même prédit des résultats dans une étude de co‑culture distincte sans recalibrage, ce qui suggère que ses règles capturent des caractéristiques générales des batailles NK‑tumeur.
Tester des choix thérapeutiques « et si » en silicium
Parce qu’ABMACT fonctionne sur ordinateur, il peut explorer des questions difficiles ou coûteuses à tester en animaux. Les auteurs ont fait varier systématiquement les propriétés cellulaires et les doses pour déterminer quels leviers influent le plus sur le contrôle tumoral. Ils ont trouvé que le ratio cellules NK / cellules tumorales, la capacité de chaque NK à tuer de nombreuses cibles successives, et leur puissance de cytotoxicité de base importent davantage que la simple prolongation de la survie des cellules. Des traitements de suivi simulés ont montré que des doses additionnelles plus précoces et des produits à plus forte capacité létale peuvent prévenir la reprise tumorale plus efficacement que des renforcements tardifs et modestes. Le modèle a aussi exploré comment un mauvais homing des NK, des tissus surpeuplés ou des poches d’hypoxie peuvent retarder les rencontres avec la tumeur et favoriser l’échec du traitement. 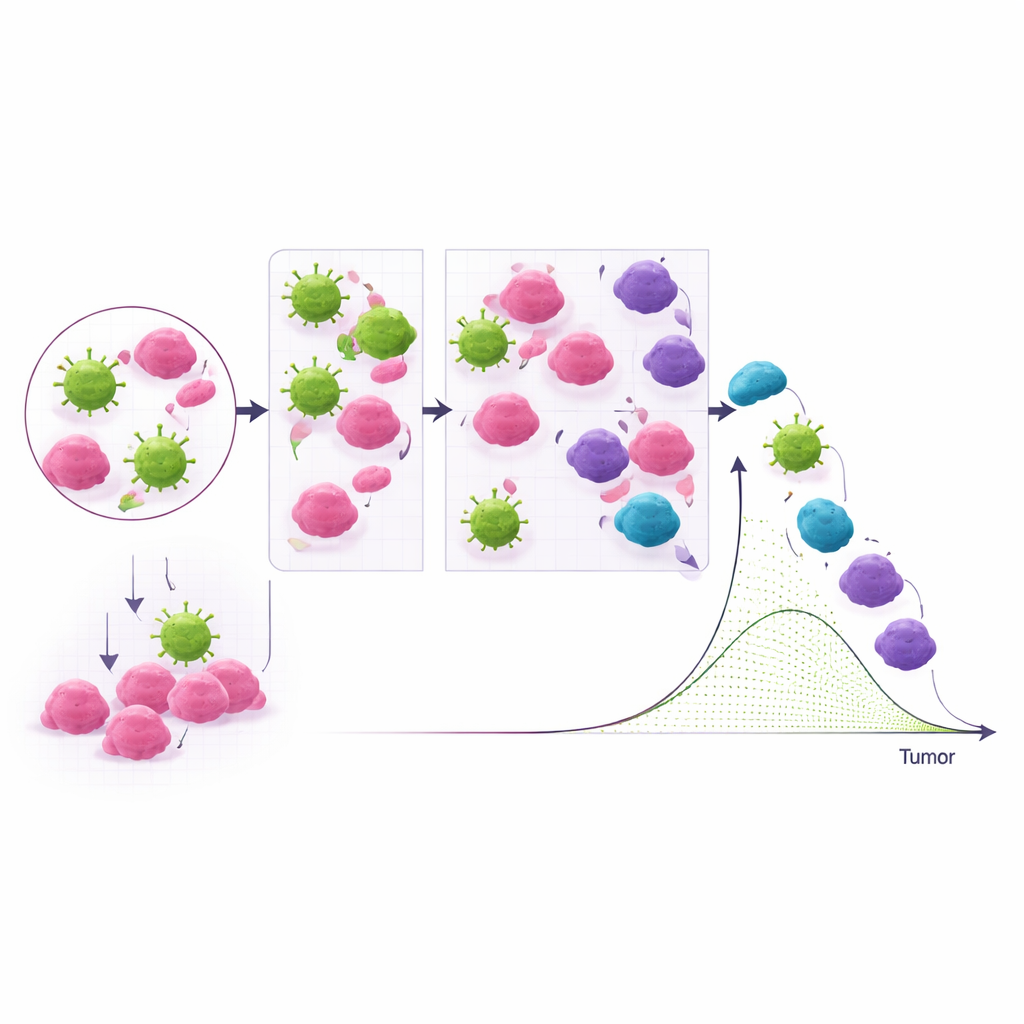
Ce que cela signifie pour les thérapies cellulaires futures
Pour un non‑spécialiste, ABMACT peut être vu comme un simulateur de vol haute résolution pour les thérapies par NK. En ancrant ses cellules numériques dans des données génétiques et expérimentales réelles, le cadre explique pourquoi certains produits NK ingénierés surpassent d’autres et pourquoi des doses plus élevées ne donnent pas toujours de meilleurs résultats. Il souligne des règles de conception pratiques : envoyer suffisamment de NK vers la tumeur, en faire des tueurs sériels puissants, et planifier les traitements tôt et de manière réfléchie, plutôt que d’augmenter simplement la dose. Si de tels modèles ne peuvent remplacer les tests en laboratoire et en clinique, ils peuvent réduire le nombre d’options à tester, diminuer la dépendance aux études animales et, avec le temps, aider à personnaliser les thérapies cellulaires selon la biologie de chaque patient.
Citation: Wang, Y., Casarin, S., Daher, M. et al. Agent-based modeling of cellular dynamics in adoptive cell therapy. Commun Biol 9, 409 (2026). https://doi.org/10.1038/s42003-026-09653-4
Mots-clés: thérapie cellulaire adoptive, cellules NK (natural killer), modélisation à base d’agents, immunothérapie du cancer, CAR-NK