Clear Sky Science · fr
Sélection de modèles dans la recherche préclinique sur les thérapies à base d’acides nucléiques
Transformer des gènes en médicaments
Les thérapies à base d’acides nucléiques constituent une nouvelle catégorie de médicaments qui n’agissent pas en bloquant des protéines, comme le font la plupart des médicaments, mais en intervenant un niveau plus en amont, au niveau de nos messages génétiques. Cette revue explique comment les scientifiques choisissent les modèles cellulaires et animaux appropriés pour tester ces médicaments ciblant l’ARN avant qu’ils n’atteignent les patients. Un lecteur non spécialiste peut s’y intéresser parce que des choix judicieux de modèles peuvent conduire à des traitements génétiques plus rapides, plus sûrs et plus efficaces, notamment pour des maladies infantiles rares et des affections plus courantes comme les maladies cardiovasculaires.
Qu’est‑ce qui rend ces médicaments génétiques différents ?
Les thérapeutiques à base d’acides nucléiques (TAN) comprennent de courtes chaînes appelées oligonucléotides antisens (ASO) et de petits ARN interférents (siRNA). Plutôt que de dépendre de la forme et de la chimie des cibles protéiques, ces médicaments reconnaissent leurs cibles selon les règles d’appariement des bases — les mêmes appariements A‑T et G‑C qui sous‑tendent l’ADN. Cela les rend programmables : une fois que vous connaissez la séquence d’ARN à modifier, vous pouvez souvent concevoir rapidement de nombreux candidats sans des années de chimie traditionnelle. La difficulté n’est plus « Pouvons‑nous fabriquer un composé actif ? » mais « Comment mesurer s’il fonctionne réellement dans un contexte biologique réaliste ? » Parce qu’une seule différence d’une lettre dans la séquence peut activer ou invalider l’efficacité, le choix des systèmes d’essai devient crucial.
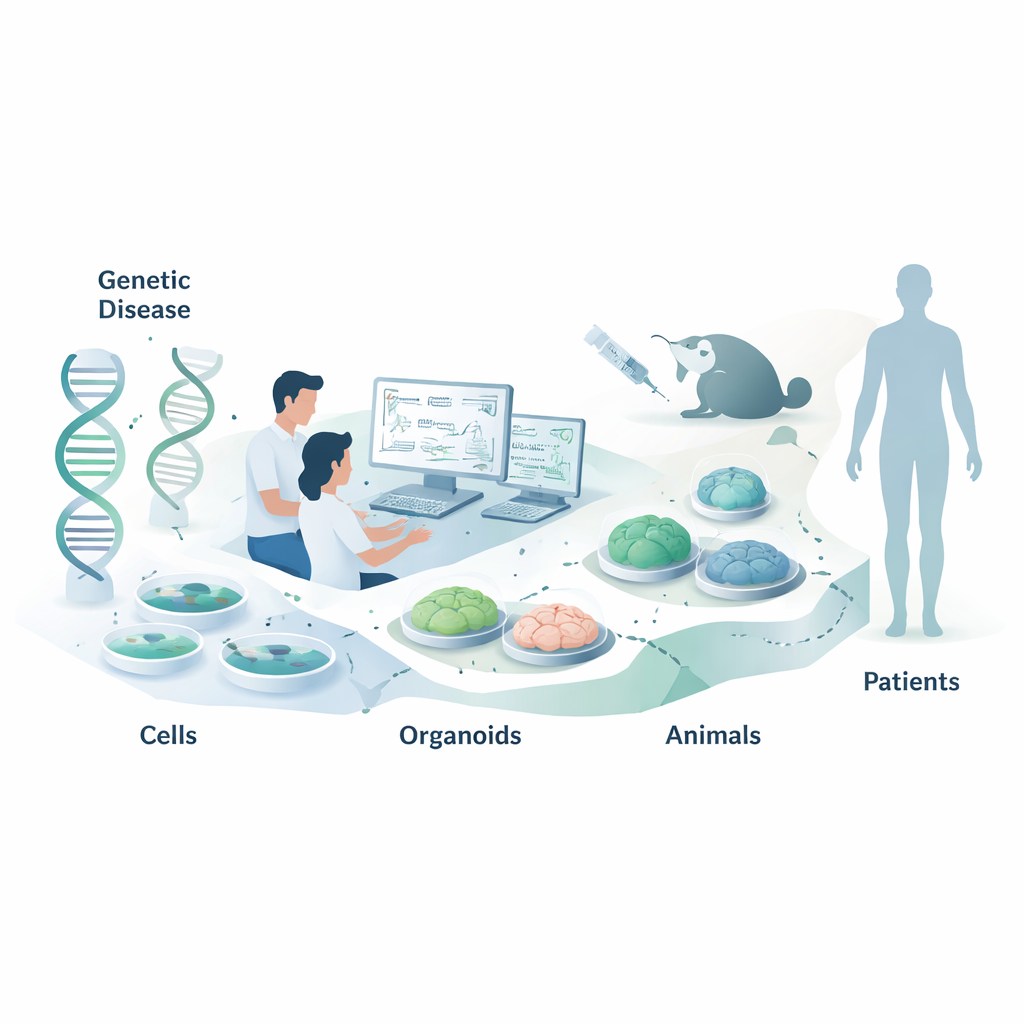
Tests cellulaires simples : rapides mais incomplets
La première étape pour la plupart des TAN est un panel de lignées cellulaires faciles à cultiver, comme HeLa ou HEK293, qui expriment déjà l’ARN cible. Les chercheurs ajoutent de larges bibliothèques d’ASO ou de siRNA candidats puis mesurent la diminution de l’ARN cible et de sa protéine, en utilisant des techniques telles que la PCR et le Western blot. Ils peuvent aussi travailler avec des cellules issues de patients, qui reflètent mieux le contexte génétique individuel et permettent de tester des médicaments « sélectifs d’allèle » qui n’inhibent que la copie défaillante d’un gène. Lorsque le gène naturel n’est pas exprimé de manière pratique, les scientifiques introduisent parfois des mini‑gènes artificiels ou des plasmides rapporteurs qui s’illuminent lorsque l’ARN est coupé ou épissé correctement. Ces systèmes sont puissants pour comparer rapidement de nombreuses conceptions, mais ils peuvent manquer des détails importants, tels que la structure naturelle de l’ARN ou le traitement spécifique à un type cellulaire, si bien que les résultats doivent être confirmés dans des contextes plus réalistes.
Des corrections moléculaires au comportement cellulaire réel
Beaucoup de TAN visent non seulement à détruire un ARN défectueux mais à le réparer en modifiant l’épissage, le processus qui recoud les segments du message génétique. Des ASO conçus avec soin peuvent amener les cellules à omettre un exon nuisible, restaurer une portion manquante ou empêcher l’insertion d’un « pseudo‑exon » qui brouille le code. Pour savoir si ces modifications améliorent réellement la fonction cellulaire, les chercheurs dépassent les simples mesures d’ARN et de protéine. Dans des cellules dérivées de patients, ils testent si l’activité enzymatique revient, si le transport d’ions dans les cellules pulmonaires se normalise, ou si les voies de signalisation des cellules immunitaires répondent correctement. De plus en plus, ils utilisent des organoïdes tridimensionnels — mini‑tissus cultivés à partir de cellules souches de patients — qui peuvent reproduire des battements cardiaques, l’activité des réseaux cérébraux ou d’autres comportements complexes. Ces modèles 3D se rapprochent des organes réels mais sont plus difficiles, plus lents et plus coûteux à exploiter, si bien que les équipes doivent équilibrer réalisme et débit d’expérimentation.
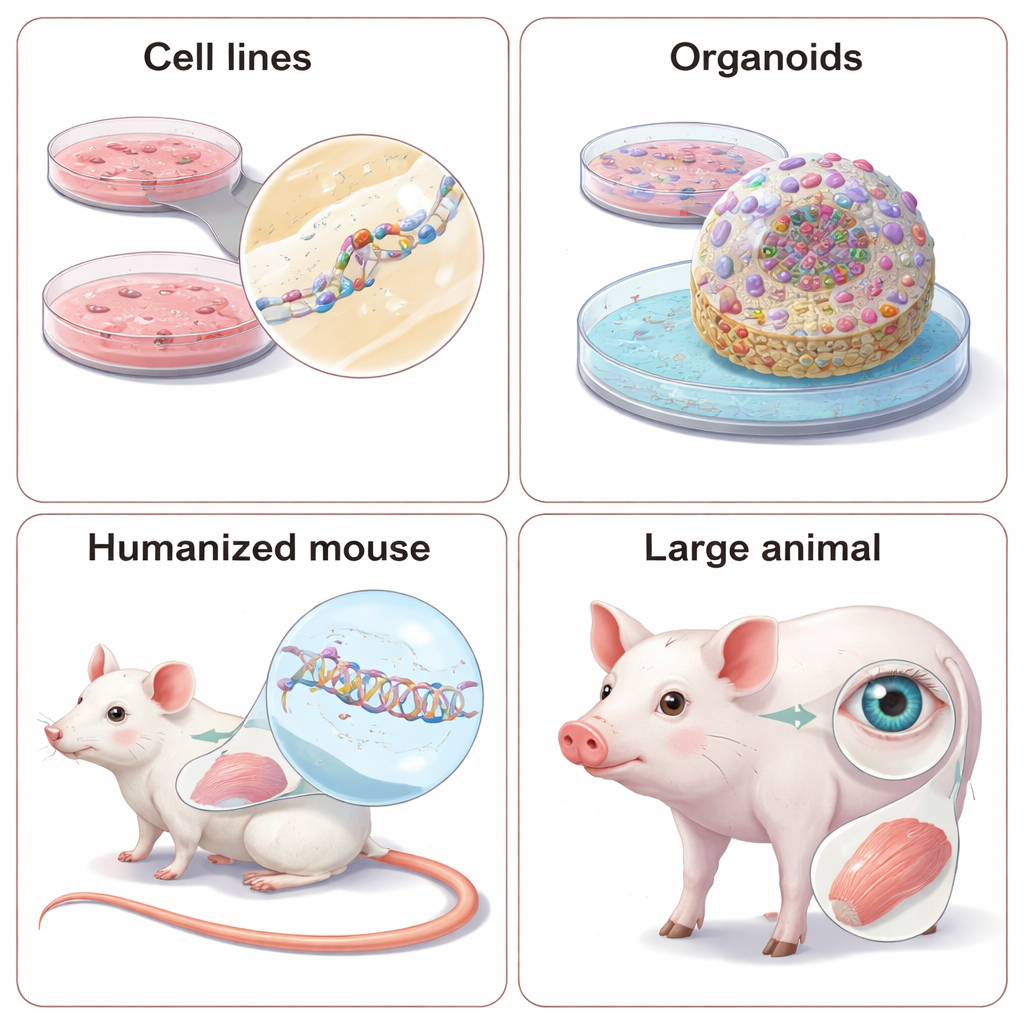
Pourquoi les animaux restent importants — et comment les humaniser
Certaines caractéristiques des maladies, comme le métabolisme à l’échelle de tout l’organisme, les interactions entre organes ou le comportement, ne peuvent tout simplement pas être reproduites en boîte de culture. Pour cela, les TAN sont testées chez des animaux vivants. Parce que ces médicaments dépendent de séquences d’ARN exactes, les scientifiques sont confrontés à un choix : concevoir des médicaments « substituts » qui correspondent à la version animale du gène, ou ré‑ingénier l’animal pour qu’il porte des séquences génétiques humaines. Les ASO et siRNA substituts peuvent révéler si l’abaissement d’un gène améliore les symptômes dans des modèles murins bien établis, mais ils ne reproduisent pas parfaitement le médicament ciblant l’humain. Les modèles humanisés — des souris ou même des mini‑cochons portant des segments ou des copies entières de gènes humains — permettent de tester le candidat clinique réel mais exigent un temps et des coûts importants, et des différences subtiles dans la régulation des gènes entre espèces peuvent encore réserver des surprises. La revue souligne également l’usage croissant d’animaux de grande taille, en particulier pour les maladies de l’œil et du muscle, où l’anatomie ressemble davantage à celle des humains.
Perspectives : des modèles plus intelligents et moins d’incertitude
Les auteurs concluent qu’il n’existe pas un « meilleur » modèle unique pour les médicaments à base d’acides nucléiques ; chaque projet nécessite plutôt une voie sur mesure qui commence par des essais rapides et simples et progresse vers des systèmes plus complexes et plus pertinents pour l’humain. À mesure que les autorités de régulation et les financeurs poussent à réduire l’utilisation des animaux, on s’attend à ce que des organoïdes sophistiqués, des dispositifs organ‑on‑a‑chip et des modèles informatiques prennent une part croissante du travail, surtout lorsqu’ils sont combinés à des outils d’apprentissage automatique qui prédisent quelles séquences et quelles chimies fonctionneront le mieux. En fin de compte, en comprenant les forces et les angles morts de chaque modèle — et en partageant les bonnes pratiques et les données au sein du domaine — les chercheurs peuvent transformer de manière plus fiable des idées génétiques programmables en médicaments sûrs et efficaces pour les patients.
Citation: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Mots-clés: thérapies à base d’acides nucléiques, oligonucléotides antisens, siRNA, modèles précliniques, thérapie génique