Clear Sky Science · fr
La liaison sélective des cations divalents remodèle la mécanique des nucléosomes et libère la dynamique des queues d’histones
Comment de minuscules ions aident à gérer notre ADN
À l’intérieur de chaque cellule, des mètres d’ADN doivent être repliés, empaquetés, et pourtant rester accessibles à la demande. Cet article explore comment deux ions minéraux courants dans nos cellules, le magnésium et le calcium, modifient subtilement la façon dont l’ADN s’enroule autour des protéines, influençant la compaction de notre matériel génétique et sa lisibilité. En simulant ces interactions au détail atomique, les auteurs montrent que des variations de la concentration ionique peuvent raidir ou détendre des structures d’ADN locales et changer le comportement des queues protéiques flexibles qui aident à organiser les chromosomes.
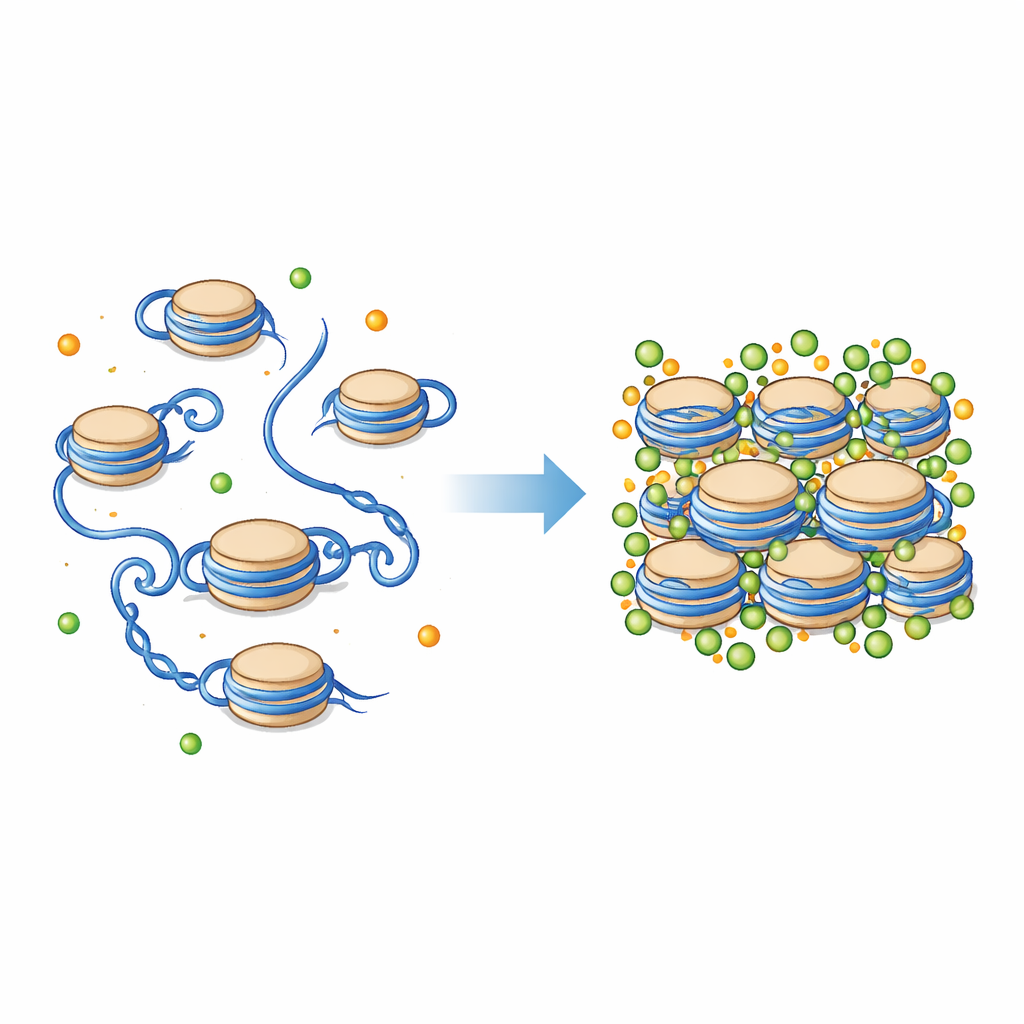
La perle au cœur de l’empaquetage des chromosomes
L’ADN de nos cellules n’est pas laissé libre ; il est enroulé autour d’enrouleurs protéiques appelés nucléosomes. Chaque nucléosome est un court segment d’ADN enroulé autour d’un agrégat de protéines histones, avec des queues flexibles qui s’étendent vers l’extérieur. Ensemble, ces unités forment la structure de base en « perles sur un fil » de la chromatine, qui peut ensuite se plier en fibres plus compactes. L’environnement autour des nucléosomes est rempli de particules chargées, y compris le magnésium (Mg²⁺) et le calcium (Ca²⁺). On sait que ces ions favorisent la condensation des chromosomes, mais la manière dont ils influent sur les détails mécaniques des nucléosomes et de leurs queues d’histones a été difficile à observer directement.
Simuler un monde atomique encombré
Pour révéler ces détails, les auteurs ont exécuté 81 microsecondes de simulations informatiques à grande échelle dans lesquelles chaque atome d’ADN, de protéine, d’eau et d’ions était modélisé explicitement. Ils ont fait varier systématiquement les niveaux de magnésium et de calcium, testé différentes descriptions du comportement des ions dans les simulations, et étudié des nucléosomes avec et sans leurs queues d’histones. En comparant les schémas de liaison ionique simulés avec des mesures expérimentales, ils ont identifié un modèle affiné qui correspond le mieux à la façon dont les nucléosomes réels attirent ces ions, où le magnésium préfère les sillons de l’ADN et le calcium saisit plus souvent l’épine dorsale de l’ADN et certains sites protéiques acides.
Comment les ions compriment l’ADN et raidissent le cœur
Les simulations montrent que les ions divalents se regroupent le long de la surface de l’ADN et dans l’espace étroit entre les deux tours d’ADN qui enroulent chaque nucléosome. En neutralisant partiellement la forte charge négative de l’ADN, ces ions réduisent la répulsion électrique entre les tours adjacents d’ADN. Le résultat est que les deux spires d’ADN se rapprochent, le nucléosome devient légèrement plus court et sa rigidité mécanique augmente, comme le mesure un modèle traitant le nucléosome comme un petit cylindre élastique. Cette rigidité accrue ne provient pas d’un détachement ou d’un déroulement majeur de l’ADN ; elle résulte plutôt de changements subtils d’espacement et de mouvements plus coordonnés de régions spécifiques de l’ADN, qui se déplacent ensemble comme une unité plus rigide.
Libérer les queues protéiques flottantes
Alors que le cœur d’ADN devient plus compact et rigide, les queues flexibles des histones réagissent en sens inverse. En conditions de faibles ions, des acides aminés positivement chargés de ces queues s’agrippent à l’ADN négatif, formant de nombreux contacts stables. Lorsque le magnésium ou le calcium se lient le long de l’ADN, ils masquent ces charges, affaiblissant l’attraction entre les queues et l’ADN. Les auteurs constatent que les contacts entre les queues — en particulier celles de l’histone H3 — et l’ADN diminuent, que les temps de résidence sur l’ADN raccourcissent et que les queues explorent une gamme plus large de positions. Cela signifie que les queues interagissent avec l’ADN par des rencontres plus fréquentes mais plus brèves, devenant plus dynamiques et potentiellement plus libres d’atteindre des nucléosomes voisins.
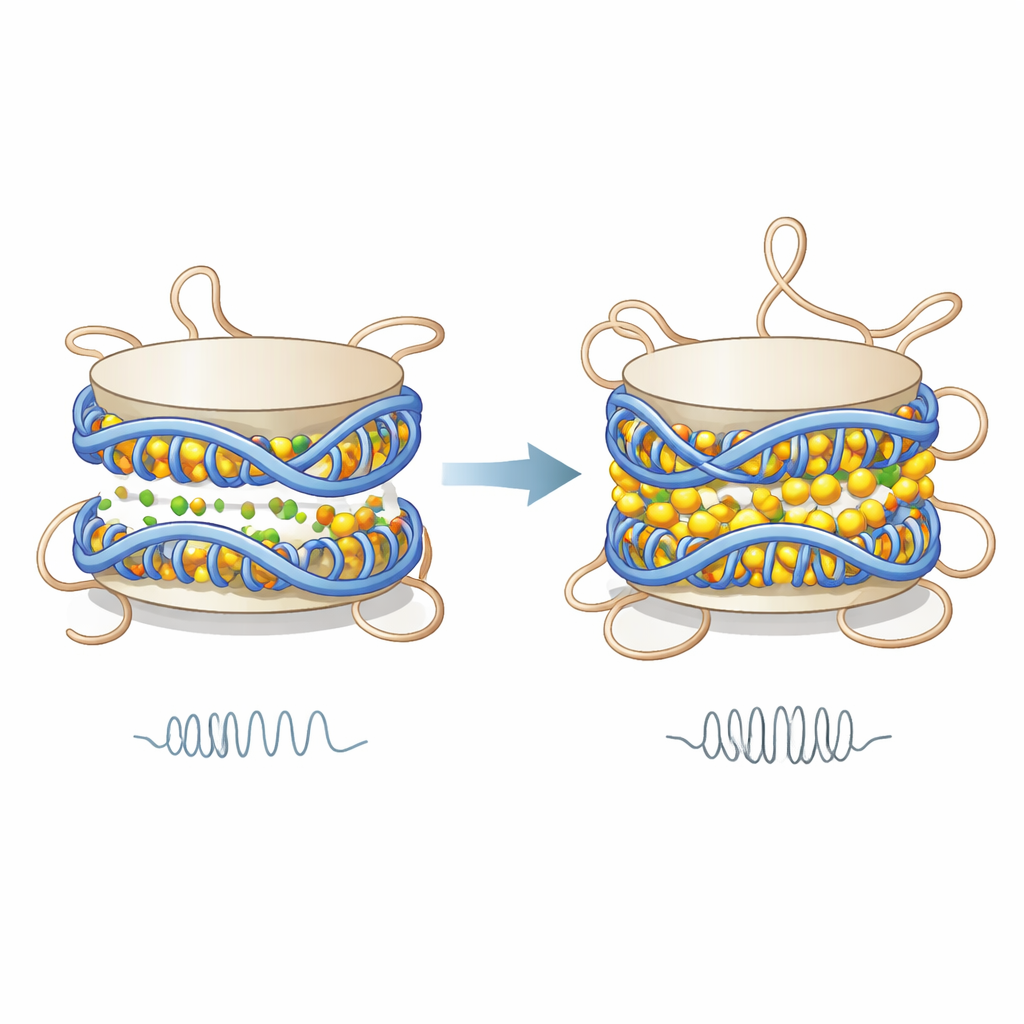
Ce que cela signifie pour le contrôle des gènes et l’état de la chromatine
Ensemble, ces résultats décrivent un double rôle pour le magnésium et le calcium dans la chromatine. En resserrant l’enroulement de l’ADN et en augmentant la rigidité des nucléosomes, ils favorisent une chromatine plus compacte et moins flexible. Parallèlement, en relâchant les contacts entre queues d’histones et ADN et en accroissant le mouvement des queues, ils exposent des sites clés susceptibles d’être modifiés chimiquement ou reconnus par des protéines régulatrices. Parce que les concentrations d’ions dans le noyau fluctuent avec les signaux et l’usage énergétique, ce travail suggère que de petites variations chimiques dans l’environnement cellulaire peuvent ajuster à la fois la sensation mécanique des nucléosomes et l’accessibilité de leurs queues régulatrices, contribuant à ouvrir ou fermer des fenêtres d’opportunité pour l’activité génique.
Citation: Hu, G., Zhang, H., Xu, W. et al. Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics. Commun Biol 9, 365 (2026). https://doi.org/10.1038/s42003-026-09648-1
Mots-clés: chromatine, mécanique des nucléosomes, ions magnésium et calcium, queues d’histones, régulation des gènes