Clear Sky Science · fr
Wnt11 médie l’interaction fibroblaste–cellule musculaire lisse pour promouvoir la fibrose vésicale neurogène chez le rat
Quand les nerfs défaillent, la vessie cicatrise
De nombreuses personnes atteintes de lésions de la moelle épinière, de sclérose en plaques ou de maladie de Parkinson développent une « vessie neurogène », où les nerfs endommagés ne contrôlent plus correctement le stockage et l’évacuation de l’urine. Avec le temps, la paroi vésicale peut devenir épaisse et rigide, envahie par un tissu cicatriciel, ce qui menace la santé des reins et la qualité de vie. Cette étude réalisée chez le rat identifie un acteur moléculaire clé de cette cicatrisation et suggère de nouvelles pistes pour ralentir voire prévenir les dégâts.
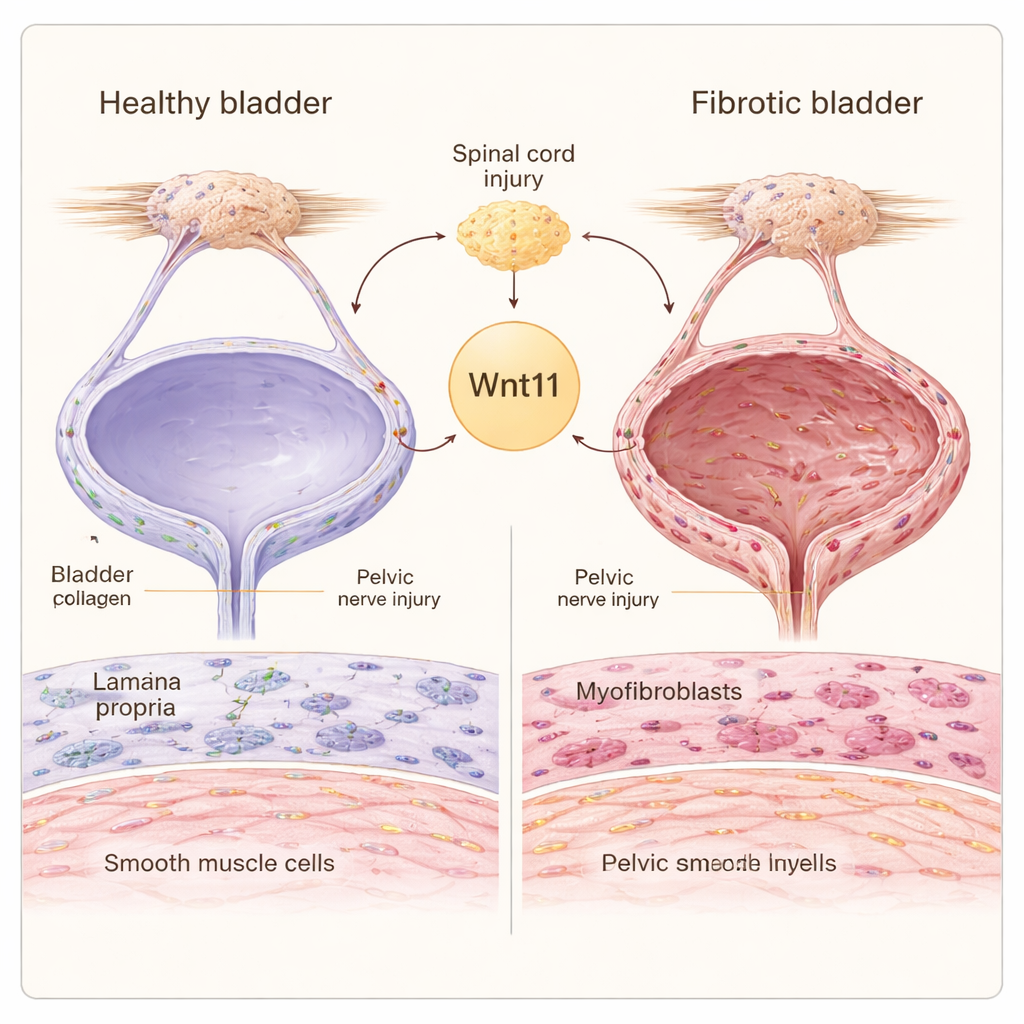
Un coût caché des dommages nerveux
Lorsque les nerfs qui desservent la vessie sont blessés, que ce soit au niveau de la moelle épinière ou près du pelvis, l’organe doit travailler davantage pour gérer l’urine. La paroi vésicale contient deux types cellulaires de soutien principaux : les fibroblastes, qui fabriquent le matériau de soutien autour des cellules, et les cellules musculaires lisses, qui se contractent pour expulser l’urine. Dans la vessie neurogène, les fibroblastes peuvent se transformer en myofibroblastes hautement actifs qui produisent un excès de collagène, tandis que les cellules musculaires lisses passent d’un état fin et contractile à un état plus volumineux et synthétique. Ensemble, ces changements déposent un tissu cicatriciel rigide qui réduit la capacité de la vessie à se distendre et à se vider.
Une molécule de signalisation au premier plan
Les chercheurs se sont concentrés sur une famille de protéines de communication cellulaire appelées ligands Wnt, connues pour réguler la croissance tissulaire et la cicatrisation dans d’autres organes. En analysant des vessies de rats présentant des lésions nerveuses, ils ont constaté qu’un membre de cette famille, Wnt11, était constamment et fortement augmenté dans les vessies fibrosées causées soit par une lésion de la moelle épinière, soit par l’écrasement d’un nerf pelvien. Les niveaux de Wnt11 augmentaient à la fois dans les fibroblastes et dans les cellules musculaires lisses, et la quantité de Wnt11 corrélait avec la gravité de la dysfonction vésicale. Lorsque des cellules vésicales normales en culture étaient exposées à un autre facteur pro-fibrosant, le TGF-β1, elles augmentaient également leur production de Wnt11, suggérant une boucle d’amplification entre ces deux signaux.
Du message chimique à la cicatrice durable
Pour vérifier si Wnt11 est un simple témoin ou un véritable moteur, l’équipe a ajouté une protéine Wnt11 supplémentaire à des rats avec une lésion nerveuse et a aussi bloqué la sécrétion de Wnt avec un médicament appelé LGK974. L’apport supplémentaire de Wnt11 a agrandi les vessies, aggravé les profils de pression pendant le remplissage et la vidange, épaissi la couche musculaire et augmenté le dépôt de collagène. Le blocage de la sécrétion de Wnt a eu l’effet inverse, améliorant les troubles urinaires et réduisant le tissu cicatriciel. In vitro, Wnt11 a poussé les fibroblastes vers le statut de myofibroblaste et incité les cellules musculaires lisses vers le phénotype synthétique favorisant la fibrose. L’extinction du gène Wnt11 a atténué ces changements, montrant clairement que Wnt11 est un accélérateur central du remodelage vésical.
Comment les cellules décodent le signal de fibrose
En approfondissant, l’étude a cartographié la voie reliant Wnt11 à la membrane cellulaire aux modifications géniques dans le noyau. Wnt11 se lie à un récepteur nommé Vangl2 sur les fibroblastes et les cellules musculaires lisses de la vessie. Ce partenariat n’utilise pas la voie Wnt classique impliquant la protéine β-caténine ; au contraire, il active une chaîne différente appelée voie de la polarité cellulaire planaire (PCP). Ici, Wnt11 et Vangl2 recrutent une protéine adaptatrice appelée DVL2, qui active ensuite l’enzyme JNK. JNK active à son tour les facteurs de transcription c-JUN et NFAT5, qui se déplacent dans le noyau et contribuent à l’activation de gènes pro-fibrotiques. La voie TGF-β1, bien connue pour promouvoir la cicatrisation, converge physiquement et fonctionnellement avec cette route Wnt11–Vangl2–JNK, de sorte que les deux signaux se renforcent mutuellement à la membrane plasmique et dans le noyau.
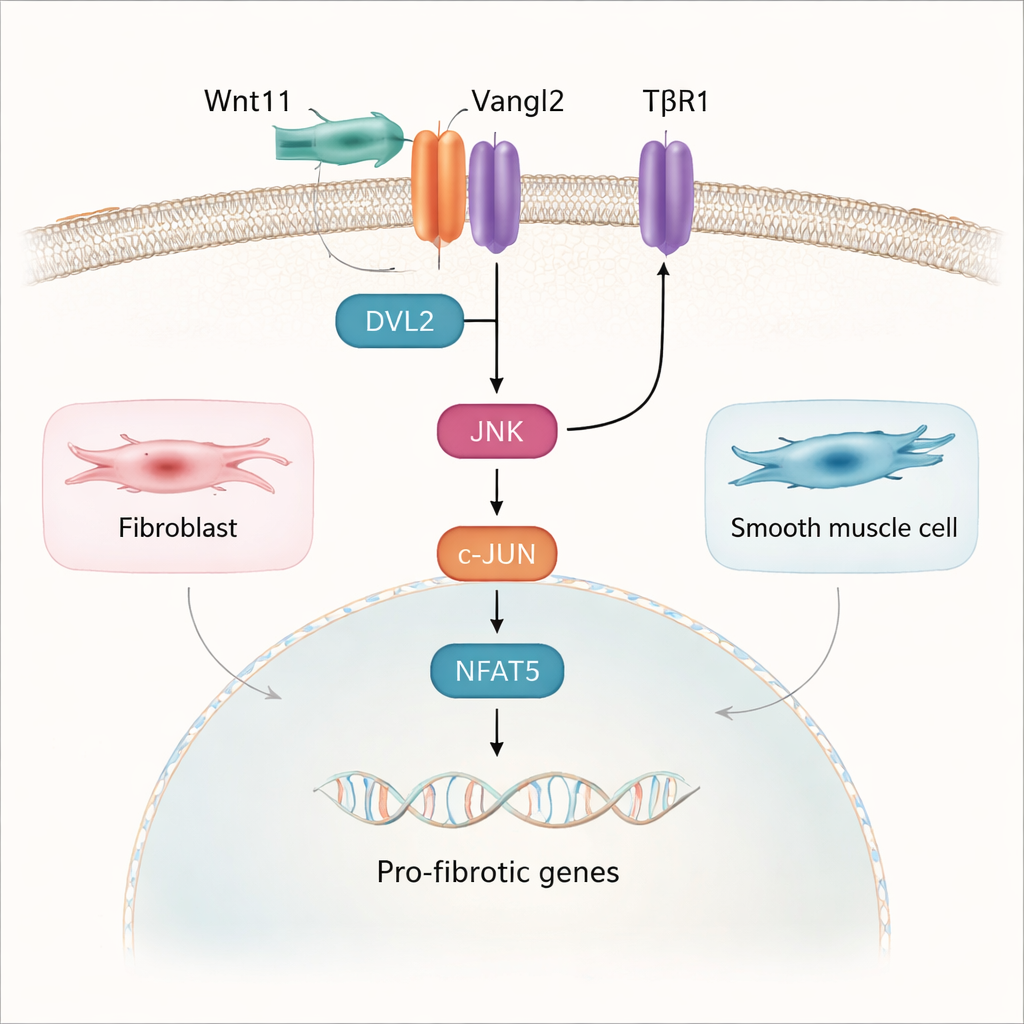
Vers des vessies plus souples et en meilleure santé
Parce que Wnt11 et le TGF-β1 coopèrent pour durcir la vessie, l’équipe a testé des médicaments qui bloquent des étapes clés des deux voies. Chez des rats présentant une vessie neurogène, l’inhibition combinée du récepteur TGF-β TβR1 et de l’enzyme JNK a donné les meilleurs résultats : vessies plus petites, parois musculaires plus fines, moins de collagène et amélioration du stockage et de l’évacuation de l’urine par rapport à un traitement par un seul médicament. Pour le grand public, la conclusion est qu’un signal induit par une lésion nerveuse, Wnt11, contribue à convertir les cellules de soutien et les cellules musculaires normales en cellules formant des cicatrices. Interrompre ce signal, en particulier en association avec des bloqueurs classiques du TGF-β, pourrait constituer la base de futurs traitements visant non seulement à gérer les symptômes, mais aussi à préserver la structure et la fonction de la vessie chez les personnes atteintes de vessie neurogène.
Citation: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
Mots-clés: vessie neurogène, fibrose, Wnt11, cellules musculaires lisses, signalisation TGF-β