Clear Sky Science · fr
Des voies parallèles dépendantes de Tbr2 régulent le développement de sous-types distincts d'ipRGC
Comment nos yeux disent l'heure et la forme
Au-delà de former des images, nos yeux régulent discrètement l'horloge interne, contrôlent l'ouverture de la pupille et aident à évaluer la luminosité globale. Une petite population de neurones rétiniens spécialisés, appelés cellules ganglionnaires rétiniennes intrinsèquement photosensibles (ipRGC), prend en charge une grande partie de ces fonctions. Elles répondent à la lumière grâce à un pigment nommé mélanopsine et envoient des signaux vers des zones profondes du cerveau. Cette étude pose une question fondamentale aux implications larges : comment un groupe précoce de cellules nerveuses en développement se scinde-t-il en plusieurs types d'ipRGC distincts, chacun câblé pour une tâche différente ?
Un interrupteur maître, plusieurs types de cellules photoréceptrices
Dans la rétine de souris, les six sous-types d'ipRGC connus proviennent tous d'une population précoce de cellules ganglionnaires qui activent un gène appelé Tbr2. Ce gène fonctionne comme un interrupteur maître, déclenchant les programmes nécessaires à la fabrication des ipRGC et au maintien de l'expression du gène de la mélanopsine, Opn4. Mais un seul interrupteur maître ne suffit pas à expliquer comment six variétés différentes d'ipRGC émergent, chacune ayant des formes, des réponses à la lumière et des cibles cérébrales spécifiques. Les auteurs ont utilisé le séquençage ARN de rétines de souris en développement pour chercher des gènes dont l'activité dépend de Tbr2. Parmi un petit nombre de candidats, deux se sont démarqués : Irx1 et Tbx20, tous deux connus comme régulateurs de l'identité cellulaire dans d'autres tissus. 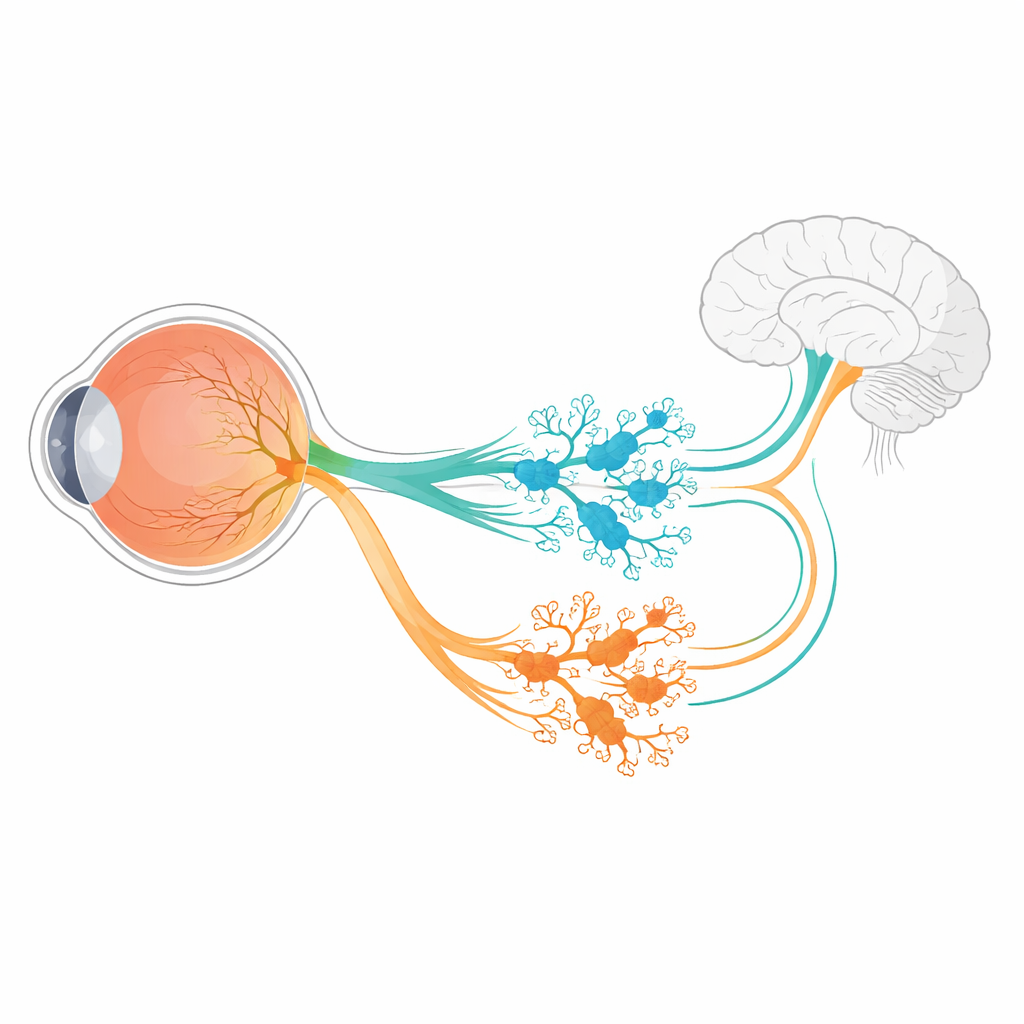
Deux voies qui se séparent à l'intérieur de la rétine
En utilisant des lignées de souris nouvellement conçues qui balisent les cellules exprimant Irx1 et Tbx20 par des marqueurs fluorescents ou enzymatiques, les chercheurs ont tracé où et quand ces facteurs s'allument. Ils ont trouvé qu'Irx1 et Tbx20 apparaissent dans des groupes chevauchants de jeunes cellules ganglionnaires rétiniennes vers la mi-gestation, puis se séparent rapidement pour former des ensembles presque complètement distincts à l'âge adulte. Irx1 se retrouve principalement dans trois types d'ipRGC étiquetés M3, M4 et M5, tandis que Tbx20 se concentre dans les cellules M1, M2 et M6, avec seulement un recoupement mineur dans certaines cellules M3 et M5. Des images détaillées, des enregistrements électriques et des traçages des projections cérébrales ont montré que chaque facteur marque une collection distincte d'ipRGC avec des dispositions dendritiques, des réponses à la lumière et des schémas de projection vers des régions cérébrales spécifiques impliquées dans la régulation de l'horloge, les réflexes et le traitement visuel.
Interrupteurs qui règlent la sensibilité à la lumière et la survie cellulaire
L'équipe a ensuite étudié ce qui se passe lorsque chaque facteur est supprimé. Lorsque Irx1 a été éliminé dans la rétine en développement, le nombre et la structure de base des ipRGC marquées par Irx1 restaient en grande partie intacts, mais leurs niveaux de mélanopsine chutaient fortement. En d'autres termes, Irx1 s'est avéré essentiel pour activer pleinement le programme Opn4 de détection de la lumière dans les cellules M3, M4 et M5, sans être nécessaire à la formation initiale de ces cellules. Tbx20 a montré un comportement différent. La suppression de Tbx20 a non seulement réduit l'expression d'Opn4 mais a aussi diminué d'environ moitié le nombre d'ipRGC positifs pour Tbx20 et a ensuite réduit la survie de ces cellules. Cela indique que Tbx20 contribue à la fois à la construction et au maintien de certains sous-types d'ipRGC, en particulier M1, M2 et M6, tout en soutenant leur sensibilité à la lumière basée sur la mélanopsine. 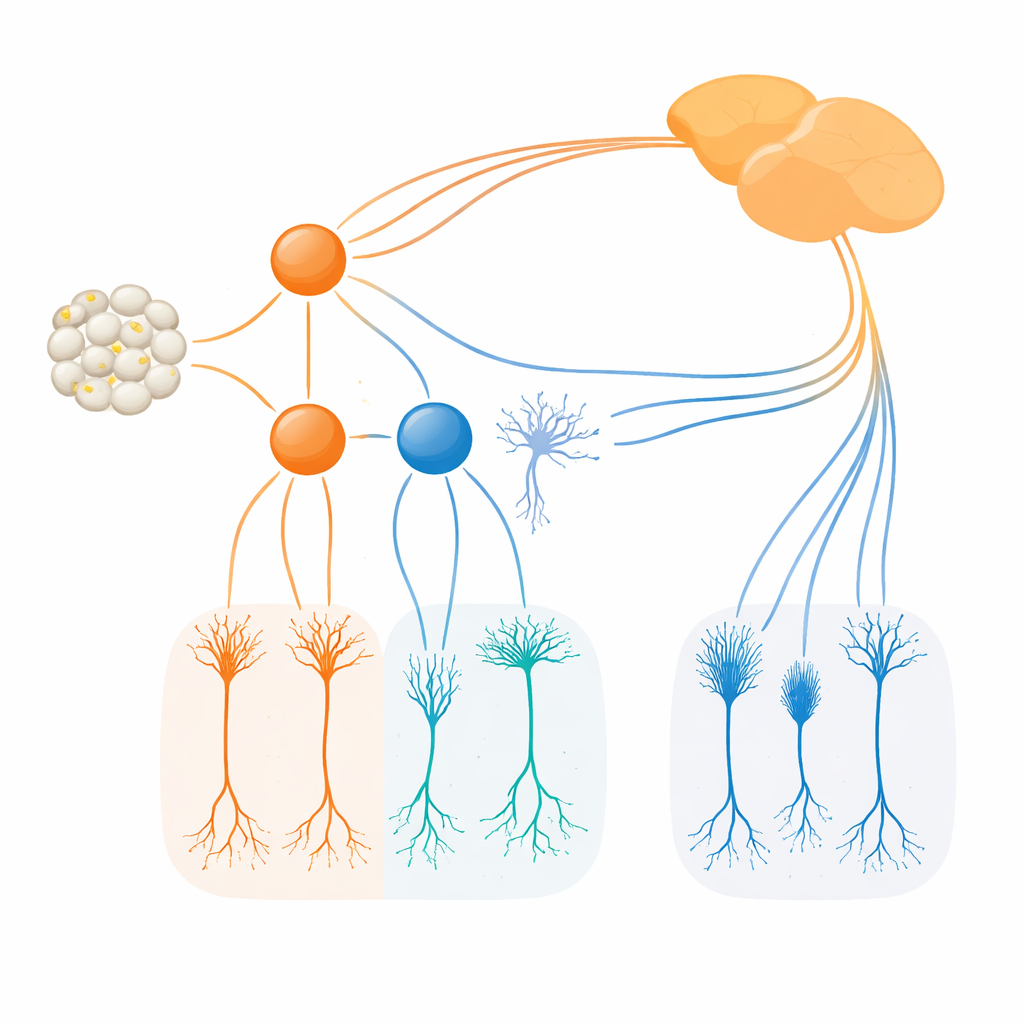
Minutage de la séparation en familles cellulaires distinctes
En activant brièvement des traceurs génétiques à des jours embryonnaires précis, les auteurs ont pu « datestamper » les cellules exprimant Irx1 ou Tbx20 et suivre leur sort jusqu'à l'âge adulte. Ces expériences ont montré que les cellules marquées par Tbx20 se déterminent à leur identité finale d'ipRGC légèrement plus tôt que celles marquées par Irx1, la plupart des décisions étant verrouillées juste avant la naissance. Pendant une courte fenêtre, Irx1 et Tbx20 peuvent être co-exprimés dans certaines cellules, et des souris double knockout dépourvues des deux gènes ont montré une perte de cellules ipRGC positives pour la mélanopsine bien plus importante que dans les mutants simples. Cela suggère que les deux voies coopèrent transitoirement, puis divergent pour guider différents sous-ensembles d'ipRGC le long de trajectoires développementales séparées.
Ce que cela signifie pour la compréhension de la vision et de la santé
Pour un non-spécialiste, le message principal est qu'un seul gène précoce, Tbr2, n'agit pas seul. Il s'inscrit plutôt dans deux voies de contrôle parallèles, l'une centrée sur Irx1 et l'autre sur Tbx20. Ces voies déterminent quel type d'ipRGC une cellule jeune deviendra, ajustent l'intensité de sa détection de la lumière et définissent si elle se connectera à des régions cérébrales impliquées dans la régulation de l'horloge corporelle, les réflexes pupillaires ou d'autres fonctions visuelles. Ce travail propose un schéma de câblage plus clair pour la construction de nos « compteurs de lumière » internes et met en évidence des étapes génétiques spécifiques qui pourraient intervenir lorsque ces cellules sont perdues ou dysfonctionnent, avec des implications potentielles pour les troubles du sommeil, les variations saisonnières de l'humeur et les maladies qui endommagent la rétine.
Citation: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Mots-clés: cellules ganglionnaires rétiniennes, mélanopsine, développement neuronal, rythmes circadiens, facteurs de transcription