Clear Sky Science · fr
L’analyse structurale révèle que des molécules d’eau médiatisent l’auto‑activation de GPR99
Pourquoi ce récepteur compte pour l’inflammation
Nos voies respiratoires et d’autres tissus détectent en permanence des signaux chimiques indiquant une infection ou une irritation. L’un de ces capteurs, une protéine appelée GPR99 située à la surface des cellules, apparaît comme un commutateur important dans des maladies inflammatoires telles que l’asthme et les polypes nasaux. Cette étude explique, en détail atomique, comment GPR99 peut s’activer tout seul même sans déclencheur chimique externe — et comment de petits amas d’eau l’aident à le faire — fournissant des indices pour concevoir de nouveaux médicaments anti‑inflammatoires.
Un interrupteur intégré à l’intérieur d’un capteur cellulaire
GPR99 appartient à une grande famille de protéines de surface cellulaire qui transmettent des messages de l’extérieur vers l’intérieur de la cellule, souvent en changeant de conformation et en recrutant des protéines partenaires appelées protéines G. Contrairement à la plupart de ces récepteurs, GPR99 est exceptionnellement actif même lorsqu’aucun ligand n’est lié. Les auteurs montrent qu’une boucle flexible du côté externe de GPR99, connue sous le nom de deuxième boucle extracellulaire, se comporte comme une clé interne : elle se replie dans la poche de liaison habituelle, imitant un signal activateur et activant le récepteur par elle‑même.
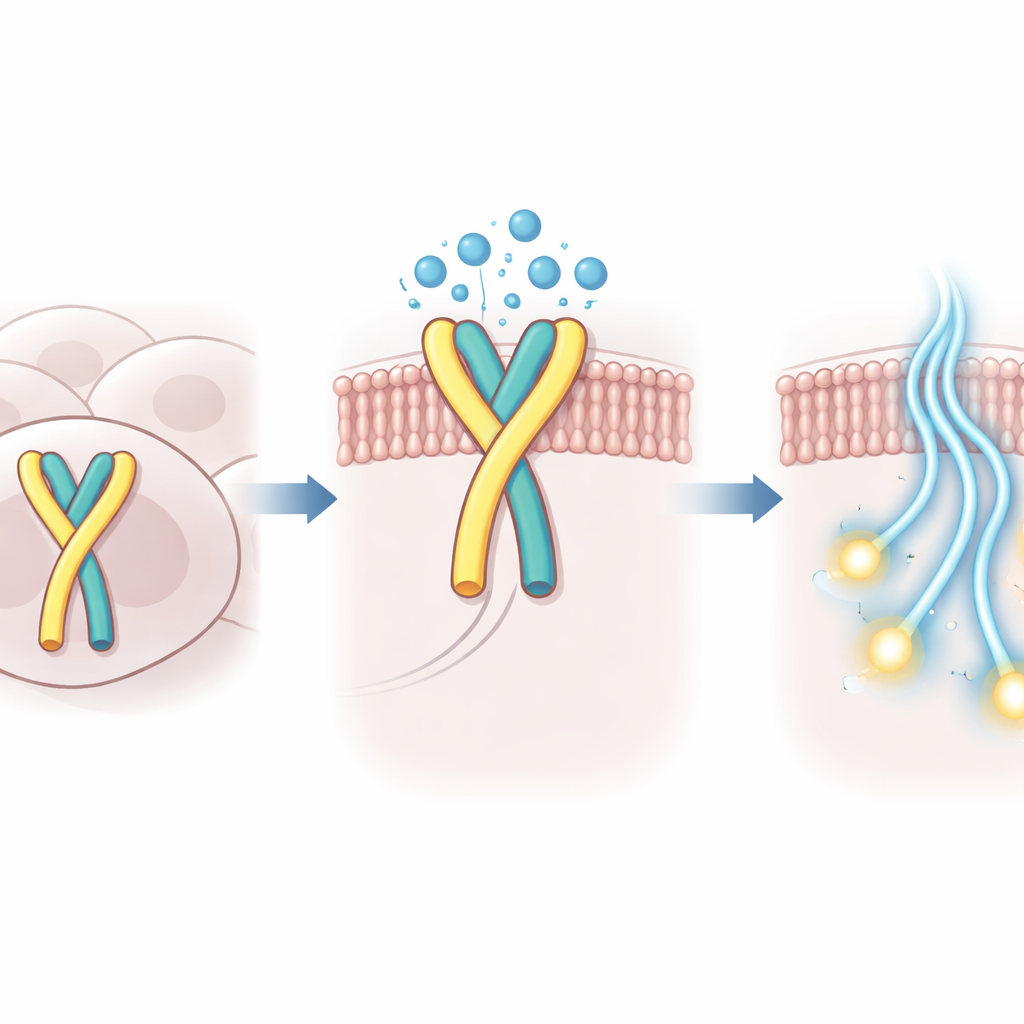
Comment l’eau aide à maintenir l’interrupteur en place
À l’aide de la cryo‑microscopie électronique à haute résolution, les chercheurs ont capturé la structure tridimensionnelle de la GPR99 humaine liée à sa protéine G partenaire dans cet état auto‑activé. Dans la poche de liaison où se placeraient normalement des molécules externes, ils ont observé non seulement la boucle repliée mais aussi un petit groupe de molécules d’eau ordonnées. Ces molécules d’eau forment un pont polaire entre la boucle et la protéine environnante, compensant l’insertion plus superficielle de la boucle et stabilisant la conformation active du récepteur. Lorsque des acides aminés clés de la boucle ou de la poche voisine ont été modifiés de façon à affaiblir ces contacts médiés par l’eau, l’activité intrinsèque de GPR99 a chuté nettement dans des tests cellulaires.
Réarranger le mécanisme interne pour un signalement constant
L’équipe a comparé leur structure auto‑activée à d’autres membres de la famille, y compris un récepteur étroitement apparenté qui lie le sous‑produit métabolique succinate et une forme active de GPR99 liée au métabolite 2‑oxoglutarate. Ils ont constaté que GPR99, en l’absence de tout ligand externe, est déjà pleinement prêt dans une conformation active : plusieurs « micros‑interrupteurs » conservés au sein de son cœur hélicoïdal adoptent des formes normalement observées uniquement lorsque ces récepteurs sont stimulés. Des positions critiques qui contribuent habituellement à maintenir les récepteurs à l’état éteint sont remplacées ou réorientées dans GPR99, relâchant les contraintes internes et favorisant la configuration ouverte qui accueille la protéine G partenaire.
Transmettre le message à l’intérieur de la cellule
Du côté interne de la membrane, la structure révèle comment GPR99 saisit la protéine G de type Gq qui transmet son signal. Une queue hélicoïdale de la protéine G s’insère dans une cavité ouverte par le balancement externe d’une des hélices de GPR99, établissant un réseau de contacts polaires et hydrophobes avec les boucles internes et la queue du récepteur. Des mutations perturbant cette interface réduisent aussi la signalisation, confirmant que l’auto‑activation créée par la boucle externe et le cluster d’eau est efficacement couplée aux partenaires intracellulaires. Ensemble, ces instantanés structuraux relient les changements à la surface externe du récepteur aux vagues de signalisation calcique qu’il déclenche à l’intérieur des cellules.
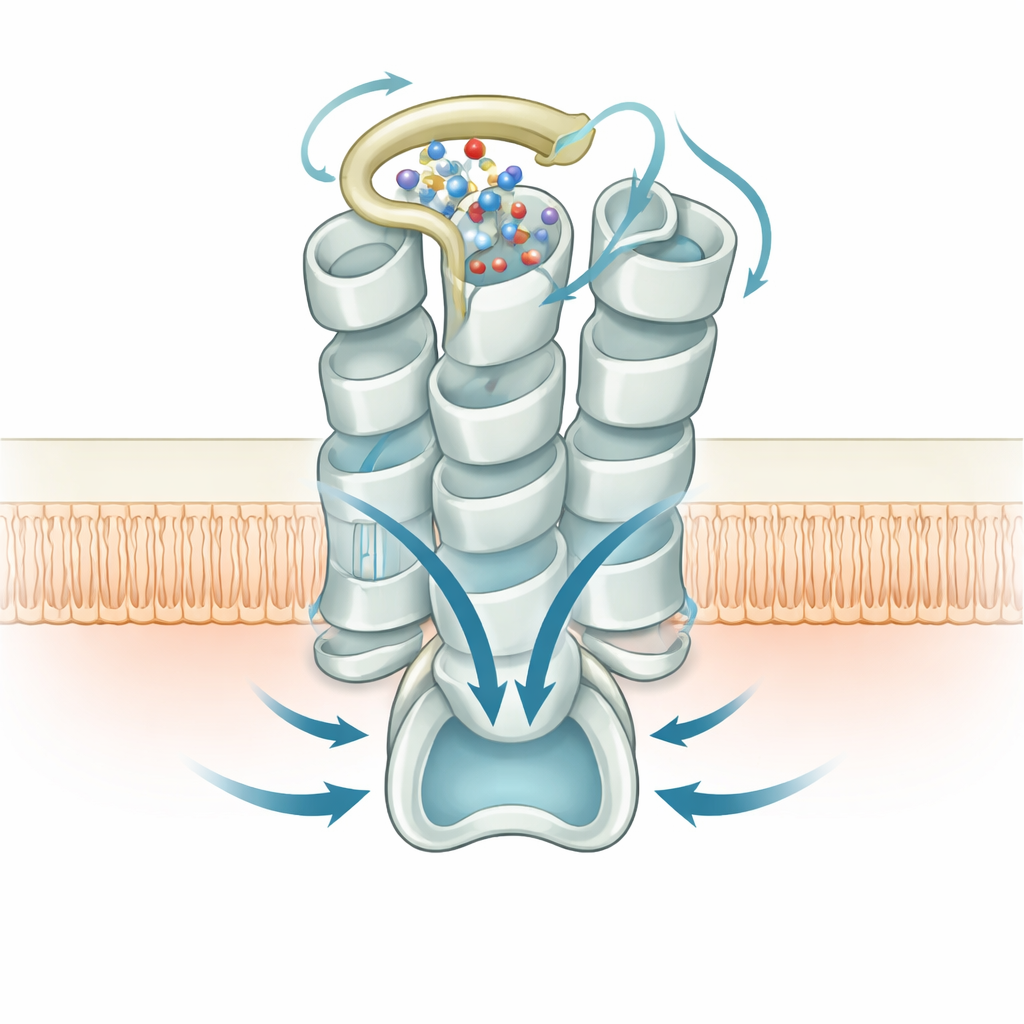
Conséquences pour la respiration et au‑delà
Les auteurs proposent que l’activité intrinsèque de GPR99, renforcée par des molécules d’eau structurales, puisse maintenir les tissus des voies respiratoires en mode « veille » — prêts à libérer du mucus et à déclencher une réponse immunitaire lorsque des lipides inflammatoires ou des changements métaboliques apparaissent. Parce que GPR99 est fortement actif même sans signaux externes, et parce que son activation repose sur une configuration spécifique boucle‑et‑eau, ces aperçus structuraux offrent des cibles concrètes pour les concepteurs de médicaments. De petites molécules qui perturbent cet interrupteur interne ou son réseau d’eau pourraient atténuer une inflammation excessive, tandis que des composés modulant finement l’interaction pourraient exploiter la sensibilité de GPR99 à des fins thérapeutiques.
Citation: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Mots-clés: GPR99, activation des GPCR, biologie structurale, inflammation, signalisation médiée par l’eau