Clear Sky Science · fr
Mécanisme structurel de blocage par un anticorps anti-CMH-I des récepteurs inhibiteurs des cellules NK dans l’immunité antitumorale
Déverrouiller les tues-cancer silencieux de l’organisme
Notre système immunitaire dispose d’un ensemble de sentinelles puissantes appelées cellules tueuses naturelles (NK) capables de détecter et de détruire les cellules cancéreuses et infectées par des virus. Pourtant, les tumeurs apprennent souvent à réduire au silence ces sentinelles. Cet article révèle, au niveau atomique, comment un anticorps spécialement conçu peut retirer ce « bouton muet », rendant aux cellules NK leur activité pour qu’elles attaquent plus efficacement les tumeurs. Le travail combine biologie structurale de pointe et expériences chez la souris pour montrer comment un seul anticorps pourrait compléter les immunothérapies anticancéreuses existantes.
Les étiquettes d’identité immunitaire à la surface de nos cellules
Chaque cellule de notre corps affiche à sa surface des « étiquettes » moléculaires appelées molécules du CMH de classe I. Ces étiquettes aident les cellules immunitaires à distinguer le tissu normal des cellules devenues dangereuses parce que cancéreuses ou infectées par des virus. Les cellules NK scrutent en permanence ces étiquettes. Lorsqu’elles détectent des motifs normaux, des récepteurs inhibiteurs à la surface des NK envoient un signal calmant qui empêche l’attaque. Les tumeurs conservent souvent ces étiquettes visibles, s’en servant comme d’un bouclier protecteur : tant que le signal inhibiteur circule, les NK retiennent leur action et le cancer peut se développer.
Un anticorps qui saisit le bouclier
Les chercheurs ont étudié un anticorps monoclonal nommé B1.23.2 qui se lie fortement à de nombreuses variantes humaines du CMH de classe I présentes sur les cellules tumorales. En utilisant la cryo‑microscopie électronique et la cristallographie aux rayons X, ils ont cartographié précisément la façon dont cet anticorps se positionne sur la surface du CMH. B1.23.2 s’accroche à une crête conservée de la molécule de CMH — une hélice α2 — sans toucher la chaîne légère associée et ne ressentant que faiblement le peptide présenté. Ceci signifie que l’anticorps peut reconnaître une large gamme de molécules HLA-A, -B et -C humaines avec une affinité très élevée, tout en étant relativement insensible aux fragments protéiques spécifiques que le CMH expose.
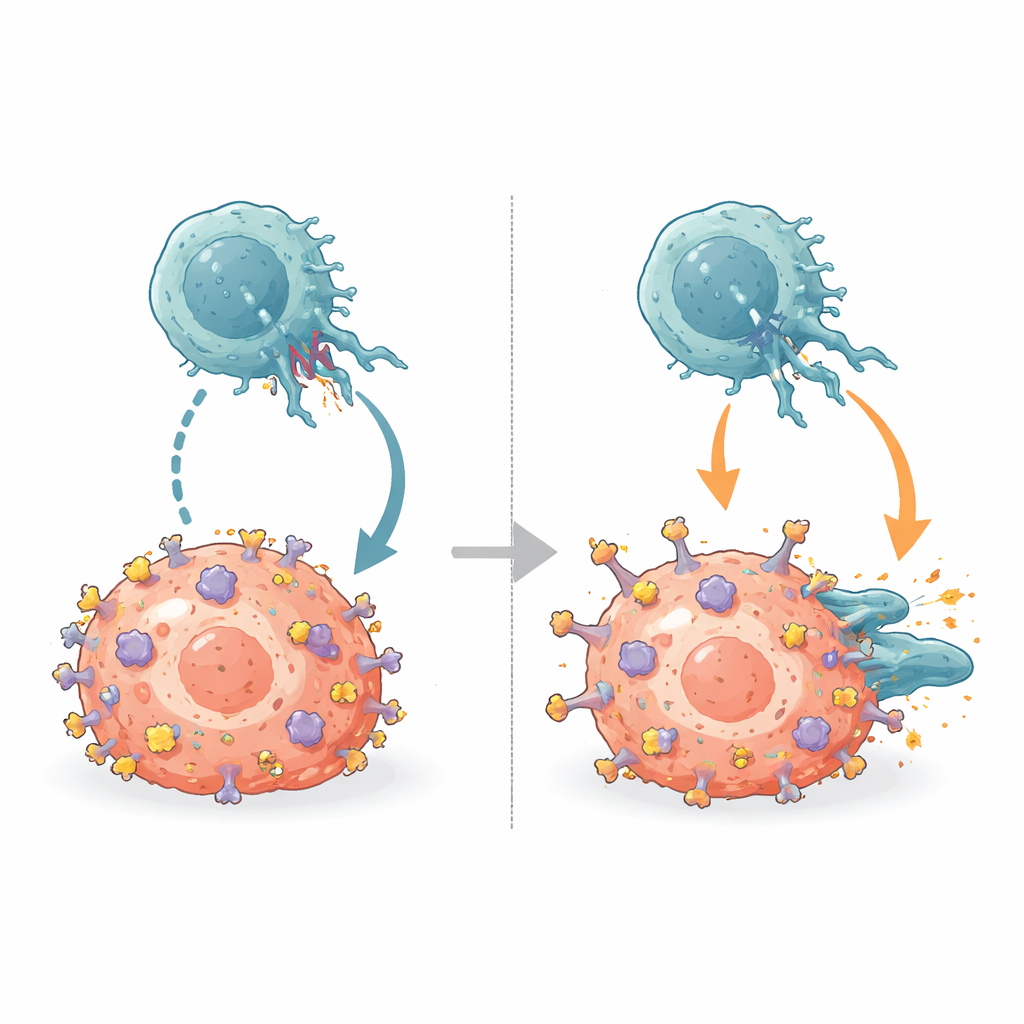
Déloger les freins immunitaires
Les cellules NK portent des récepteurs inhibiteurs appelés KIR qui se fixent normalement sur la même crête α2 du CMH. En alignant les nouvelles structures anticorps–CMH avec des structures connues KIR–CMH, l’équipe a montré que B1.23.2 occupe physiquement la zone du CMH dont les KIR ont besoin pour s’accrocher. Le site de liaison de l’anticorps et l’empreinte des KIR se chevauchent tellement que les deux ne peuvent simplement pas se lier simultanément. B1.23.2 se lie également plus fortement au CMH que les KIR, ce qui lui fait gagner cette lutte moléculaire. En conséquence, lorsque l’anticorps enrobe les molécules de CMH des cellules tumorales, les KIR des NK ne peuvent plus délivrer leurs signaux inhibiteurs, faisant basculer l’équilibre vers l’activation des NK.
Ajuster l’appairage et étendre la portée
Bien que B1.23.2 cible principalement la surface conservée du CMH, les auteurs ont constaté que de petites différences dans le peptide lié au CMH peuvent moduler finement la force de liaison de l’anticorps. En substituant systématiquement un seul résidu d’acide aminé dans le peptide, ils ont observé des variations modestes de l’affinité — généralement d’environ un facteur dix — sans perte de reconnaissance globale. Ils ont aussi exploré pourquoi certains types courants de CMH, tels que HLA‑A*02:01, échappent à la liaison. En transplantant des résidus de contact clé d’un variant de CMH réactif dans HLA‑A*02:01, l’équipe a construit des versions que l’anticorps pouvait désormais reconnaître, confirmant précisément quelles positions forment la surface d’amarrage critique. Ces découvertes suggèrent que des variantes d’anticorps futures pourraient être conçues pour couvrir encore plus de types de CMH ou, au contraire, les éviter sélectivement.
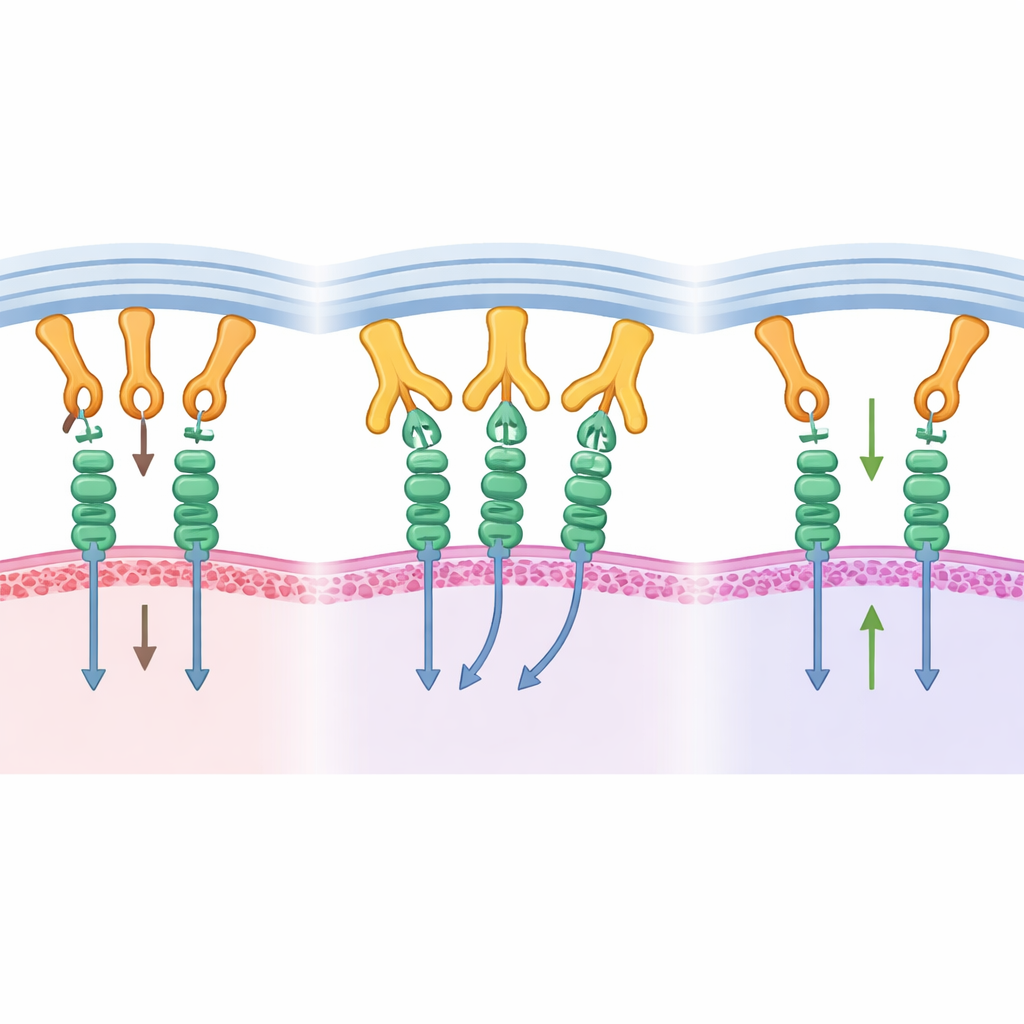
Transformer l’insight structural en contrôle tumoral
Est‑ce que ce blocage moléculaire aide réellement à combattre les tumeurs ? Pour le tester, les chercheurs ont utilisé un modèle murin humanisé portant un cancer pancréatique humain. Ils ont conçu une forme de B1.23.2 incapable de signaler via sa queue Fc, de sorte que tout effet découlerait principalement du blocage de l’interaction CMH–KIR. Lorsque des souris ont reçu l’anticorps en présence de cellules NK humaines, la croissance tumorale a été considérablement ralentie. Les NK ont montré une prolifération accrue, une plus grande activité des voies de croissance et de signalisation, et une production renforcée de molécules inflammatoires associées à la destruction des cellules cancéreuses. Au sein des tumeurs, les NK affichaient davantage de récepteurs activateurs, cohérent avec une libération d’une inhibition continue.
Ce que cela pourrait signifier pour les thérapies anticancer futures
En termes simples, cette étude montre comment un seul anticorps peut se glisser entre les cellules tumorales et les freins du système immunitaire, interrompant le signal « ne pas attaquer » qui maintient normalement les NK en silence. En cartographiant l’interaction à résolution atomique et en confirmant ses effets chez l’animal, ce travail offre une feuille de route pour une nouvelle classe de traitements : des anticorps qui se lient aux étiquettes d’identité tumorales plutôt qu’aux récepteurs immunitaires eux‑mêmes. De tels agents pourraient être combinés aux inhibiteurs de points de contrôle existants ou aux thérapies cellulaires pour mobiliser à la fois les NK et les lymphocytes T, offrant au système immunitaire un angle d’attaque supplémentaire contre les cancers difficiles à traiter.
Citation: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Mots-clés: cellules tueuses naturelles, CMH de classe I, immunothérapie du cancer, anticorps monoclonaux, récepteurs inhibiteurs