Clear Sky Science · fr
LukS-PV ciblant C5aR inhibe l’EMT dans le carcinome hépatocellulaire via l’axe BCL6/HDAC6/HSPD1
Transformer une arme bactérienne en combattant du cancer
Le carcinome hépatocellulaire, la forme la plus fréquente de cancer du foie, est souvent mortel parce qu’il se propage du foie vers d’autres organes. Cet article explore un allié inattendu contre cette dissémination : une protéine, LukS-PV, issue à l’origine d’une toxine produite par la bactérie Staphylococcus aureus. Les chercheurs montrent comment cette protéine se fixe sur un récepteur spécifique des cellules du cancer du foie et, au lieu d’endommager les tissus normaux, bloque des étapes clés qui permettent aux cellules tumorales de se détacher, migrer et former de nouvelles tumeurs.
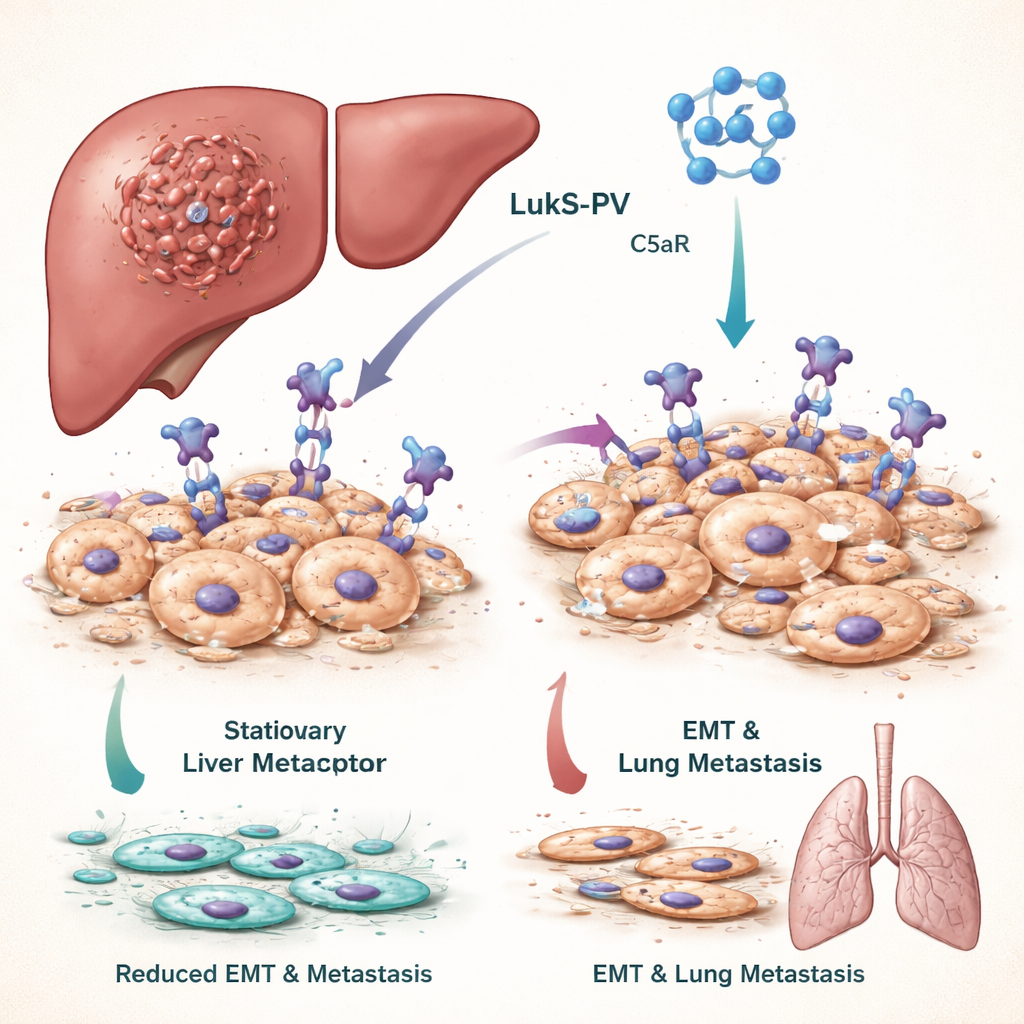
Pourquoi arrêter les cellules cancéreuses qui changent de forme est important
Pour que le cancer du foie se propage, les cellules tumorales doivent subir un changement majeur de forme et de comportement appelé transition épithélio–mésenchymateuse, ou EMT. Lors de l’EMT, des cellules normalement serrées et immobiles deviennent plus souples, mobiles et invasives, ce qui leur permet de s’insinuer dans les vaisseaux sanguins et de coloniser des organes distants comme les poumons. Les patients dont les tumeurs présentent une forte activité d’EMT ont généralement un pronostic plus mauvais. L’équipe s’est concentrée sur une voie de signalisation pilotée par une molécule appelée C5a et son récepteur C5aR, qui est anormalement abondant sur de nombreuses cellules tumorales et connu pour favoriser l’EMT et les métastases.
Un composant de toxine qui cible un signal cancéreux
La leucocidine de Panton–Valentine, une toxine de Staphylococcus aureus, contient un composant nommé LukS-PV qui reconnaît et se lie naturellement à C5aR. Des travaux antérieurs des auteurs ont montré qu’une version recombinante, non-formant de pores, de LukS-PV peut freiner la croissance de plusieurs cancers sans toxicité évidente chez l’animal. Dans cette étude, ils ont traité des lignées cellulaires de cancer du foie avec LukS-PV et ont observé que les cellules devenaient moins migratoires et invasives. Des analyses moléculaires ont révélé que les marqueurs de cellules stationnaires et bien différenciées augmentaient, tandis que les marqueurs de cellules agressives et mobiles diminuaient. Chez des souris injectées avec des cellules de cancer du foie, le traitement par LukS-PV a entraîné beaucoup moins de nodules tumoraux dans les poumons, indiquant une réduction des métastases.
Bloquer une réaction en chaîne à l’intérieur des cellules tumorales
En approfondissant, les chercheurs ont mis au jour une chaîne de protéines de contrôle à l’intérieur des cellules cancéreuses que LukS-PV perturbe. D’abord, LukS-PV se lie à C5aR à la surface cellulaire et bloque efficacement le signal pro-métastatique émis par C5a. Cet affaiblissement de la signalisation de C5aR diminue les niveaux d’une protéine nommée BCL6, un facteur de transcription qui active normalement certains gènes dans le noyau. L’un des cibles de BCL6 est HDAC6, une enzyme qui retire de petits groupes chimiques appelés groupes acétyle d’autres protéines. Lorsque BCL6 est abondant, les niveaux de HDAC6 augmentent, rendant la cellule plus susceptible d’entrer en EMT et de migrer. L’interférence de LukS-PV avec C5aR réduit BCL6, ce qui à son tour diminue la production de HDAC6 et ralentit ce programme pro-métastatique.
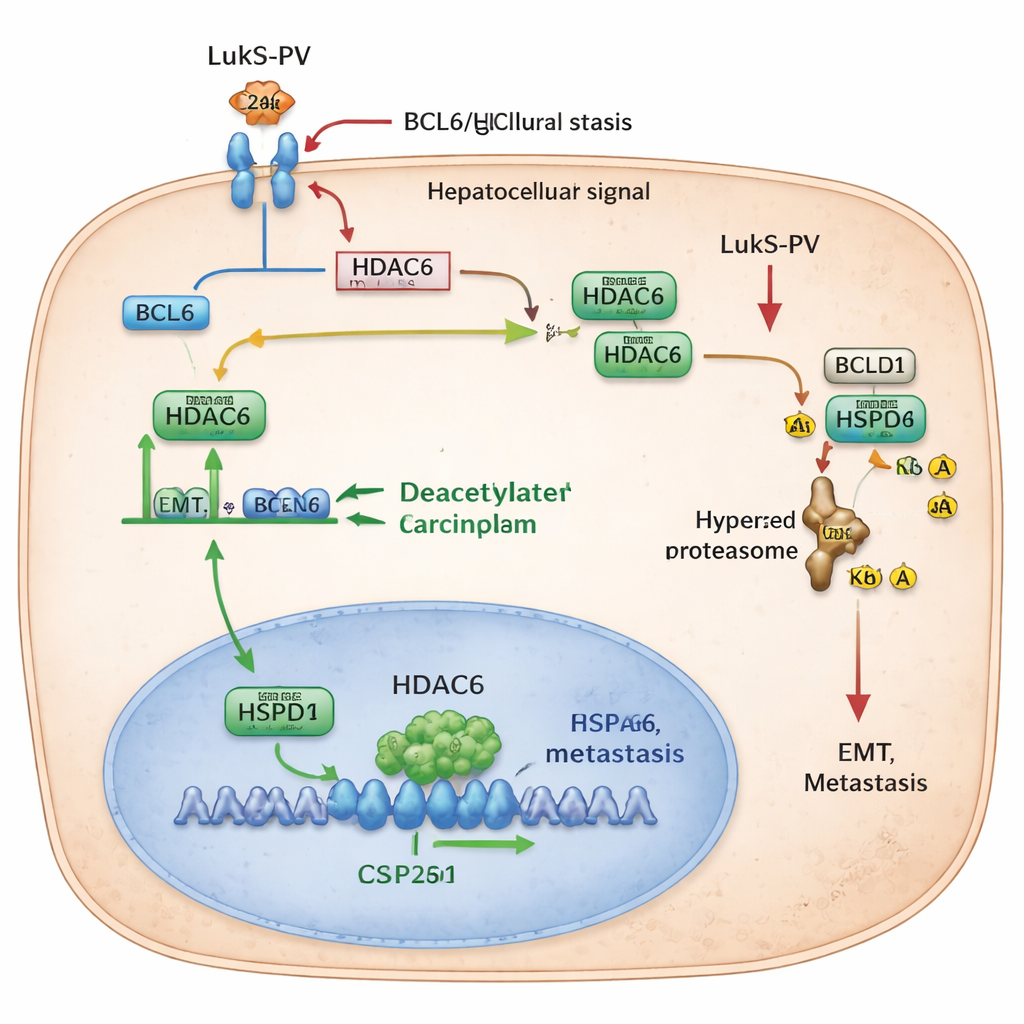
Marquer une chaperonne pour destruction
L’équipe a ensuite identifié un partenaire clé de HDAC6 appelé HSPD1, également connu sous le nom de HSP60, une protéine chaperonne qui aide d’autres protéines à se replier et à rester stables. Dans le cancer du foie, les niveaux de HSPD1 sont plus élevés que dans les tissus normaux adjacents et sont liés à une survie moindre des patients. Les chercheurs ont découvert que HDAC6 interagit physiquement avec HSPD1 et lui enlève des groupes acétyle à deux positions spécifiques. Quand ces marques acétyles sont retirées, HSPD1 devient plus stable et favorise l’EMT et les métastases. Lorsque HDAC6 est réduit — soit par des manipulations génétiques soit par le traitement par LukS-PV — HSPD1 devient plus acétylée. Cette forme hyperacétylée est reconnue par le système d’élimination cellulaire, marquée par l’ubiquitine et dégradée. À mesure que les niveaux de HSPD1 diminuent, les cellules cancéreuses perdent une partie de leur capacité à migrer, envahir et coloniser les poumons.
Des voies complexes à une conclusion simple
Pour un non-spécialiste, le message est que les auteurs ont cartographié un effet domino à l’intérieur des cellules du cancer du foie : un récepteur de surface (C5aR) augmente une protéine contrôleur (BCL6), qui élève une enzyme (HDAC6) qui protège une chaperonne (HSPD1) de la destruction. Ensemble, ces acteurs aident les cellules cancéreuses à changer de forme, à se déplacer et à se propager. LukS-PV, une protéine bactérienne réutilisée en laboratoire, interrompt cette séquence dès la surface cellulaire, conduisant finalement à la dégradation de HSPD1 et à un frein sur les métastases. Bien qu’encore au stade expérimental, ce travail suggère que des médicaments inspirés de LukS-PV — ou ciblant BCL6, HDAC6 ou HSPD1 — pourraient offrir de nouvelles façons d’empêcher la dissémination des tumeurs hépatiques et d’améliorer le pronostic des patients.
Citation: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Mots-clés: carcinome hépatocellulaire, métastase, transition épithélio-mésenchymateuse, HDAC6, thérapie par toxine bactérienne