Clear Sky Science · fr
Matrice extracellulaire dérivée de cellules souches mésenchymateuses pour la régénération des tissus musculosquelettiques
Aider le corps à reconstruire sa propre charpente
À mesure que l’espérance de vie augmente et que les personnes restent actives jusqu’à un âge avancé, les blessures et l’usure des os, des articulations, des muscles et des tendons deviennent une cause majeure de douleur et d’incapacité. Cet article explore une nouvelle classe de matériaux de réparation « intelligents » cultivés à partir de nos propres cellules souches — des structures de soutien particulières appelées matrice extracellulaire dérivée de cellules souches mésenchymateuses (mECM). Ces échafaudages naturels pourraient un jour aider le corps à reconstruire les tissus musculosquelettiques endommagés de manière plus sûre et plus efficace que nombre de traitements actuels.
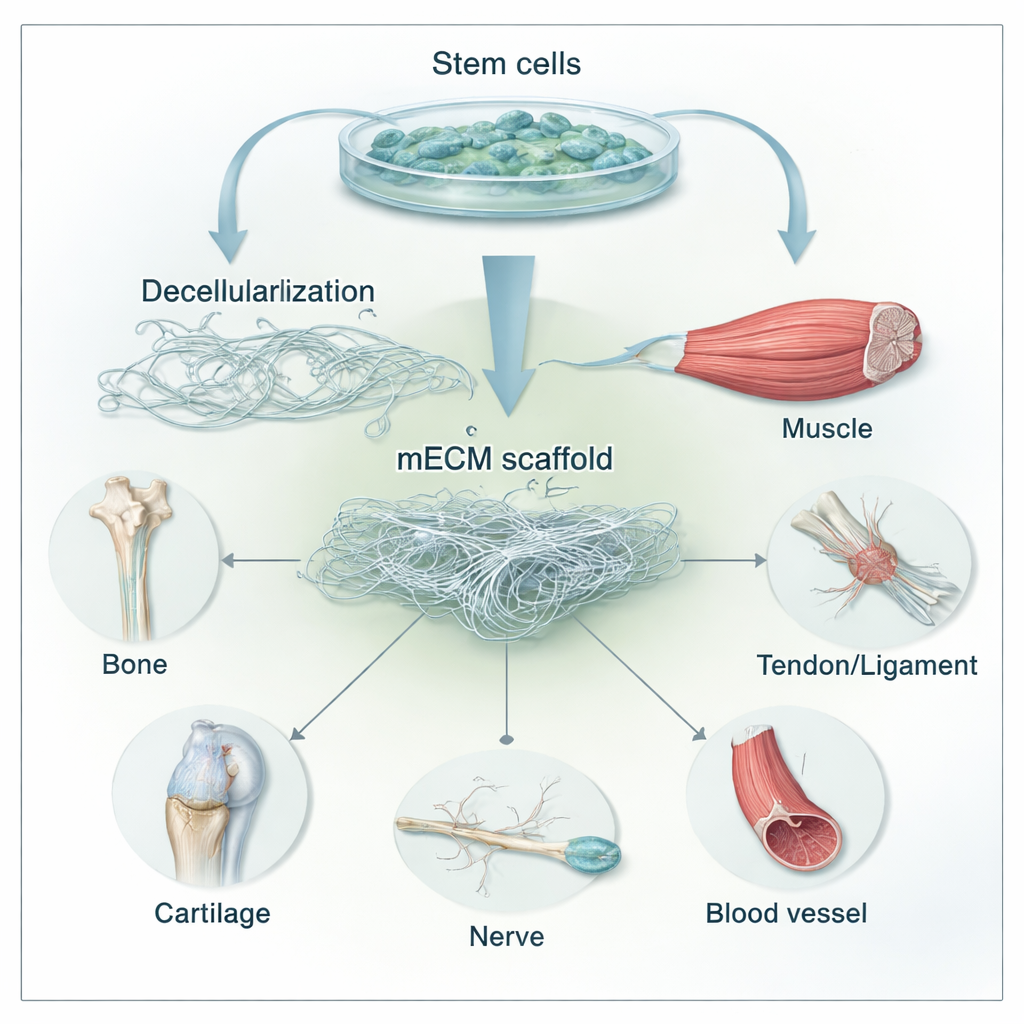
Le support de construction caché du corps
Chaque cellule du corps vit au sein d’un maillage de soutien connu sous le nom de matrice extracellulaire, ou MEC. Ce n’est pas un simple adhésif passif : ses fibres, ses pores et ses molécules liées envoient en permanence des signaux aux cellules sur la façon de croître, de se déplacer et de mûrir. Avec l’âge et lors de maladies, cette matrice se raidit, s’effiloche et perd son élasticité, affaiblissant directement notre capacité à réparer os et cartilage. Les scientifiques ont appris à éliminer les cellules de tissus comme la peau, l’intestin ou le cartilage, laissant derrière eux des échafaudages de MEC « décellularisés » qui peuvent être implantés pour guider la cicatrisation. Mais ces matériaux d’origine tissulaire peuvent varier d’un donneur à l’autre, déclencher encore des réactions immunitaires et sont difficiles à personnaliser selon les patients ou les blessures.
Cultiver un matériau de réparation sur mesure à partir de cellules souches
La revue se concentre sur la MEC produite non pas à partir d’organes entiers mais à partir de cellules souches mésenchymateuses (CSM), des cellules polyvalentes présentes dans la moelle osseuse, la graisse, le cordon ombilical et d’autres tissus. En laboratoire, on laisse les CSM se répartir sur une surface et déposer leur propre matrice — une toile tridimensionnelle délicate de collagène, fibronectine, laminine, sucres et facteurs de croissance. Les cellules sont ensuite éliminées en douceur à l’aide de détergents et d’enzymes doux, laissant une mECM sans cellules. Parce que les molécules de la MEC sont hautement conservées entre les espèces et dépourvues d’ADN et d’autres déclencheurs immunitaires puissants, ces échafaudages sont souvent bien tolérés. Fait important, les chercheurs peuvent ajuster la composition et la rigidité de la mECM en choisissant la source des cellules souches (par exemple moelle osseuse vs tissu adipeux) et en « préconditionnant » les cellules avec différents signaux avant la décellularisation.
Comment cet échafaudage vivant s’adresse aux cellules
Lorsque de nouvelles cellules sont resemées sur la mECM, elles se comportent très différemment que sur du plastique plat. Les études montrent que la mECM stimule la croissance cellulaire tout en aidant les cellules à rester « plus jeunes », retardant l’apparition du vieillissement cellulaire et préservant leur capacité à se différencier en os ou en cartilage. La mECM jeune, avec des propriétés mécaniques plus souples et une teneur plus élevée en acide hyaluronique, semble particulièrement efficace pour rajeunir des cellules plus âgées. Des composants spécifiques, tels que le collagène de type I et la fibronectine, influencent la résistance des cellules au vieillissement, la formation d’ostéoclastes résorbant l’os, ou la réponse à l’inflammation. La matrice active aussi des voies de signalisation internes liées à la longévité et à la résistance au stress, notamment SIRT1 et NF-κB, et peut orienter les cellules immunitaires vers un état plus apaisé, favorable à la réparation tissulaire. En bref, la mECM agit à la fois comme un nid physique et comme un manuel d’instructions biochimiques pour les cellules.
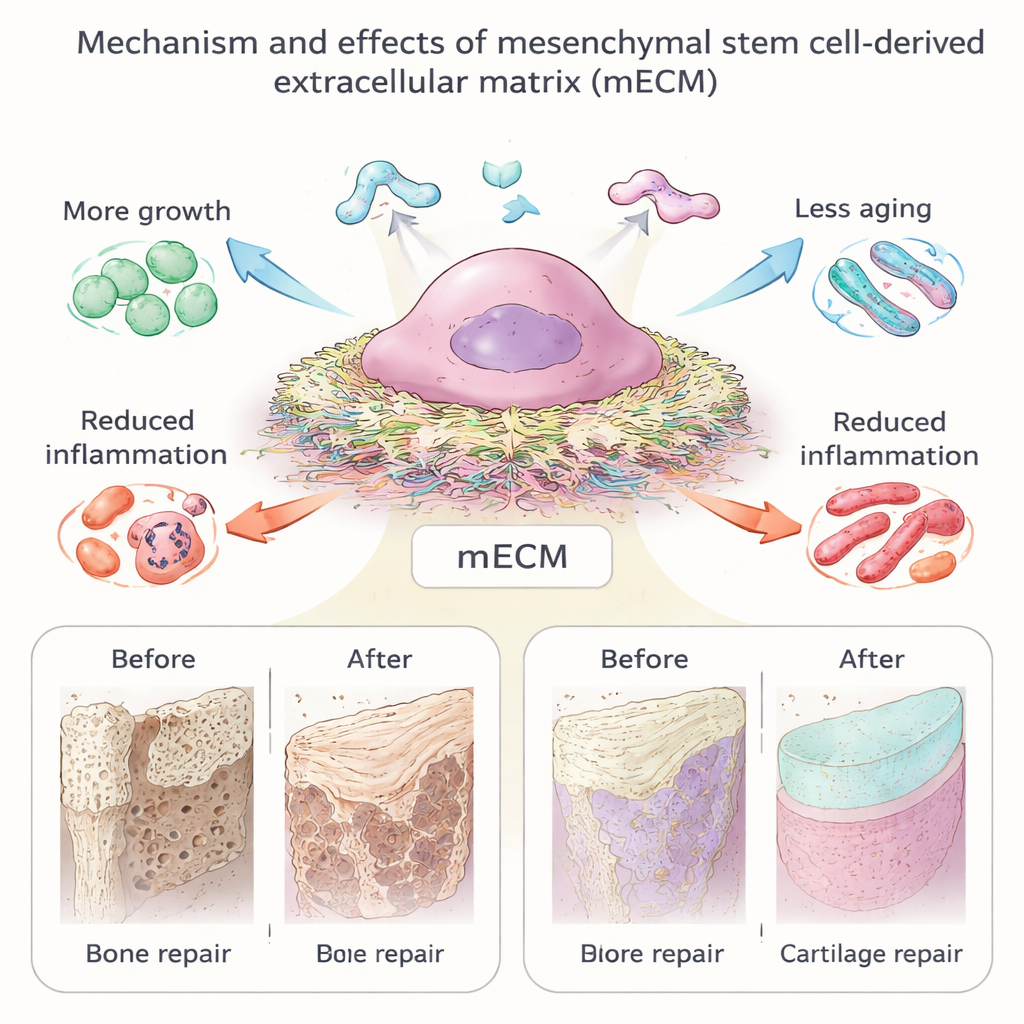
Réparer os, cartilage, muscle, tendon, nerfs et vaisseaux
Parce que la mECM imite de très près les tissus qu’elle est censée réparer, elle a été testée sous de nombreuses formes : feuilles fines enroulées autour d’implants, poudres incorporées dans des hydrogels et des microsphères, et revêtements sur des échafaudages synthétiques. Pour la réparation osseuse, les cellules cultivées sur mECM acquièrent une capacité osteogénique et contribuent à construire un tissu plus solide et mieux vascularisé chez l’animal, même sans cocktails médicamenteux lourds. Dans le cartilage, la mECM favorise la formation d’un cartilage lisse de type hyalin et aide les chondrocytes (cellules du cartilage) à éviter de dériver vers des états cicatriciels — surtout lorsque la matrice provient de cellules souches jeunes ou en cours de différenciation. Les travaux préliminaires sur le muscle et le tendon suggèrent que les matrices dérivées de cellules souches peuvent attirer les cellules de l’hôte, réduire la formation de cicatrices et mieux aligner les nouvelles fibres. Dans les nerfs et les vaisseaux sanguins, l’intégration de mECM dans des tubes guides ou des nanofibres accélère la repousse nerveuse et stimule la néoformation vasculaire, soulignant son large potentiel régénératif.
Du banc de laboratoire aux traitements en clinique
Malgré des résultats encourageants, la mECM n’est pas encore prête pour un usage clinique courant. Le domaine manque encore de protocoles standardisés pour retirer les cellules en préservant les détails délicats de la matrice, et les « ingrédients actifs » exacts qui contrôlent le comportement cellulaire ne sont que partiellement compris. Différentes sources et âges de cellules souches produisent des matrices sensiblement différentes, ce qui soulève la question des meilleures combinaisons selon le type de lésion. La production de mECM à grande échelle est coûteuse et techniquement exigeante, et les chercheurs doivent démontrer que des implants volumineux et durables sont sûrs, stables et mécaniquement suffisamment résistants pour des zones porteuses de charge comme les articulations et les tendons. Les auteurs soutiennent que des progrès en protéomique, bioinformatique et biofabrication seront cruciaux pour cartographier, standardiser et industrialiser ces échafaudages vivants. Si ces obstacles peuvent être levés, la mECM spécifique au patient pourrait devenir une nouvelle référence pour réparer la charpente du corps de l’intérieur.
Citation: Lv, S., Wang, J., Chen, J. et al. Mesenchymal stem cell-derived extracellular matrix for musculoskeletal tissue regeneration. Commun Biol 9, 147 (2026). https://doi.org/10.1038/s42003-026-09638-3
Mots-clés: matrice extracellulaire, cellules souches mésenchymateuses, réparation os et cartilage, ingénierie tissulaire, médecine régénérative