Clear Sky Science · fr
La migration cellulaire confinée périodique entraîne une réorganisation partiellement réversible de la chromatine dans des lignées cancéreuses
Comment les cellules cancéreuses comprimées se souviennent du stress
Les cellules cancéreuses qui se détachent d’une tumeur doivent ramper à travers de minuscules interstices dans les tissus et les vaisseaux sanguins. Pour y parvenir, elles compressent leur intérieur mou — et en particulier leur noyau, qui contient l’ADN — à travers des espaces parfois plus petits que le noyau lui‑même. Cette étude examine ce qui arrive à l’emballage de l’ADN lors de ces compressions répétées et pose une question clé : le noyau reprend‑t‑il simplement son état initial, ou conserve‑t‑il une sorte de « mémoire mécanique » susceptible de favoriser la propagation du cancer ?
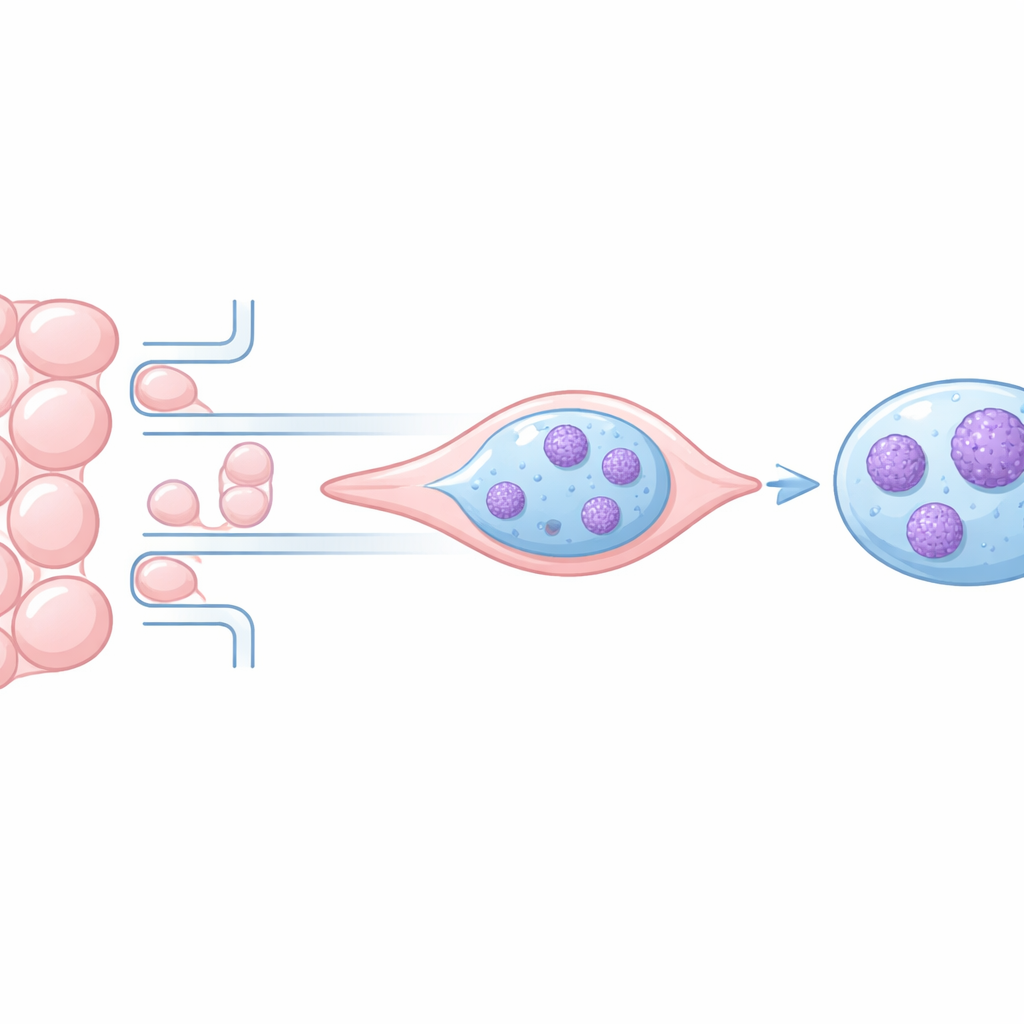
Pourquoi le compactage de l’ADN compte quand les cellules se déplacent
À l’intérieur du noyau, l’ADN est enroulé autour de protéines et replié en chromatine, qui peut être faiblement compacte ou fortement condensée. Les régions lâches tendent à être actives, abritant des gènes fréquemment utilisés, tandis que les régions fortement compactes sont plus silencieuses. Lorsque les cellules migrent à travers des espaces étroits, le noyau se déforme, et des travaux antérieurs ont montré que cela peut compacter temporairement la chromatine et même endommager l’ADN. Mais il n’était pas clair si ces changements s’inversent complètement ou laissent des traces durables susceptibles d’altérer l’agressivité des cellules cancéreuses.
Un minuscule labyrinthe pour comprimer des cellules cancéreuses isolées
Les chercheurs ont construit un dispositif microfluidique sur mesure — une puce transparente contenant des dizaines de canaux microscopiques qui alternent à plusieurs reprises entre segments larges et étroits. Deux lignées cellulaires cancéreuses différentes, toutes deux modifiées pour que leur chromatine s’illumine au microscope, ont été guidées pour ramper à travers ces canaux à l’aide d’un attractant chimique. L’imagerie en time‑lapse haute résolution a permis à l’équipe de suivre chaque noyau cellulaire en mouvement, de mesurer la taille nucléaire et de cartographier, image par image, les amas de chromatine fortement condensée chez plus de 100 cellules individuelles.
Que devient le noyau sous pression
Chaque fois qu’une cellule entrait dans une constriction étroite, son noyau se rétractait brusquement en surface projetée, traduisant une réduction réversible du volume nucléaire. Simultanément, la fraction du noyau occupée par la chromatine fortement condensée augmentait — souvent de deux à trois fois — puis revenait à son niveau de base une fois la cellule sortie dans une région plus large. Ce schéma se répétait au cours de plusieurs constrictions successives et dans les deux types cellulaires testés, suggérant que la quantité globale de chromatine dense est une réponse flexible et à court terme au stress mécanique plutôt qu’un changement permanent. Cependant, un examen plus fin des motifs de fluorescence a révélé que les pixels d’intensité très élevée et très faible augmentaient pendant la compression, laissant présager une réorganisation interne plus complexe qu’un simple compactage uniforme.
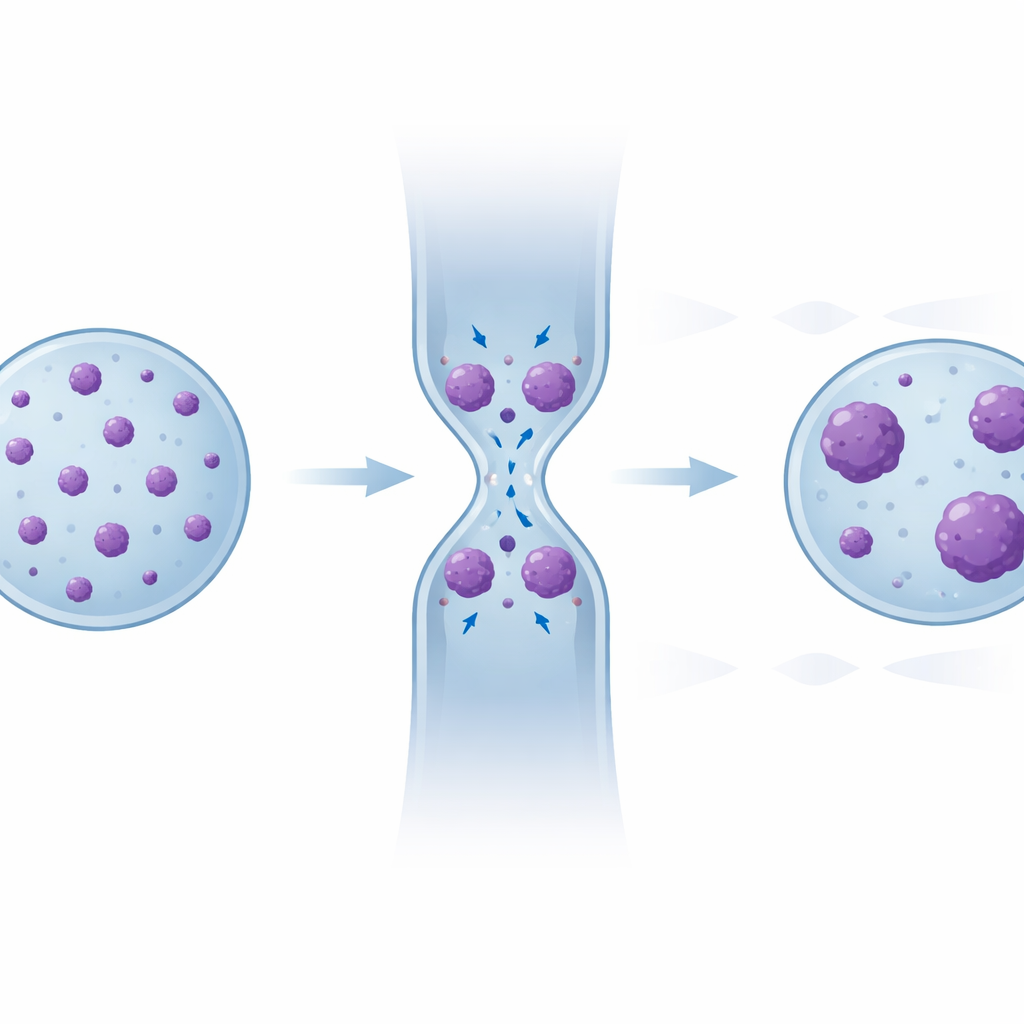
Une mémoire cachée dans la disposition des amas d’ADN
Pour mettre en lumière cette réorganisation cachée, l’équipe a examiné chaque amas individuel de chromatine condensée — sa taille et le nombre d’amas par noyau — avant, pendant et après le confinement. Pendant la compression, de petits amas avaient tendance à fusionner en amas plus grands. Après la détente du noyau, la surface totale condensée revenait à son niveau initial, mais le motif ne revenait pas : comparées à l’état de départ, les cellules ayant traversé plusieurs constrictions présentaient globalement moins d’amas, avec une distribution biaisée vers des tailles plus grandes. Des comparaisons statistiques ont confirmé que les distributions observées dans les régions de « récupération » ultérieures ressemblaient de plus en plus à celles vues en confinement. Des marquages par immunofluorescence ont en outre montré que bon nombre de ces régions denses chevauchaient des marques de chromatine « silencieuse » établies, et un modèle informatique traitant la chromatine comme un polymère interactif a reproduit cette relaxation partielle mais incomplète simplement à partir de la physique de segments d’ADN adhésifs rapprochés par la déformation.
Ce que cela signifie pour la propagation du cancer et les thérapies futures
Concrètement, l’étude montre que lorsque les noyaux des cellules cancéreuses sont comprimés de façon répétée, l’organisation de leur ADN se comporte comme une balle anti‑stress qui garde une mémoire. Le noyau peut retrouver sa taille, et la quantité globale de compactage peut se réinitialiser, mais le motif détaillé des amas d’ADN dense ne revient pas complètement à l’état initial. Après de nombreux cycles de compression, le noyau présente moins d’amas mais de plus grande taille, ce qui peut modifier l’accès à certains gènes. Cette « mémoire mécanique » pourrait aider les cellules cancéreuses à mieux tolérer de futures déformations lorsqu’elles envahissent de nouveaux tissus. Comprendre et, éventuellement, cibler ce couplage entre forces physiques et organisation de l’ADN pourrait ouvrir de nouvelles voies pour limiter la métastase en perturbant la manière dont les cellules cancéreuses s’adaptent au stress mécanique.
Citation: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Mots-clés: migration cellulaire confinée, condensation de la chromatine, mécanique nucléaire, mémoire mécanique, métastase cancéreuse