Clear Sky Science · fr
PTBP1 soutient la spermatogenèse chez la souris en facilitant l’organisation du cytosquelette via la voie mTORC2–PKCα dans les cellules de Sertoli
Pourquoi cette étude importe pour la fertilité masculine
L’infertilité masculine semble souvent mystérieuse, mais, en substance, elle dépend d’un partenariat finement réglé entre les spermatozoïdes en développement et les cellules « nourricières » qui les soutiennent. Cette étude explore l’un des assistants moléculaires discrets présents dans ces cellules nourricières et montre comment sa défaillance peut arrêter la production de spermatozoïdes. Comprendre cette couche cachée de contrôle pourrait orienter vers de nouveaux diagnostics ou traitements pour certaines formes d’infertilité masculine.
Les cellules de soutien qui rendent possible la production de spermatozoïdes
Les spermatozoïdes sont produits à l’intérieur de longs tubes enroulés du testicule appelés tubules séminifères. Ces tubes sont tapissés de cellules de Sertoli, un type de cellule de soutien spécialisée qui berce les cellules germinales en développement, les nourrit et les guide lorsqu’elles se divisent et mûrissent en spermatozoïdes. Les cellules de Sertoli construisent aussi une paroi protectrice connue sous le nom de barrière hémato-testiculaire, qui sépare les cellules en stade précoce du système immunitaire. Pour accomplir tout cela, elles s’appuient sur un échafaudage interne d’actine et de microtubules qui se remanie constamment à mesure que des vagues de cellules germinales traversent les tubules. Si cet échafaudage est perturbé, la barrière devient perméable et les cellules germinales en maturation peuvent se détacher ou mourir, menaçant la fertilité.
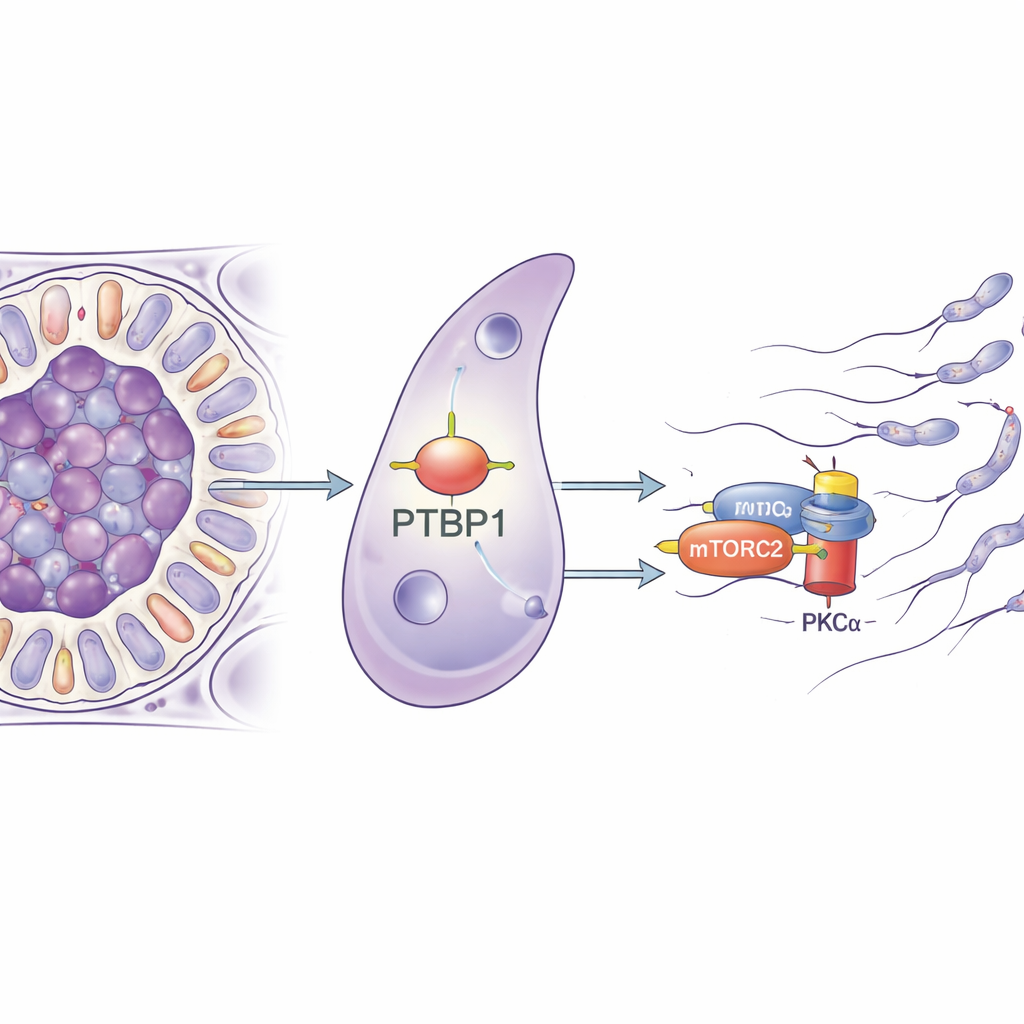
Un petit gestionnaire d’ARN avec une grande mission
Les chercheurs se sont concentrés sur une protéine appelée PTBP1, surtout connue pour son rôle dans la gestion des molécules d’ARN au sein des cellules — décidant comment les gènes sont épissés, la stabilité de leurs messages et l’efficacité de leur traduction en protéines. PTBP1 est abondante à la fois dans les cellules germinales et les cellules de Sertoli, et des travaux antérieurs ont montré que la supprimer dans les cellules germinales entrave la production de spermatozoïdes. Dans cette étude, l’équipe a spécialement supprimé PTBP1 uniquement dans les cellules de Sertoli chez la souris. À première vue, les jeunes souris semblaient normales, mais à la maturité sexuelle leurs testicules ont rétréci, le nombre de spermatozoïdes dans l’épididyme a chuté, et aucun mâle n’a pu engendrer de descendants, révélant une perte complète de fertilité.
Quand l’échafaudage cellulaire s’effondre
L’examen microscopique des testicules de ces souris a montré que la spermatogenèse s’arrêtait à mi‑parcours. De nombreux tubules contenaient des espaces vides, des amas anormaux de noyaux de cellules germinales fusionnés et une pénurie de spermatozoïdes entièrement allongés. Les noyaux des cellules de Sertoli, qui normalement s’alignent contre la paroi externe des tubules, étaient souvent déplacés vers le centre, suggérant que ces cellules de soutien perdaient leur ancrage. Des marquages pour des composants de jonctions clés et des protéines structurelles ont confirmé que la barrière hémato-testiculaire était affaiblie et que les faisceaux serrés d’actine habituels étaient remplacés par des brins désorganisés et excessivement intenses s’étirant de la base vers le centre du tubule. Une molécule traceuse qui reste normalement du « côté sanguin » de la barrière a fui profondément dans les tubules, démontrant directement la rupture de la barrière.
Retracer l’échec jusqu’à un nœud de signalisation
Pour comprendre comment une protéine liant l’ARN pouvait entraîner de tels problèmes mécaniques, l’équipe a purifié les cellules de Sertoli et analysé les gènes dont l’activité changeait en l’absence de PTBP1. Beaucoup des gènes affectés participaient au contrôle du cytosquelette et des adhérences cellulaires, indiquant un défaut global de remodelage. Les chercheurs ont ensuite isolé les molécules d’ARN qui se lient physiquement à PTBP1 et ont constaté qu’il se fixe au message codant pour Rictor, une composante centrale d’un complexe de signalisation appelé mTORC2. Ce complexe active à son tour une enzyme nommée PKCα qui module les filaments d’actine. Dans les cellules de Sertoli dépourvues de PTBP1, la quantité de protéine RICTOR a diminué et PKCα était beaucoup moins active, même si le niveau d’ARN sous‑jacent pour Rictor avait peu changé. Cela suggère fortement que PTBP1 aide les cellules de Sertoli à produire suffisamment de protéine RICTOR à partir de son message ARN, maintenant ainsi la voie mTORC2–PKCα opérationnelle.
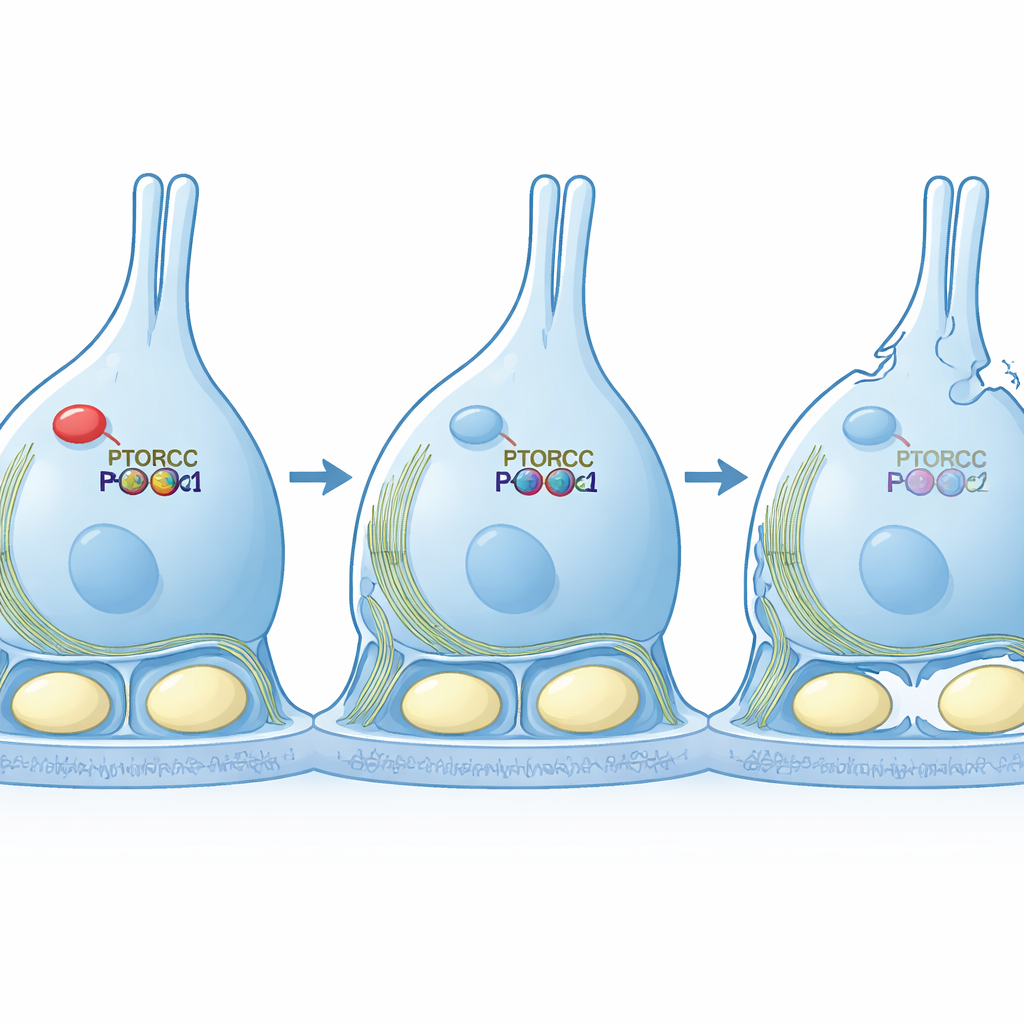
Restaurer l’échafaudage en rétablissant le signal
L’équipe est ensuite passée à des modèles en culture cellulaire pour tester la causalité. Lorsqu’ils ont réduit PTBP1 dans une lignée cellulaire de type Sertoli, les cellules se sont étirées en formes longues et fines et ont affiché un réseau d’actine brouillé — signes d’un affaiblissement du signal mTORC2. De manière importante, lorsqu’ils ont forcé ces cellules à produire une version constitutivement active de PKCα, les cellules ont retrouvé leur forme compacte normale et des structures d’actine plus ordonnées, bien que RICTOR demeure bas. Cette expérience de « sauvetage » montre que la fonction principale de PTBP1 dans ce contexte est de maintenir la voie mTORC2–PKCα suffisamment active pour organiser l’échafaudage interne de la cellule.
Ce que cela signifie pour la compréhension de l’infertilité
En termes simples, ce travail révèle une chaîne de dépendance dans le testicule : PTBP1 aide les cellules de Sertoli à établir un nœud de signalisation clé ; ce nœud organise leur cytosquelette ; et un cytosquelette intact leur permet de saisir et protéger les spermatozoïdes en développement. Brisez la chaîne au niveau de PTBP1, et les cellules de Sertoli perdent leur structure, la barrière protectrice cède et le développement des spermatozoïdes s’effondre, entraînant une infertilité masculine. Bien que cette recherche ait été réalisée chez la souris, les mêmes molécules existent chez l’humain, laissant envisager que des défauts subtils du contrôle de l’ARN dans les cellules de Sertoli pourraient sous‑tendre certains cas inexpliqués d’infertilité masculine et offrant un nouvel ensemble de cibles moléculaires pour des études futures.
Citation: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Mots-clés: fertilité masculine, cellules de Sertoli, spermatogenèse, cytosquelette, protéines liant l’ARN