Clear Sky Science · fr
Régulation négative de la voie NF-κB par la ligase ubiquitine Nedd4-1(NE)
Pourquoi il est important d’éteindre l’inflammation
Notre système immunitaire dépend d’épisodes rapides d’inflammation pour combattre les infections et réparer les blessures, mais ces mêmes forces peuvent endommager les tissus et alimenter le cancer si elles restent activées trop longtemps. Cet article examine comment les cellules humaines et d’autres primates évitent ce danger en utilisant un « frein » interne nouvellement caractérisé qui calme l’un des systèmes d’alarme centraux de l’organisme une fois sa tâche accomplie.
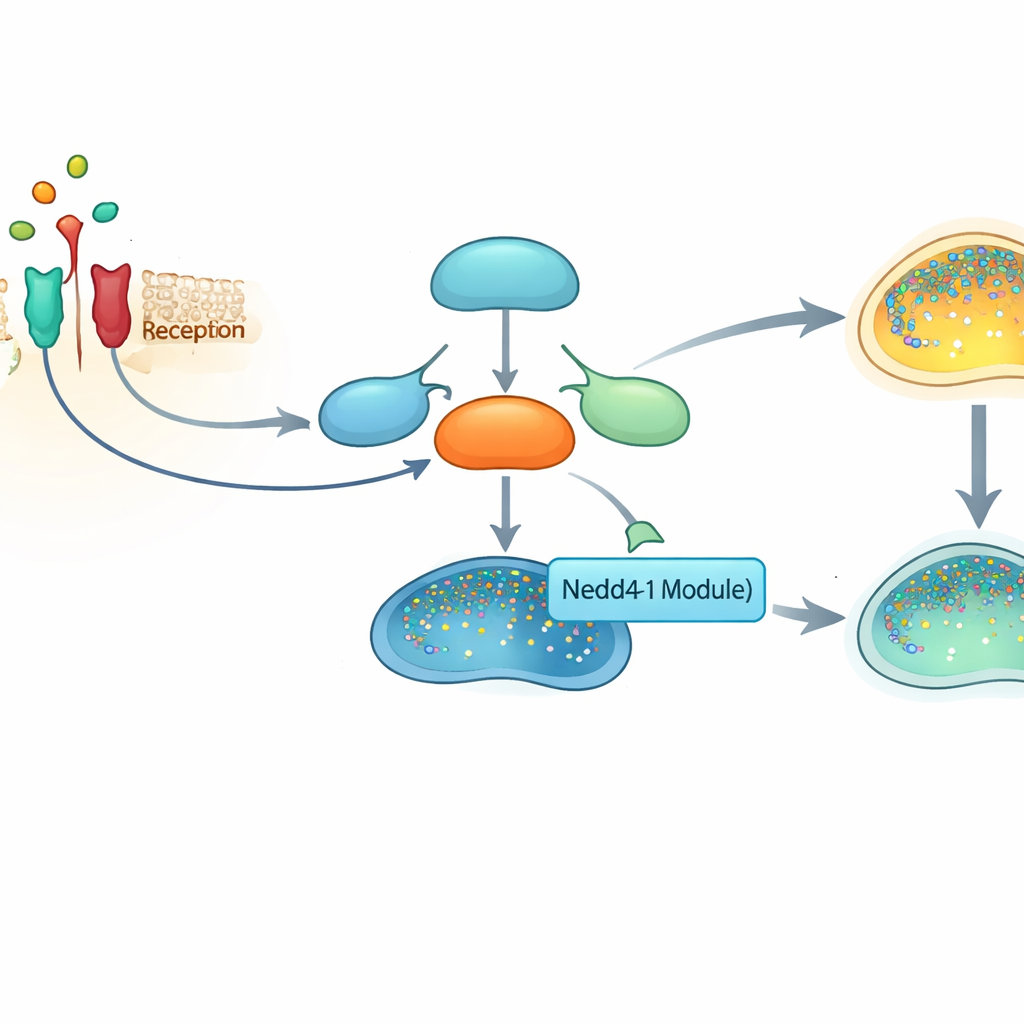
Un interrupteur d’alarme central dans nos cellules
Au cœur de cette histoire se trouve NF-κB, une famille de protéines qui agit comme un interrupteur maître pour des centaines de gènes impliqués dans l’inflammation, la survie cellulaire et l’immunité. Lorsque les cellules détectent des signaux de stress tels que la molécule inflammatoire TNFα, une chaîne d’événements libère NF-κB de ses « chaperons » protéiques dans le milieu liquide de la cellule et lui permet de migrer vers le noyau, où il active des gènes pro‑inflammatoires et pro‑survie. Parce que cette voie est si puissante, les cellules doivent régler finement son activation et son arrêt. L’incapacité à l’éteindre a été associée à des maladies inflammatoires chroniques et à de nombreux cancers.
Un frein spécifique aux primates sur l’alarme
Les chercheurs se sont intéressés à Nedd4-1, membre d’une grande famille d’enzymes qui marquent d’autres protéines avec une petite molécule appelée ubiquitine. Cette étiquette signale souvent la destruction ou le repositionnement des protéines dans la cellule, remodelant les réseaux de signalisation. Un variant d’épissage de Nedd4-1, appelé Nedd4-1(NE), découvert antérieurement, se retrouve uniquement chez les primates et porte un long segment additionnel à son extrémité N qui modifie sa localisation cellulaire et ses cibles. Contrairement à la forme standard de Nedd4-1, qui peut en réalité stimuler l’activité de NF‑κB via d’autres partenaires, l’équipe a montré que Nedd4-1(NE) a l’effet contraire : il atténue la signalisation NF‑κB, en particulier après une exposition prolongée au TNFα.
Deux façons de maintenir NF-κB sous contrôle
Pour découvrir comment fonctionne ce frein, les auteurs ont utilisé le marquage de proximité et des méthodes d’extraction de protéines pour identifier les molécules qui s’associent physiquement à Nedd4-1(NE). Ils ont identifié des composants clés de la voie NF‑κB, y compris la kinase IKKβ et la protéine précurseur NF‑κB1 (aussi appelée p105). Des expériences complémentaires ont montré que Nedd4-1(NE) ajoute des étiquettes ubiquitine sur IKKβ, conduisant à sa dégradation. Avec moins d’IKKβ disponible, sa cible habituelle IκBα n’est plus phosphorylée et détruite aussi efficacement. En conséquence, IκBα reste plus stable et maintient la sous‑unité active de NF‑κB, p50, séquestrée dans le cytosol, l’empêchant d’entrer dans le noyau pour activer les gènes inflammatoires.
Un transfert guidé par un adaptateur vers le frein
Nedd4-1(NE) agit également en aval en limitant les niveaux de NF‑κB1 lui‑même. Ici, l’enzyme ne travaille pas seule : elle collabore avec une autre protéine d’ubiquitination appelée KPC1. KPC1 participe au traitement du précurseur NF‑κB1 p105 en la forme active p50 et réside dans des compartiments cellulaires appelés endosomes tardifs, où Nedd4-1(NE) se trouve aussi. L’équipe a montré que Nedd4-1(NE) peut ubiquitiner KPC1 et que ce KPC1 modifié sert d’adaptateur, recrutant NF‑κB1 vers Nedd4-1(NE) sur les endosomes tardifs. Ce complexe à trois favorise la déstabilisation à la fois de p105 et de p50, réduisant une nouvelle fois le réservoir de NF‑κB pouvant atteindre le noyau.
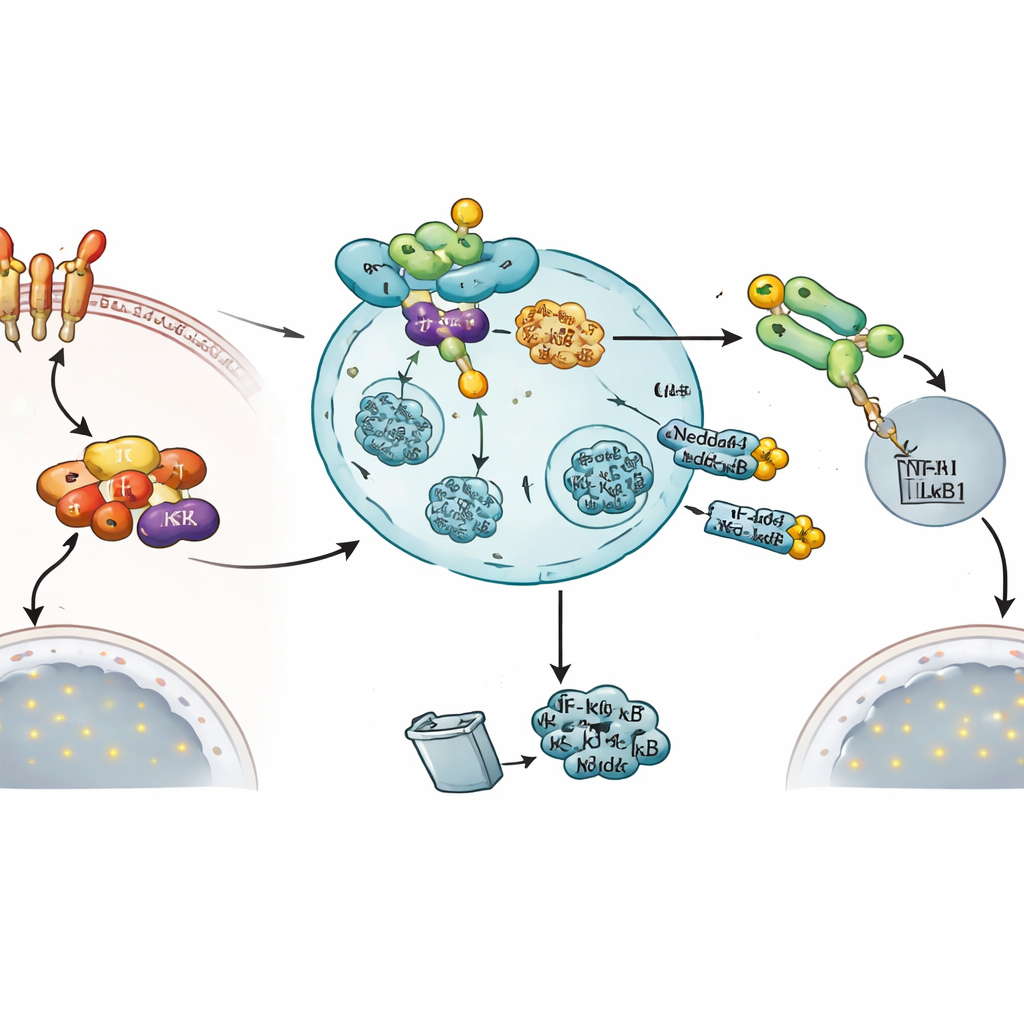
Une boucle de rétroaction intégrée pour mettre fin au signal
Fait remarquable, le signal même qui active NF‑κB semble aussi induire ce frein. Lorsque les cellules ont été traitées par TNFα, les niveaux d’ARN messager de Nedd4-1(NE) ont fortement augmenté, tandis que la forme standard de Nedd4-1 n’a pas changé. Des mesures fonctionnelles ont soutenu l’idée que Nedd4-1(NE) constitue une vanne d’arrêt : l’augmentation de Nedd4-1(NE) actif réduisait la migration de NF‑κB1 vers le noyau, abaissait l’activité d’un gène rapporteur sensible à NF‑κB, et diminuait l’expression d’un gène inflammatoire régulé par NF‑κB, TNFAIP3. Ensemble, ces résultats décrivent une boucle de rétroaction négative dans laquelle l’activation de la voie NF‑κB augmente finalement Nedd4-1(NE), qui cible alors deux nœuds critiques — IKKβ et NF‑κB1 — pour ramener la réponse inflammatoire à un niveau plus bas.
Ce que cela signifie pour la santé et la maladie
Pour un public non spécialisé, le message clé est que nos cellules intègrent un mécanisme de sécurité supplémentaire, spécifique aux primates, pour empêcher la signalisation inflammatoire de déraper. En marquant sélectivement et en réduisant les composants centraux du système NF‑κB, Nedd4-1(NE) contribue à terminer la réponse au TNFα et peut participer à l’équilibre immunitaire à long terme. Comprendre ce frein intégré pourrait ouvrir de nouvelles pistes pour traiter des maladies où NF‑κB est chroniquement hyperactif, comme les troubles auto‑immuns et certains cancers, en suggérant des façons d’imiter ou d’augmenter ce processus naturel d’arrêt.
Citation: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Mots-clés: Signalisation NF-kB, inflammation, ligase ubiquitine, Nedd4-1(NE), TNF alpha