Clear Sky Science · fr
Notch3 régule la plasticité phénotypique des péricytes dans le cancer colorectal
Pourquoi les vaisseaux sanguins autour des tumeurs comptent
Le cancer colorectal est l’un des cancers les plus fréquents et les plus meurtriers au monde, et pourtant la plupart des thérapies visent directement les cellules tumorales en négligeant souvent le système de soutien environnant qui favorise la croissance tumorale. Cet article se concentre sur un groupe de cellules de soutien moins connues, les péricytes, qui entourent les petits vaisseaux. En révélant comment un interrupteur de signalisation nommé Notch3 modifie le comportement des péricytes, les auteurs montrent comment l’alimentation sanguine de la tumeur peut être orientée soit vers des vaisseaux fuyants et chaotiques favorables au cancer, soit vers des vaisseaux plus normaux susceptibles de ralentir la maladie et d’améliorer le traitement. 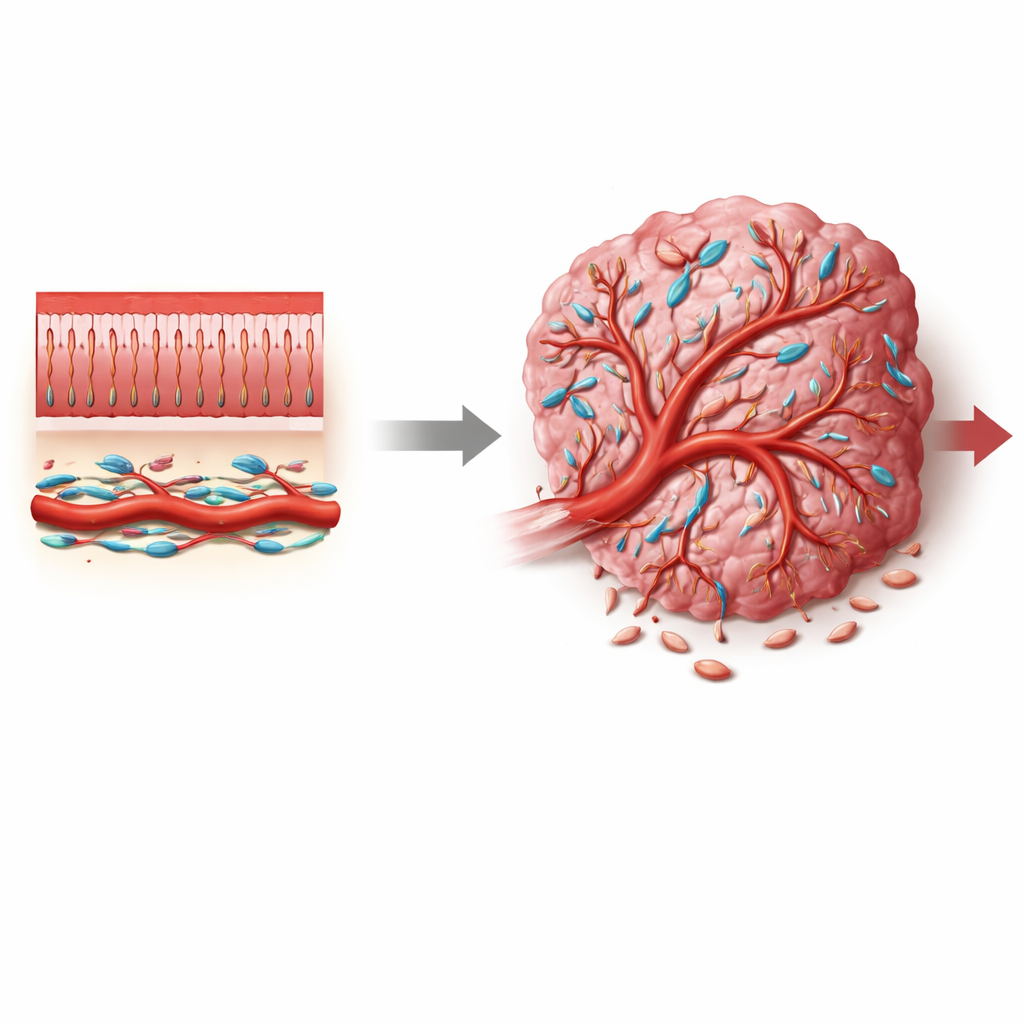
Les aides cachés autour des vaisseaux tumoraux
Les vaisseaux sanguins sont plus que de simples tubes creux. Dans les tissus sains, les petits vaisseaux sont étroitement entourés par des péricytes—des cellules spécialisées qui stabilisent la paroi des vaisseaux, contrôlent le flux sanguin et limitent les fuites. Dans les tumeurs, cependant, ces péricytes présentent souvent un aspect et un comportement différents : ils peuvent se détacher, proliférer ou changer d’identité, contribuant ainsi à la vascularisation anormale et perméable typique des cancers. Dans les tumeurs colorectales, où le microenvironnement est encombré de fibroblastes, de cellules immunitaires et de cellules vasculaires, il était jusqu’ici peu clair d’où proviennent les péricytes associés aux tumeurs, quels états ils adoptent et quels signaux moléculaires les orientent vers des rôles favorisant la tumeur.
Suivre les péricytes pendant la formation tumorale
Pour suivre les péricytes au fil du temps, les chercheurs ont utilisé des modèles murins de cancer colorectal associé à la colite dans lesquels ils pouvaient « étiqueter » génétiquement des types cellulaires spécifiques et observer leur destin. Ils ont montré que les péricytes trouvés dans les tumeurs proviennent majoritairement de péricytes résidents normaux du tissu qui s’étendent et prolifèrent à mesure que le cancer se développe, plutôt que d’arriver de sources distantes comme la moelle osseuse. À l’aide d’un séquençage ARN unicellulaire avancé, ils ont répertorié des dizaines de milliers de cellules stromales issues de tumeurs murines et de côlon normal et ont constaté que les péricytes sont significativement enrichis dans le microenvironnement tumoral. Ils ont également identifié une expansion similaire des péricytes dans plusieurs jeux de données de cancers colorectaux humains, soulignant que ce phénomène n’est pas spécifique aux souris.
Un interrupteur moléculaire qui change le comportement des péricytes
L’équipe s’est ensuite interrogée sur les signaux qui façonnent le comportement des péricytes dans les tumeurs et a découvert que Notch3—un récepteur permettant aux cellules de communiquer avec leurs voisines—est particulièrement actif dans les péricytes tumoraux. L’analyse computationnelle de la communication cellule–cellule suggérait que les péricytes émettent et reçoivent des signaux liés à Notch, notamment via des partenaires situés sur les cellules des vaisseaux sanguins. En activant artificiellement Notch3 dans les péricytes, les chercheurs ont observé que ces cellules proliféraient davantage mais exprimaient moins de protéines contractiles typiquement associées au comportement stabilisant des vaisseaux. Les vaisseaux sanguins tumoraux chez ces souris sont devenus plus larges, plus perméables et bordés par davantage de cellules endothéliales en prolifération, indiquant une vascularisation moins stable. À l’inverse, la suppression de Notch3 a réduit la prolifération des cellules endothéliales, diminué la taille des vaisseaux et limité les fuites, suggérant une bascule vers des vaisseaux plus normalisés sans modifier de façon marquée le nombre ou la taille initiale des tumeurs. 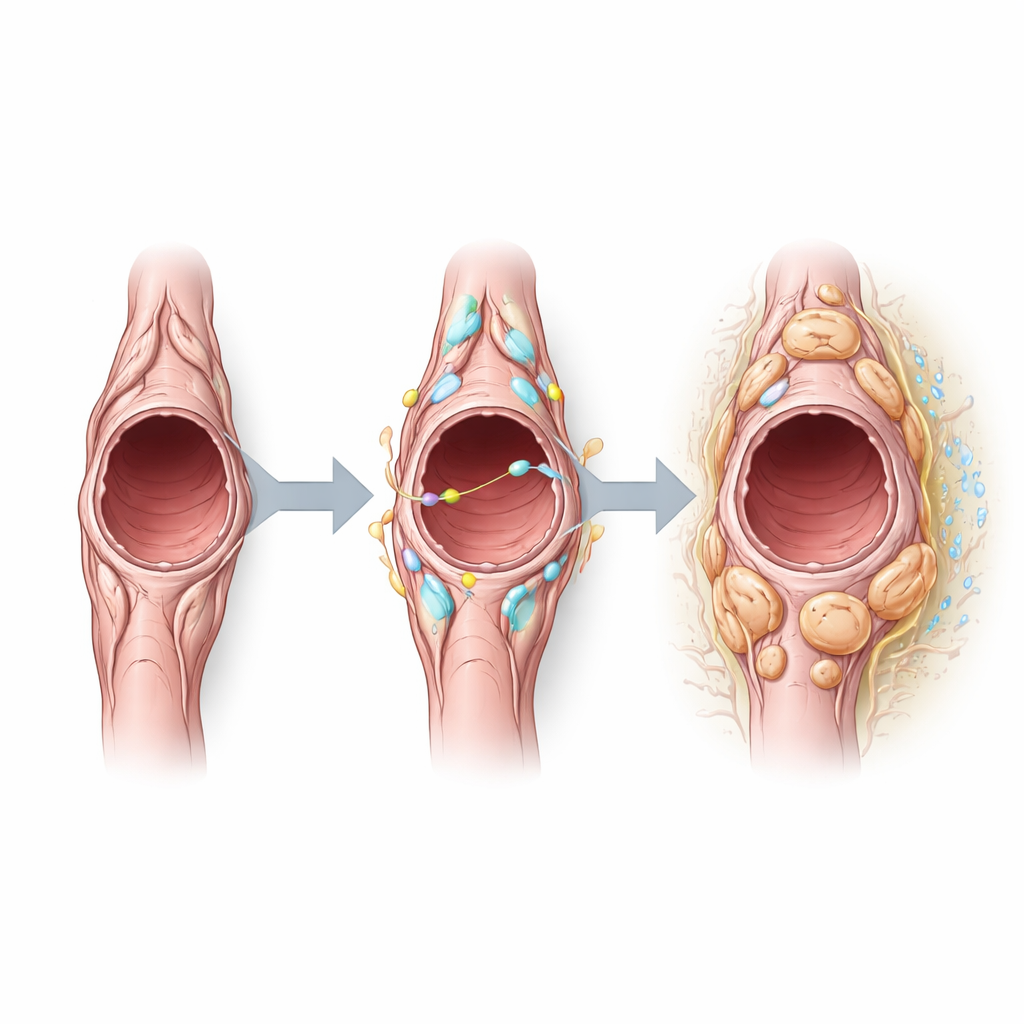
Les multiples visages des péricytes dans les tumeurs
Au-delà d’un simple changement marche/arrêt, l’étude a révélé que les péricytes tumoraux existent dans plusieurs états distincts. Certains sous-groupes présentaient des traits de cellules hautement contractiles, d’autres produisaient de grandes quantités de matrice extracellulaire, certains affichaient des caractéristiques inflammatoires, et un sous‑ensemble portait même des signatures généralement observées chez les cellules endothéliales. L’activité de Notch3 n’était pas répartie uniformément : elle était enrichie dans une population de péricytes « synthétiques » productrice de matrice et faible dans le sous-groupe le plus contractile. Les analyses de trajectoire suggéraient que les péricytes peuvent passer d’un état contractile à un état synthétique et prolifératif à mesure que l’activité de Notch3 augmente. Lorsque les auteurs ont examiné des données de cancers colorectaux humains, ils ont trouvé un spectre comparable d’états de péricytes et ont de nouveau observé une activité plus élevée d’un gène cible de Notch3 dans les péricytes associés aux tumeurs et en prolifération, reflétant les résultats murins.
Transformer le chaos vasculaire en opportunité thérapeutique
Globalement, ce travail présente Notch3 comme un bouton de réglage clé qui module l’identité des péricytes et, par leur intermédiaire, la structure et la fonction des vaisseaux sanguins tumoraux. Une forte activité de Notch3 pousse les péricytes vers un état prolifératif et moins contractile lié à des vaisseaux élargis et fuyants favorisant la progression tumorale. Une faible activité de Notch3 est associée à des péricytes plus contractiles, des cellules endothéliales plus calmes et une vascularisation plus normalisée susceptible de freiner la croissance tumorale et d’améliorer la distribution des médicaments. En ciblant spécifiquement Notch3 dans les péricytes, des thérapies futures pourraient orienter les vaisseaux tumoraux du chaos vers la stabilité, offrant un nouvel angle pour traiter le cancer colorectal avancé en combinaison avec les traitements existants.
Citation: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Mots-clés: cancer colorectal, microenvironnement tumoral, péricytes, signalisation Notch3, vaisseaux sanguins tumoraux