Clear Sky Science · fr
TRIM47 endothélial régule l’intégrité de la barrière hémato-encéphalique et la cognition via la voie de signalisation KEAP1/NRF2 chez la souris
Pourquoi la protection des tout petits vaisseaux cérébraux compte
La maladie des petits vaisseaux cérébraux est un perturbateur discret du cerveau. Elle endommage les vaisseaux sanguins les plus fins, augmente le risque d’accident vasculaire cérébral et érode lentement la mémoire et les fonctions cognitives, alors même que les médecins manquent encore de traitements ciblant ses causes biologiques fondamentales. Cette étude explore une protéine spécifique, TRIM47, présente dans les cellules qui tapissent les vaisseaux cérébraux, pour poser une question simple mais cruciale : participe‑t‑elle au maintien de l’intégrité de la barrière hémato‑encéphalique, et cela a‑t‑il des conséquences pour la cognition ?
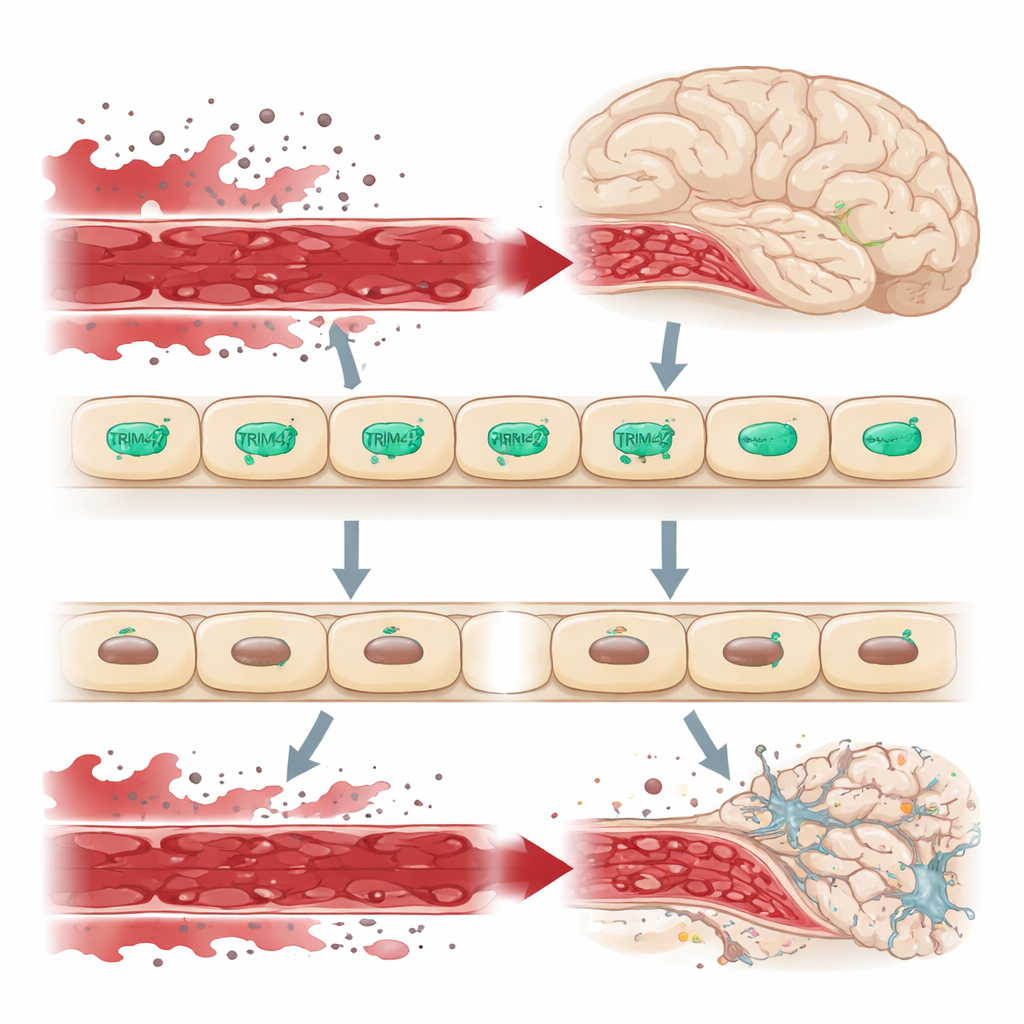
Un gardien à la frontière du cerveau
Le cerveau est protégé de la circulation générale par la barrière hémato‑encéphalique, une couche étanche d’endothélium qui contrôle strictement ce qui peut pénétrer dans le tissu cérébral. Lorsque cette barrière fuit, des molécules nocives du sang s’infiltrent dans le cerveau, stressant les neurones et les cellules de soutien et contribuant à des troubles comme la démence. Des études génétiques sur de larges populations humaines avaient identifié une zone d’ADN contenant le gène TRIM47 comme région de risque pour la maladie des petits vaisseaux cérébraux. TRIM47 est particulièrement active dans les cellules endothéliales cérébrales, ce qui suggère qu’elle pourrait être un gardien important de cette barrière.
Comment TRIM47 protège les cellules du stress oxydatif
Les auteurs ont d’abord étudié des cellules endothéliales cérébrales humaines cultivées en laboratoire et réduit les niveaux de TRIM47 par interférence ARN. Cela a déclenché de vastes changements d’activité génique, le réseau le plus fortement affecté étant centré sur NRF2, un régulateur maître des défenses antioxydantes cellulaires. En conditions normales, NRF2 est maintenu sous contrôle par une autre protéine, KEAP1, qui le dirige vers la dégradation. L’équipe a montré que TRIM47 se lie à KEAP1 et contribue à empêcher la dégradation de NRF2. En présence de TRIM47, NRF2 peut s’accumuler, migrer vers le noyau et activer des gènes qui détoxifient les espèces réactives de l’oxygène. Quand TRIM47 disparaît, les niveaux de NRF2 chutent, les gènes antioxydants sont moins actifs et les cellules endothéliales deviennent plus vulnérables au stress oxydatif.
De vaisseaux qui fuient à des troubles de la mémoire chez la souris
Pour savoir comment ce mécanisme se manifeste dans un cerveau vivant, les chercheurs ont généré des souris dépourvues du gène Trim47 dans tout l’organisme, et une autre lignée dans laquelle Trim47 pouvait être supprimé uniquement dans les cellules endothéliales. Les animaux adultes de ces deux modèles ont développé des troubles évidents de l’apprentissage spatial et de la mémoire, échouant à des tâches comme le labyrinthe en Y et le test de la piscine de Morris malgré une motricité normale. L’examen de leur cerveau a révélé que la barrière hémato‑encéphalique était devenue perméable : de petits traceurs fluorescents et des protéines sanguines s’échappaient des vaisseaux vers les tissus environnants. Les protéines « d’étanchéité » formant les jonctions serrées et d’adhérence entre cellules endothéliales, en particulier Claudin‑5 et Occludin, étaient réduites. Les astrocytes voisins, ces cellules de soutien en forme d’étoile qui réagissent rapidement aux lésions, étaient activés, bien qu’il y ait peu de signes d’inflammation étendue ou de perte neuronale à ce stade.
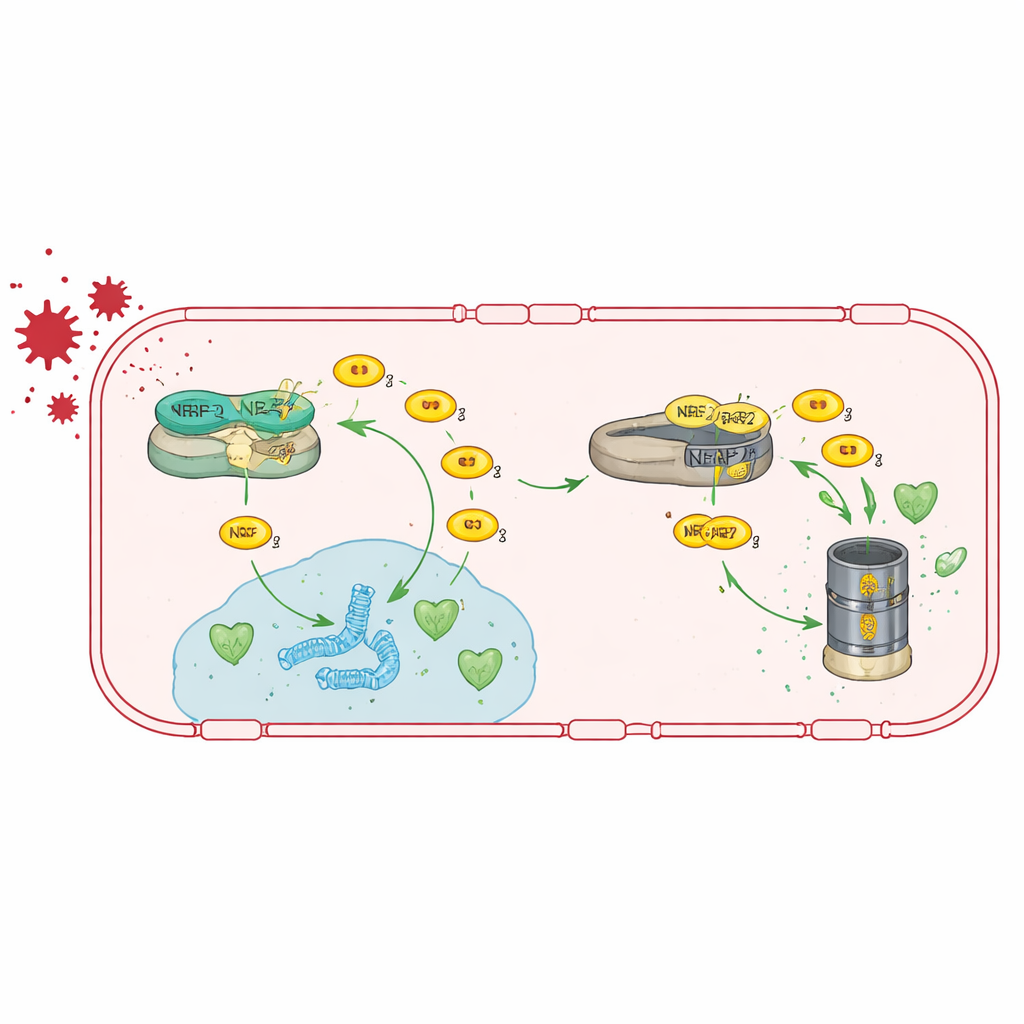
Rallumer la voie antioxydante
Étant donné que TRIM47 agit principalement en renforçant l’activité de NRF2, l’équipe a testé s’il était possible de contourner sa perte en stimulant directement NRF2. Ils ont donné à des souris déficientes en Trim47 une alimentation contenant du tert‑butylhydroquinone (tBHQ), un composé connu pour stabiliser NRF2 et activer ses gènes cibles. Ce traitement a rétabli l’activité des gènes antioxydants dans les cellules endothéliales cérébrales, ramené l’expression des gènes des jonctions serrées vers la normale et réduit la fuite de la barrière hémato‑encéphalique. De façon saisissante, il a aussi normalisé l’activation des astrocytes et restauré les performances des animaux aux tests de mémoire, suggérant que le renforcement de cette voie antioxydante peut inverser à la fois les problèmes vasculaires et cognitifs, du moins chez la souris.
Indices issus du sang humain et perspectives
Pour relier leurs expériences chez la souris à la maladie humaine, les chercheurs ont analysé des protéines liées à la voie NRF2 dans des échantillons sanguins de milliers de personnes ayant subi une IRM cérébrale. Les niveaux de plusieurs protéines régulées par NRF2 étaient associés à des marqueurs d’imagerie de la maladie des petits vaisseaux, comme l’élargissement des espaces périvasculaires et des altérations de la matière blanche. Cela soutient l’idée que une signalisation TRIM47–NRF2 altérée est pertinente chez l’homme, pas seulement chez l’animal expérimental, et que ces protéines pourraient servir de biomarqueurs de la sévérité ou de la progression de la maladie.
Ce que cela signifie pour la santé cérébrale
Dans l’ensemble, le travail présente TRIM47 comme un garde du corps moléculaire qui aide les vaisseaux cérébraux à résister aux dommages oxydatifs en stabilisant le système antioxydant NRF2. Lorsque TRIM47 manque ou est déficiente, la barrière hémato‑encéphalique s’affaiblit, de petites lésions cérébrales s’accumulent et la mémoire commence à décliner. La réactivation de la voie NRF2 peut réparer la barrière et restaurer la cognition chez la souris, mettant en lumière cet axe de signalisation comme une cible thérapeutique prometteuse pour les formes vasculaires de démence. Bien que le tBHQ lui‑même ne soit pas adapté comme médicament chez l’humain, des composés plus sûrs stimulant NRF2 ou des stratégies imitant le rôle protecteur de TRIM47 pourraient un jour aider à préserver la santé cérébrale en renforçant ses vaisseaux les plus petits et les plus fragiles.
Citation: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Mots-clés: maladie des petits vaisseaux cérébraux, barrière hémato‑encéphalique, TRIM47, voie NRF2, démence vasculaire