Clear Sky Science · fr
Un chemin inter‑sous‑unité est nécessaire pour la liaison entropiquement favorisée et la coopérativité négative des nucléotides cycliques dans le canal HCN2
Comment les minuscules commutateurs pacemakers du cœur détectent les signaux chimiques
Chaque battement de cœur et de nombreux rythmes cérébraux dépendent de canaux microscopiques qui s’ouvrent et se ferment dans les membranes de nos cellules. Ces canaux, appelés canaux pacemakers HCN, sont contrôlés non seulement par la tension électrique mais aussi par de petites molécules messagères connues sous le nom de nucléotides cycliques. Cette étude pose une question apparemment simple mais aux implications larges : comment ces petites molécules se lient‑elles de manière coordonnée au canal HCN2, et comment de subtiles défaillances dans ce processus peuvent‑elles contribuer à des troubles comme l’épilepsie ?
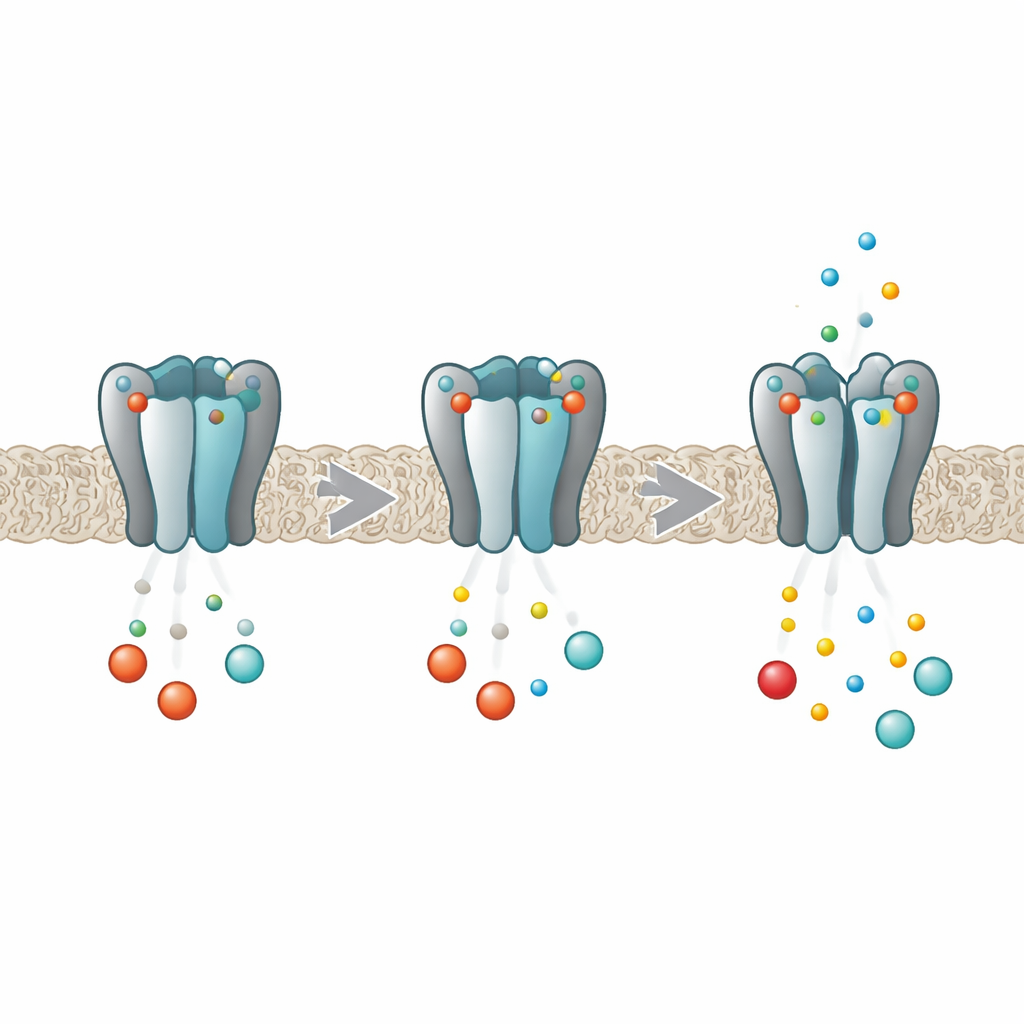
Un variateur moléculaire pour les rythmes du corps
Les canaux HCN fonctionnent comme des variateurs d’intensité pour l’activité électrique des cellules cardiaques et cérébrales. Chaque canal est composé de quatre sous‑unités protéiques identiques qui forment ensemble un pore central laissant passer les ions. Au cœur de chaque sous‑unité se trouve une poche capable de capturer des nucléotides cycliques tels que le cAMP et le cGMP. Lorsque ces messagers se lient, ils facilitent l’ouverture du pore, augmentant le courant pacemaker. Des travaux antérieurs ont montré que dans la variante HCN2, la liaison ne se produit pas de façon indépendante à chaque poche ; au contraire, les quatre sites s’influencent mutuellement de sorte que la première molécule se lie plus facilement que les suivantes, un comportement connu sous le nom de coopérativité négative. Le travail nouveau visait à découvrir exactement comment les quatre sous‑unités communiquent entre elles au cours de ce processus.
Des sous‑unités sensibles à leurs voisines
Les chercheurs ont combiné simulations informatiques et mesures expérimentales sur des fragments isolés du canal HCN2. À l’aide de longues simulations de dynamique moléculaire, ils ont observé comment la région terminale du canal — la partie qui contient les poches de liaison des nucléotides cycliques et le soi‑disant C‑linker qui relie au pore — fléchit et oscille selon le nombre de molécules de cAMP ou cGMP liées. Ils ont constaté que lorsqu’un messager se verrouillait dans une sous‑unité, il ne stabilisait pas simplement cette sous‑unité seule. Au contraire, il modifiait subtilement la stabilité de ses voisines, les rendant parfois plus rigides, parfois plus flexibles, alors que la conformation globale de la protéine changeait à peine. Ces influences de voisin à voisin dépendaient du nombre de sites occupés et de leur position autour de l’anneau, concordant avec ce que l’on attend d’une coopérativité négative.
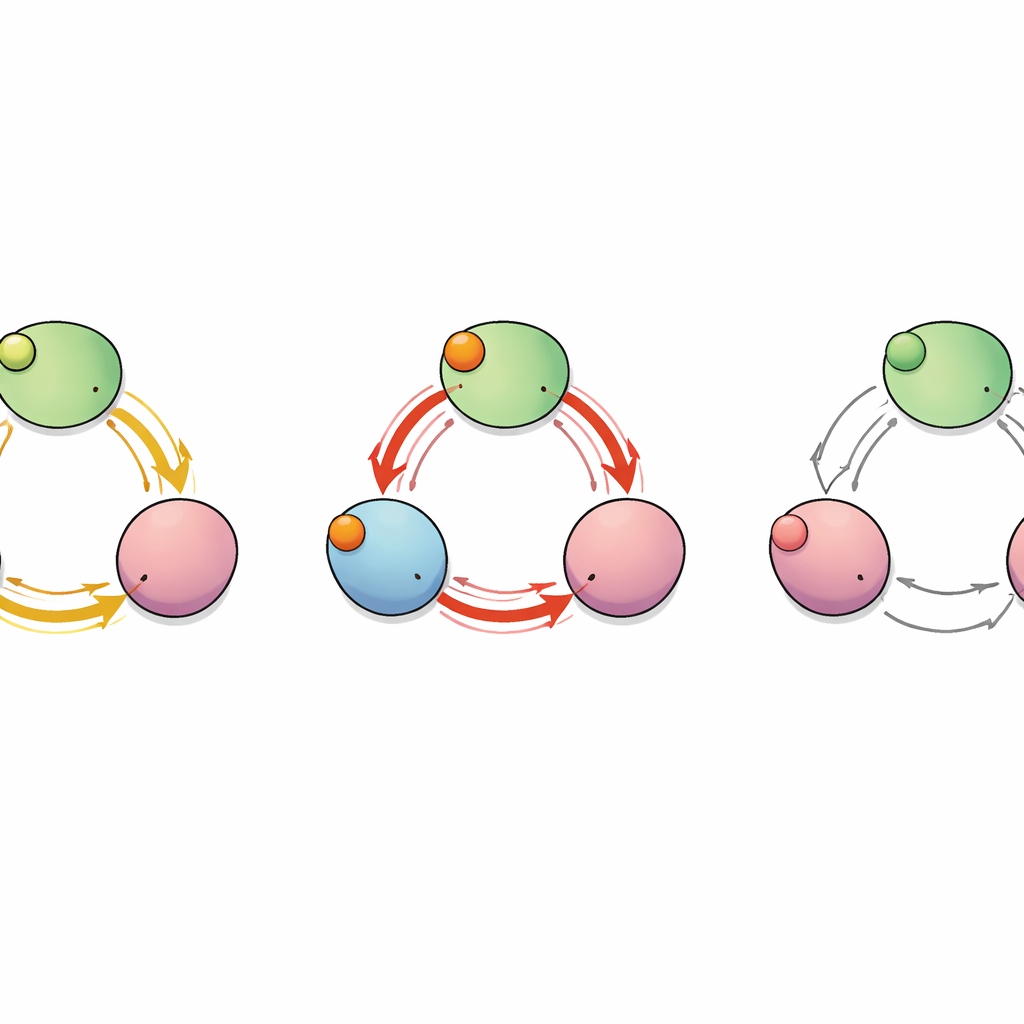
Une voie cachée entre sous‑unités
Pour cartographier la manière dont le « signal » de la liaison se propage à travers la protéine, l’équipe a traité le canal comme un réseau d’acides aminés en interaction. Ils ont calculé quels résidus bougeaient de façon corrélée pendant les simulations et utilisé des outils de théorie des graphes pour identifier les chemins de communication les plus courts et les plus efficaces depuis les poches de liaison jusqu’aux segments du C‑linker qui contrôlent le pore. Cette analyse a révélé plusieurs itinéraires possibles, mais deux se sont distingués : l’un qui reste au sein d’une seule sous‑unité et un autre qui saute d’une sous‑unité vers sa voisine. Le long de cette voie inter‑sous‑unité, un seul résidu — le glutamate en position 488 (E488) — a joué le rôle de pivot critique par lequel passait une grande partie des chemins les plus courts, ce qui suggère qu’il pourrait être un relais clé pour la liaison coopérative.
Des mutations qui interrompent la conversation
Les auteurs se sont ensuite tournés vers des expériences sur des queues de canal purifiées pour tester l’importance de cette voie. Ils ont modifié E488 et la tyrosine voisine en position 459 (Y459), située sur la sous‑unité voisine où la voie arrive. À l’aide de diffusion dynamique de la lumière, ils ont confirmé que les protéines mutantes s’assemblaient toujours en complexes à quatre sous‑unités, mais n’affichaient plus le resserrement inter‑sous‑unités induit par le ligand observé chez la protéine normale. La titration calorimétrique isotherme, qui mesure les faibles chaleurs de liaison, a révélé un changement encore plus net : le HCN2 sauvage présentait deux événements de liaison distincts, une première étape à haute affinité principalement portée par une augmentation d’entropie (plus grande mobilité interne), suivie de trois étapes à plus faible affinité. En revanche, les mutants en E488 ou Y459 ne montraient qu’un seul mode de liaison d’affinité modeste dépourvu de cette contribution entropique favorable et avaient perdu la caractéristique de coopérativité négative.
Pourquoi de subtiles variations d’entropie comptent
En réunissant ces éléments, l’étude dresse le portrait du canal HCN2 comme un anneau dynamique de quatre sous‑unités reliées par des « chemins de conversation » spécifiques. Lorsque le premier nucléotide cyclique se lie, il ajuste les mouvements de parties distantes de l’anneau via E488 et Y459, rendant les liaisons ultérieures moins favorables et modulant la réponse du pore. Cet effet est porté non pas par de grandes réarrangements structurels mais par des changements de flexibilité interne — des variations d’entropie invisibles sur des clichés statiques mais cruciales pour la fonction. Les mutations qui perturbent les résidus clés le long de cette voie inter‑sous‑unité étouffent la conversation, abolissent la coopérativité négative et sont associées à des maladies telles que l’épilepsie généralisée idiopathique. Pour un lecteur non spécialiste, la conclusion est que les commutateurs essentiels à la vie dans le cœur et le cerveau reposent sur des « chuchotements » moléculaires finement chorégraphiés entre sous‑unités protéiques, et que comprendre ces chuchotements aide à expliquer à la fois les rythmes normaux et ce qui se passe quand ils déraillent.
Citation: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Mots-clés: canal ionique HCN2, liaison des nucléotides cycliques, coopérativité négative, communication allostérique, mutation liée à l’épilepsie