Clear Sky Science · fr
Une petite molécule active allostériquement la sécrétion dépendante de SecA
Transformer le quai d’expédition bactérien en mode surmultiplié
Les bactéries survivent en exportant constamment des protéines par de petites portes dans leurs membranes. Ces exportations les aident à construire la paroi cellulaire, sécréter des toxines et s’adapter au stress—des processus au cœur de nombreuses infections. Cette étude rapporte une petite molécule, nommée HSI#6, qui fait quelque chose d’inhabituel : au lieu de bloquer cette machinerie d’exportation, elle la bascule dans un mode hyperactif et moins sélectif. Comprendre comment fonctionne cet interrupteur pourrait à la fois révéler de nouvelles stratégies antibactériennes et offrir au secteur biotech un moyen d’augmenter la sécrétion de protéines à la demande.
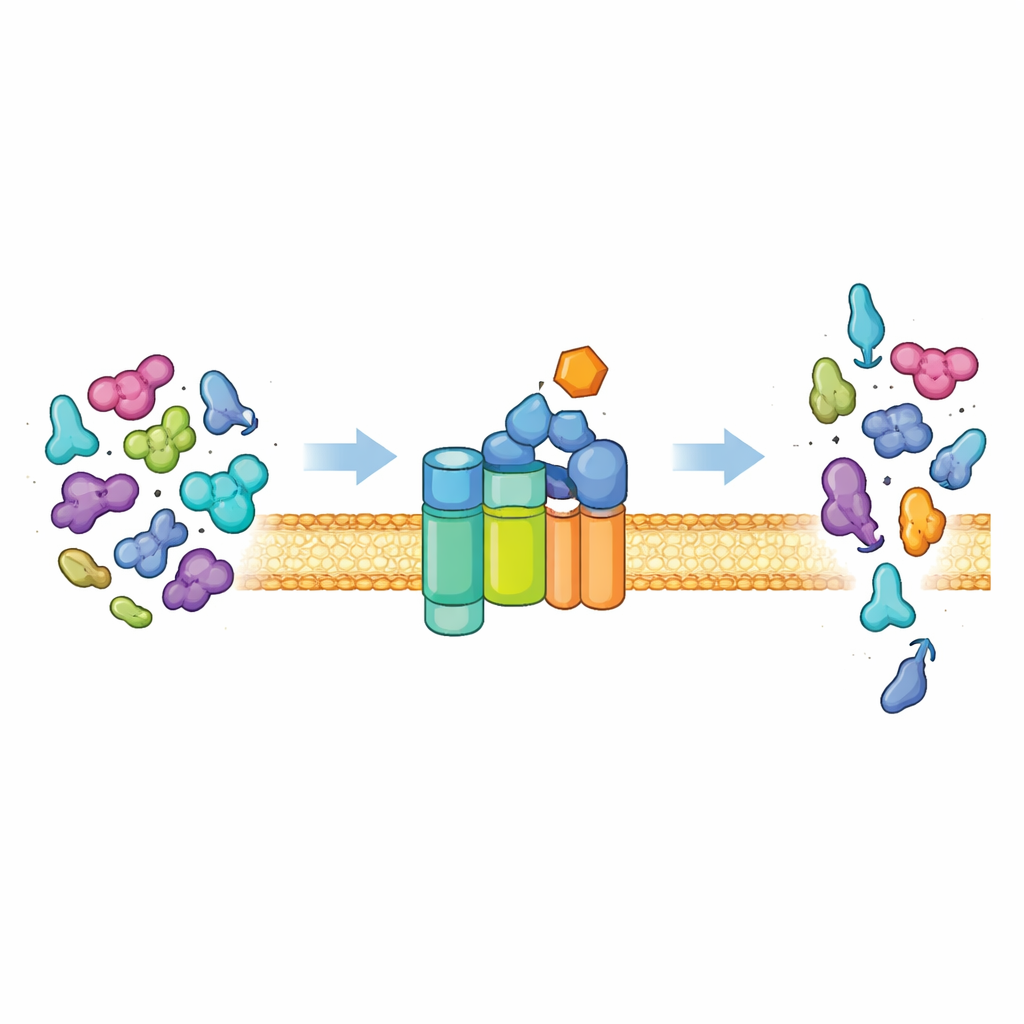
La porte de sortie des protéines de la cellule
La plupart des bactéries exportent des protéines hors de la cellule via une voie universelle connue sous le nom de système Sec. Au cœur de ce système se trouve un canal membranaire (SecYEG) et une protéine-moteur (SecA) qui consomme le carburant cellulaire (ATP) pour pousser des chaînes protéiques dépliées à travers le canal. En conditions normales, ce système est exigeant. Il exporte principalement des « préprotéines » portant des étiquettes d’adresse spéciales, appelées peptides signal, ainsi que des caractéristiques additionnelles dans leur corps principal. Ces éléments sont nécessaires pour faire passer SecA d’un état calme et peu actif à un moteur puissant. Seules les protéines présentant la bonne combinaison de signaux peuvent déclencher l’activité maximale, ce qui garantit que la cellule exporte la cargaison adéquate et maintient les protéines cytoplasmiques ordinaires à l’intérieur.
Une petite molécule qui réveille le moteur
Les chercheurs ont découvert HSI#6 lors d’un criblage de composés qui interfèrent avec la sécrétion protéique bactérienne et la croissance. Des tests biochimiques ont montré que HSI#6 se lie directement à SecA avec une affinité micromolaire et modifie son efficacité d’utilisation de l’ATP. En solution, il fait que SecA retienne l’ATP plus fermement ; lorsque SecA est attaché au canal, HSI#6 améliore à la fois la liaison de l’ATP et accélère son turnover. Ce profil est la marque d’un activateur allostérique : une molécule qui se lie à un site d’une protéine mais modifie l’activité à un autre site éloigné. Contrairement aux clients protéiques naturels, HSI#6 n’a pas besoin d’agir comme une cargaison pour stimuler le moteur—il module simplement la dynamique interne de SecA de sorte que l’ensemble du translocase devienne prêt à catalyser.
Du filtre sélectif à la nanomachine opportuniste
Une fois HSI#6 lié, le système Sec n’exige plus les étiquettes d’exportation habituelles. Dans des expériences in vitro, le composé a à peu près doublé la sécrétion d’une préprotéine standard et a rendu le complexe plus résistant à l’azoture de sodium, un inhibiteur connu de SecA. Plus remarquable, HSI#6 a permis à la machinerie « sauvage » normale de transporter des protéines dépourvues complètement de peptides signal, ainsi que des protéines qui résident normalement dans le cytoplasme. Dans des cellules bactériennes vivantes, le même effet a été observé avec des rapporteurs basés sur la phosphatase alcaline : lorsque des protéines cytoplasmiques étaient fusionnées à une enzyme sécrétée, la présence de HSI#6 a provoqué une forte augmentation de l’activité sécrétée sans changer la quantité de protéine produite. En d’autres termes, HSI#6 découple effectivement l’exportation des contrôles d’identité habituels des clients, transformant le système Sec en une pompe d’exportation à action large pour toute protéine suffisamment dépliée.
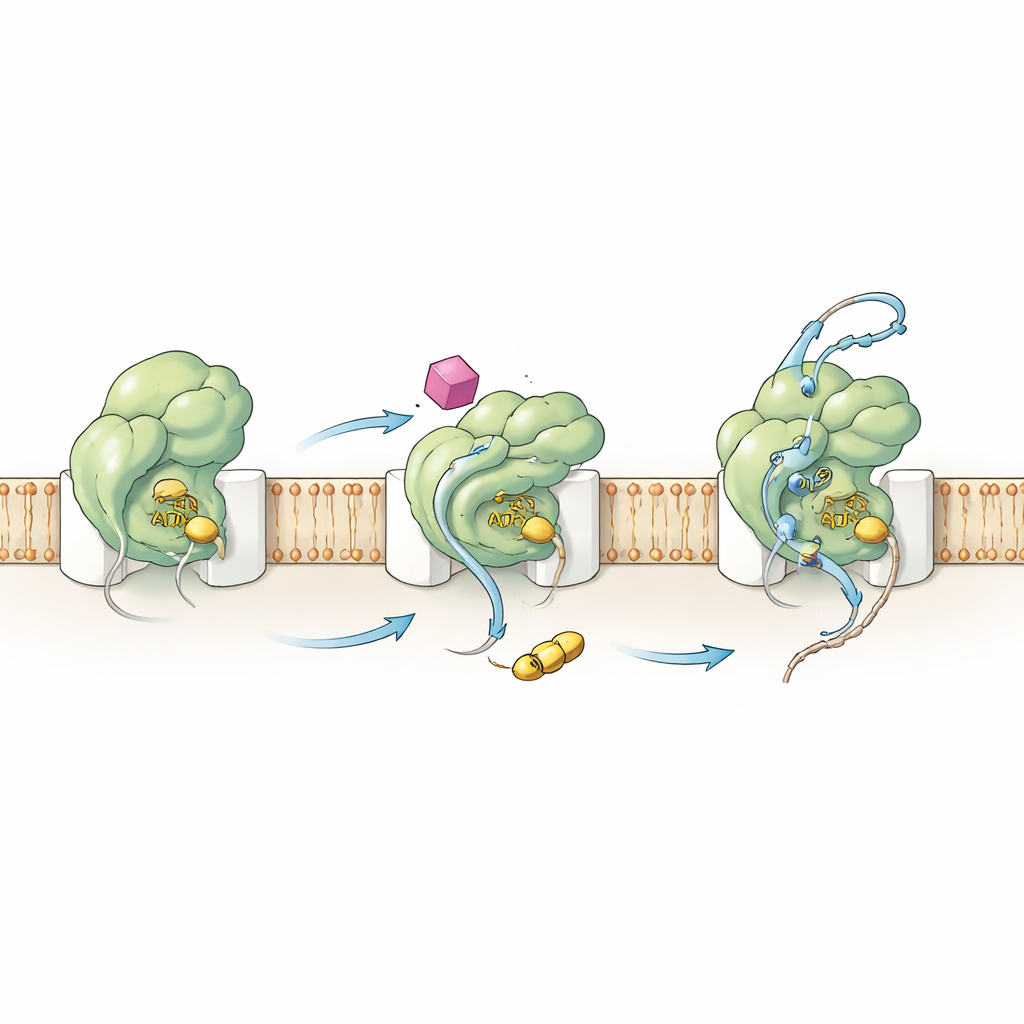
Reconfigurer le moteur depuis l’intérieur
Pour comprendre comment HSI#6 déclenche ce comportement, l’équipe a examiné à la fois la chimie et les mouvements de SecA. Des mesures cinétiques ont montré que le composé déplace l’étape clé d’activation en amont : le complexe SecA–canal devient catalytiquement actif avant même que se lie un client protéique. HSI#6 favorise aussi la libération du carburant usé (ADP) par SecA, une étape normalement lente et limitante, et soutient ainsi un cycle d’ATP plus rapide. En utilisant la spectrométrie de masse d’échange hydrogène–déutérium, les auteurs ont cartographié comment HSI#6 reconfigure la flexibilité de différentes régions de SecA. Le composé desserre sélectivement des parties de la protéine qui détectent les clients et se connectent au canal, tout en rigidifiant une région échafaudage qui héberge probablement son site de liaison. Le motif de mouvement résultant ressemble à un état déjà engagé et « activé » du translocase, ce qui suggère que HSI#6 stabilise une forme activée—favorisant possiblement même une SecA monomérique liée au canal—sans qu’aucun client soit présent.
Pourquoi cela importe pour la médecine et la biotechnologie
En montrant qu’une petite molécule peut activer allostériquement SecA et supprimer sa sélectivité habituelle des clients, ce travail révèle une nouvelle façon de contrôler une machinerie bactérienne centrale. Pour les maladies infectieuses, une telle sécrétion forcée et incontrôlée pourrait affaiblir les pathogènes en vidant leur énergie et en perturbant leurs programmes d’exportation finement réglés, faisant des activateurs de type HSI#6 des points de départ attractifs pour la conception d’antibiotiques—ou des guides pour élaborer des inhibiteurs futurs ciblant les mêmes fonctionnalités régulatrices. Pour la biotechnologie, le même principe pourrait être réutilisé pour améliorer la sécrétion de protéines recombinantes utiles, sans nécessité de peptides signal ingénierés ni de modifications génétiques complexes. En substance, l’étude démontre que le « quai d’expédition » protéique bactérien peut être reprogrammé chimiquement, ouvrant de nouvelles voies tant pour lutter contre les microbes que pour les exploiter comme usines microscopiques.
Citation: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Mots-clés: ségrégation protéique bactérienne, translocase SecA, activation allostérique, régulateurs de petite molécule, découverte d'antibiotiques