Clear Sky Science · fr
Un pseudokinase à histidine module la croissance polaire et la forme cellulaire chez Streptomyces venezuelae
Comment les bactéries construisent des corps finement ramifiés
Les bactéries filamenteuses du genre Streptomyces vivent dans le sol et forment des réseaux ramifiés de filaments qui ressemblent à des champignons microscopiques. Ces bactéries sont une source naturelle majeure d’antibiotiques, et leur succès dépend de la précision avec laquelle elles contrôlent où et comment leurs cellules croissent. Cette étude révèle une protéine jusque-là inconnue qui aide Streptomyces à stabiliser leurs pointes de croissance et à ordonner leurs ramifications, offrant un nouvel éclairage sur la façon dont des formes cellulaires complexes sont construites et maintenues.
Croissance concentrée aux extrémités
Contrairement à de nombreuses bactéries bien connues en bâtonnet qui s’étendent sur toute leur longueur, Streptomyces croissent principalement à leurs extrémités. Chaque filament, ou hyphe, s’allonge en ajoutant du matériau de paroi cellulaire uniquement dans une petite zone à l’extrémité. Cette zone de croissance est organisée par un ensemble protéique appelé polarisome. Au cœur se trouve une protéine nommée DivIVA, qui a tendance à se concentrer aux extrémités courbées et signale où le nouveau matériau de paroi doit être inséré. Lorsque de petits amas de DivIVA bourgeonnent à partir de la pointe principale et se déposent le long du côté d’une hyphe, ils peuvent mûrir en nouveaux centres de croissance, donnant naissance à des branches latérales et à un réseau mycélien finement ramifié.
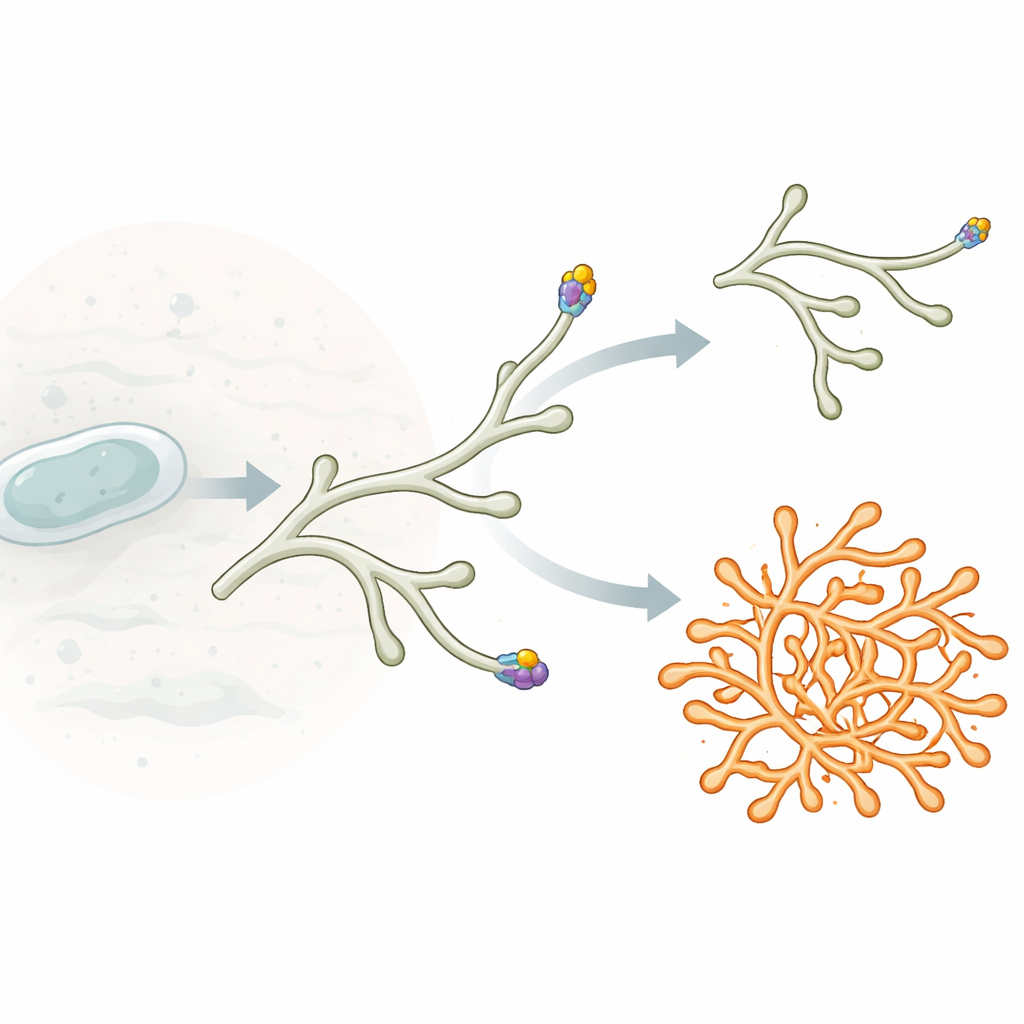
Un nouveau contrôleur de forme à la pointe
Les auteurs se sont lancés dans la recherche de composants du polarisome de Streptomyces encore inconnus. En isolant DivIVA à partir d’extraits cellulaires et en identifiant les partenaires co‑précipitants, ils ont découvert une grande protéine, désormais nommée PsmA (pour polar growth and shape modulator A). PsmA ressemble, dans son agencement de domaines, à une enzyme de signalisation bactérienne courante appelée histidine kinase, avec des régions de type capteur, un cœur catalytique central et un domaine récepteur reliés par un long segment flexible. Toutefois, une analyse plus poussée a montré que PsmA est dépourvue des acides aminés clés nécessaires au transfert de groupes phosphate et ne présente pas d’activité kinase détectable, ce qui en fait un « pseudokinase » susceptible d’agir davantage comme un partenaire structural ou un échafaudage que comme une enzyme classique.
Quand le contrôleur de forme manque
Pour sonder le rôle de PsmA, les chercheurs ont supprimé son gène dans Streptomyces venezuelae. Les colonies du mutant étaient plus petites et plus denses, avec une surface criblée. Au microscope, les hyphes végétatifs étaient plus épais, plus irréguliers et présentaient une ramification des pointes fortement augmentée. Au lieu de s’étendre de manière régulière en produisant occasionnellement des branches latérales, de nombreuses pointes se scindaient en deux ou plusieurs extrémités actives, créant un mycélium hyperramifié et compact. Il est important de noter que la capacité à former des filaments aériens et des spores restait en grande partie intacte, indiquant que PsmA agit principalement pendant la croissance végétative des pointes plutôt que lors de l’étape ultérieure de sporulation.
Maintenir la zone de croissance en un seul morceau
En marquant les protéines par fluorescence, les auteurs ont visualisé la localisation de PsmA dans des cellules vivantes. PsmA formait des points concentrés juste à l’apex des hyphes en croissance, en recouvrement étroit avec DivIVA et une autre protéine de pointe, Scy, mais distinct de FilP, qui se situe juste derrière la pointe. En l’absence de PsmA, les amas de DivIVA aux extrémités des hyphes devenaient plus larges et de forme plus irrégulière. L’imagerie en timelapse a révélé que ces amas déformés étaient beaucoup plus susceptibles de se diviser en deux parties de taille similaire. Chaque partie pilotait alors la croissance de sa propre pointe, entraînant des bifurcations très proches de la pointe originale et expliquant le motif d’hyperbranchement. Lorsque la production de PsmA était réactivée chez le mutant, les amas de DivIVA se resserraient rapidement, la forme de la pointe redevenait plus lisse et les scissions excessives diminuaient.
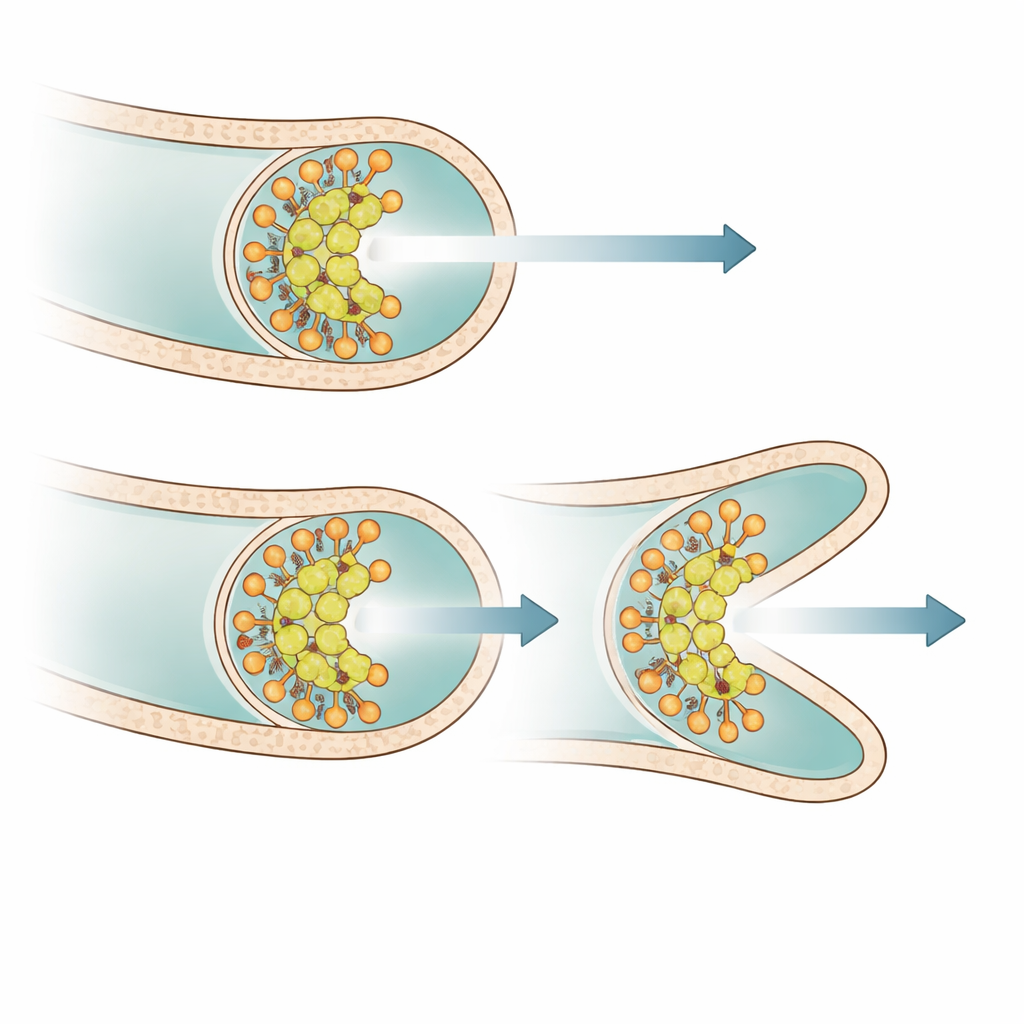
Agir en parallèle avec d’autres facteurs de pointe
PsmA n’est pas la seule protéine qui contribue à stabiliser les pointes de Streptomyces. Des travaux antérieurs avaient identifié Scy et FilP, deux protéines allongées en hélice coiled‑coil qui s’associent à DivIVA et influencent le comportement des pointes. Les doubles mutants dépourvus à la fois de PsmA et de Scy ou de FilP présentaient des défauts de croissance encore plus sévères et des mycéliums plus denses et enchevêtrés que ceux de tout mutant simple, tout en restant viables. Ce schéma suggère que PsmA agit largement en parallèle de Scy et FilP : les trois contribuent de manière partiellement indépendante à maintenir la cohésion de la zone de croissance et à empêcher sa fragmentation en multiples pointes concurrentes.
Ce que cela signifie pour l’architecture bactérienne
Pris ensemble, ces résultats présentent PsmA comme un partenaire non enzymatique qui affine la stabilité et la dynamique du polarisome à base de DivIVA aux pointes des hyphes de Streptomyces. Plutôt que d’agir en commutant des gènes via des voies de signalisation classiques, PsmA semble fonctionner directement à l’extrémité en croissance, probablement comme un organisateur structurel aidant les amas de DivIVA à maintenir une zone de croissance focalisée et unique. En l’absence de PsmA, la machinerie de la pointe devient trop instable, se divise trop souvent et produit une ramification excessive. Comprendre ce type de contrôle architectural local enrichit non seulement nos connaissances fondamentales en biologie cellulaire bactérienne, mais peut aussi éclairer des efforts pour manipuler les modes de croissance de Streptomyces en biotechnologie et pour la production d’antibiotiques.
Citation: Singh Mavi, P., Flärdh, K. A histidine pseudokinase modulates polar growth and cell shape in Streptomyces venezuelae. Commun Biol 9, 345 (2026). https://doi.org/10.1038/s42003-026-09620-z
Mots-clés: Streptomyces, polarité cellulaire, morphogenèse bactérienne, pseudokinase, ramification hyphal