Clear Sky Science · fr
L’alimentation limitée la nuit perturbe la spermatogenèse chez la souris via l’homéostasie du KYNA dérivé du microbiote intestinal
Pourquoi le moment de vos repas pourrait compter pour les futurs pères
Beaucoup savent que sauter les en-cas nocturnes ou pratiquer le jeûne intermittent peut aider à contrôler le poids et la glycémie. Mais cette étude chez la souris pose une question différente : limiter la prise alimentaire à certaines heures pourrait-il nuire à la fertilité masculine si ce timing entre en conflit avec l’horloge interne du corps ? En suivant comment les horaires d’alimentation remodèlent les bactéries intestinales et un médiateur chimique peu connu, les chercheurs mettent au jour une chaîne d’événements qui aboutit à un nombre réduit de spermatozoïdes de moindre qualité.
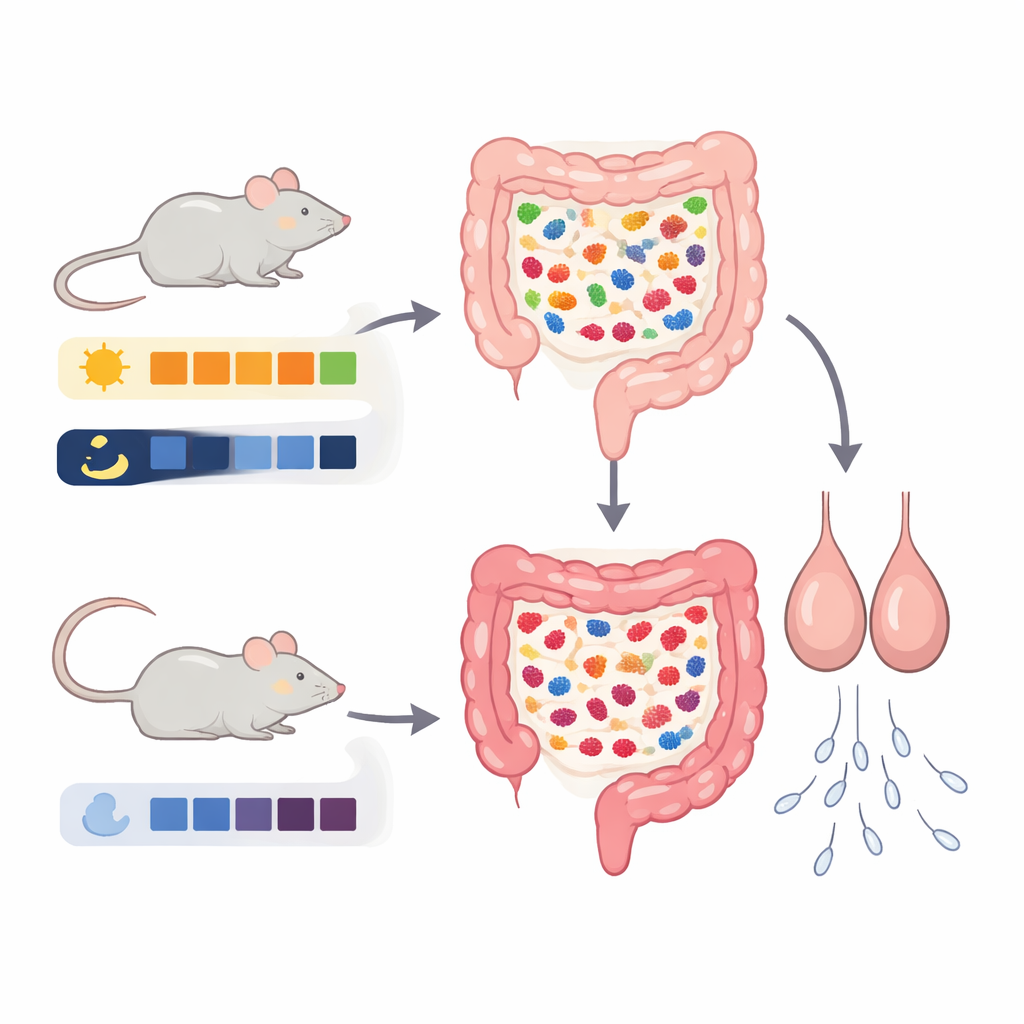
Fenêtres d’alimentation et horloge interne
L’équipe a travaillé avec des souris mâles et a établi trois schémas d’alimentation. Un groupe pouvait manger à volonté à tout moment. Un deuxième groupe ne pouvait manger que le jour, et un troisième groupe seulement la nuit. Important : ces souris n’étaient pas mises à un régime calorique restreint ; elles pouvaient consommer autant qu’elles voulaient, seulement à des moments différents. Après quatre semaines, les souris nourries uniquement la nuit présentaient des testicules plus petits et une concentration et une mobilité des spermatozoïdes réduites, bien qu’elles n’aient pas consommé moins au total. Les niveaux d’hormones liées au stress ont changé, tandis que l’hormone du sommeil est restée à peu près stable, ce qui suggère que le dommage provenait davantage des réponses métaboliques et de stress aux repas mal synchronisés que d’une simple perturbation de l’horloge maîtresse cérébrale.
Ce qui dysfonctionnait dans les testicules
À l’examen microscopique des tissus testiculaires, les scientifiques ont constaté que les souris nourries la nuit avaient moins de cellules spermatogoniales en cours de maturation intermédiaire, tandis que les cellules souches initiales et les cellules de soutien étaient pour l’essentiel inchangées. Les indicateurs de dommages chimiques liés au stress oxydatif étaient plus élevés, suggérant que l’environnement testiculaire était devenu plus hostile et moins équilibré. Fait intéressant, les toutes dernières étapes du remodelage du spermatozoïde — la formation de l’acrosome à la tête du spermatozoïde — n’étaient pas fortement affectées. Cela pointe vers les stades précoces et intermédiaires de la spermatogenèse comme points faibles lorsque l’alimentation est désynchronisée par rapport aux rythmes du corps.
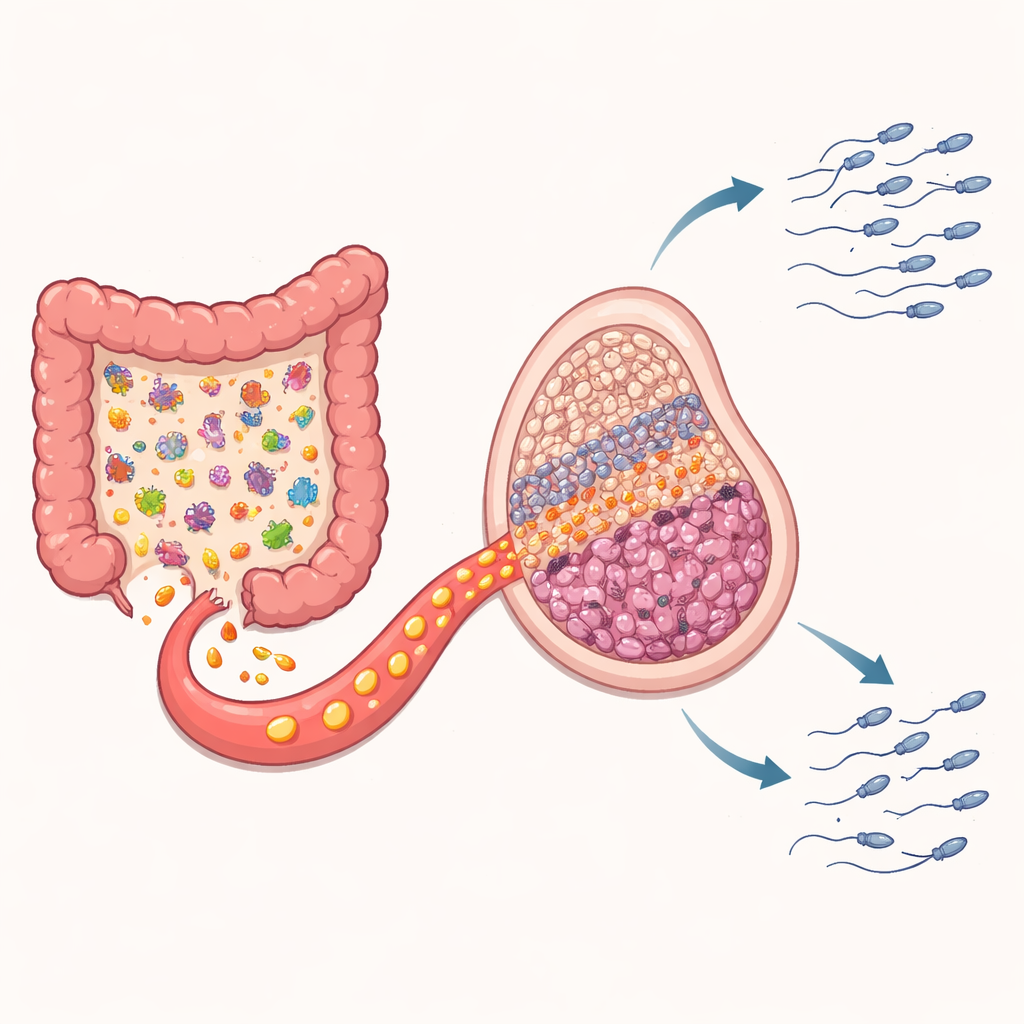
Le rôle caché de l’intestin et un médiateur chimique clé
Parce que le microbiote intestinal est connu pour varier avec le moment des repas et pour envoyer des signaux à travers le corps, les chercheurs ont ensuite examiné les communautés intestinales des animaux. Les souris nourries uniquement la nuit présentaient une réorganisation nette des bactéries intestinales par rapport aux groupes en libre accès et à alimentation diurne. Certaines espèces associées dans des travaux antérieurs à l’inflammation et à une mauvaise qualité du sperme sont devenues plus abondantes. Lorsque l’équipe a profilé des centaines de petites molécules produites dans l’intestin, une s’est démarquée : l’acide kynurénique, ou KYNA, un produit de dégradation de l’acide aminé tryptophane. Les niveaux de KYNA étaient plus élevés dans l’intestin et dans le sang uniquement chez les souris nourries la nuit. Des analyses statistiques ont lié cette hausse de KYNA à la prolifération de groupes bactériens particuliers, soutenant l’idée que des microbes altérés entraînaient ce changement.
Tester si le KYNA nuit lui-même aux spermatozoïdes
Pour déterminer si le KYNA n’était qu’un témoin ou un agent actif, les chercheurs ont administré du KYNA par voie orale à des souris saines pendant quatre semaines, à des doses visant à reproduire les niveaux augmentés observés avec l’alimentation nocturne. Les résultats furent remarquablement similaires à ceux du groupe nourri la nuit : réduction de la taille des testicules, diminution des spermatozoïdes en cours de développement, et baisse du nombre et de la motilité des spermatozoïdes, tandis que les taux de testostérone restaient globalement stables. En culture cellulaire, le KYNA s’est avéré toxique directement pour des cellules en développement ressemblant à des spermatozoïdes à des doses élevées, mais était moins nocif pour les cellules productrices d’hormones. Dans le tissu testiculaire, le KYNA a abaissé l’expression d’un type de récepteur et activé fortement une autre voie, connue pour déclencher la mort cellulaire des cellules germinales. Ensemble, ces résultats suggèrent que l’excès de KYNA, produit dans l’intestin et transporté par le sang, joue un rôle central dans l’arrêt de la production spermatique.
Ce que cela signifie pour les hommes et le timing des repas
Pour le grand public, le message n’est pas que toute alimentation à heures restreintes soit nocive. En fait, les souris limitées à manger le jour dans cette étude n’ont pas montré les mêmes problèmes reproductifs, et certains essais chez l’humain indiquent des bénéfices métaboliques d’un jeûne bien calibré. Le travail met plutôt en lumière que le « quand » nous mangeons peut influencer la fertilité masculine, du moins chez la souris, en remodelant le microbiote intestinal et en augmentant un médiateur chimique qui sabote discrètement la spermatogenèse. Bien que des recherches supplémentaires soient nécessaires pour confirmer à quel point ces résultats s’appliquent aux hommes, notamment en raison des différences d’espèces et de la complexité des modes de vie, l’étude apporte une note de prudence : aligner les habitudes alimentaires sur les rythmes quotidiens naturels et préserver une communauté intestinale saine pourrait être important non seulement pour le poids et la glycémie, mais aussi pour la protection de la capacité à engendrer des enfants.
Citation: Yang, D., Xie, D., Li, C. et al. Nighttime-restricted feeding disrupts spermatogenesis in mice via gut microbiota-derived KYNA homeostasis. Commun Biol 9, 354 (2026). https://doi.org/10.1038/s42003-026-09619-6
Mots-clés: fertilité masculine, alimentation à heure limitée, microbiote intestinal, acide kynurénique, rythme circadien