Clear Sky Science · fr
LncRNA P4HA2-AS1 entraîne la fibrose interstitielle rénale via l’ubiquitination en K63 de l’ULK1 médiée par TRIM32 et une dysrégulation de l’autophagie
Pourquoi la cicatrisation rénale compte
La maladie rénale chronique touche des centaines de millions de personnes dans le monde et progresse souvent silencieusement jusqu’à ce que la dialyse ou la greffe deviennent les seules options pour survivre. Au cœur de ce déclin se trouve un processus appelé cicatrisation, où le tissu rénal normal est progressivement remplacé par une matière rigide et non fonctionnelle. Cette étude pose une question simple mais cruciale : quels interrupteurs moléculaires à l’intérieur des cellules rénales les poussent vers cette cicatrisation néfaste, et peut‑on inverser ces commutateurs ?
Un interrupteur ARN caché dans les cellules rénales
Nos reins filtrent le sang à l’aide de réseaux élaborés de petits tubules. Lorsque ces tubules sont endommagés par une obstruction des voies urinaires, une hyperglycémie, ou une perte soudaine d’apport sanguin, ils peuvent répondre en déposant du tissu cicatriciel entre les cellules. Les chercheurs ont analysé les reins de souris soumises à plusieurs types de lésion et les ont comparés à des reins sains par séquençage de l’ARN, une technique qui lit quels gènes sont activés. Ils ont découvert qu’une molécule peu connue appelée P4HA2‑AS1, un ARN long non codant qui ne produit pas de protéine, était de façon constante élevée dans les reins endommagés formant des cicatrices et dans des cellules rénales humaines soumises au stress en laboratoire. Cet ARN se trouvait principalement dans la partie riche en fluide des cellules, suggérant qu’il pourrait réguler d’autres protéines à cet emplacement. 
Réduire l’ARN pour protéger le rein
Pour tester si P4HA2‑AS1 est simplement un témoin ou un véritable moteur des dommages, l’équipe a diminué son niveau chez la souris et dans des cellules rénales humaines cultivées. Dans un modèle murin bien établi où un uretère est ligaturé pour provoquer une obstruction prolongée, la diminution de cet ARN par un vecteur viral ciblé a atténué de nombreux signes de fibrose : les tubules restaient plus intacts, il y avait moins de collagène et d’autres protéines cicatricielles entre les cellules, et les marqueurs de fonction rénale dans le sang se sont améliorés. En culture de cellules rénales humaines, la réduction de P4HA2‑AS1 a aussi limité la réponse à un signal puissant de fibrose, le TGF‑β, entraînant une moindre production de fibronectine, de collagène et d’autres facteurs pro‑fibrotiques. Ces expériences montrent que cet ARN n’est pas seulement un marqueur de lésion mais alimente activement le processus de cicatrisation.
Autophagie : du ménage au dommage
Les chercheurs se sont ensuite demandé comment cet ARN cause ses effets. Leurs données d’expression génique et d’imagerie ont pointé vers l’autophagie, le système de recyclage cellulaire qui dégrade les protéines et organites usés. Dans des conditions normales, l’autophagie est un processus d’entretien bénéfique, mais lorsqu’elle est trop active et trop prolongée, elle peut pousser les reins blessés vers une réparation inadaptée et la fibrose. Dans des cellules rénales stressées, P4HA2‑AS1 a augmenté le flux de matériel via l’autophagie, conduisant à une accumulation de vésicules de recyclage. Lorsque l’ARN était bloqué, ce recyclage excessif retombait vers la normale, à la fois dans les cellules et dans les reins de souris obstructées. Des souris dépourvues d’ULK1, une enzyme initiatrice centrale de l’autophagie, étaient également protégées de la fibrose, et chez ces animaux la surexpression de P4HA2‑AS1 ne pouvait plus aggraver les lésions, reliant ainsi de manière robuste les effets de l’ARN à cette voie.
Une chaîne moléculaire en trois maillons
En creusant davantage, l’équipe a utilisé des techniques biochimiques d’« appâtage » pour identifier les protéines qui se lient physiquement à P4HA2‑AS1. Une protéine s’est distinguée : TRIM32, une enzyme qui marque d’autres protéines avec de petits « drapeaux » moléculaires appelés ubiquitines. L’ARN se lie à TRIM32 et le protège de la dégradation, augmentant ainsi ses niveaux à l’intérieur des cellules rénales. TRIM32 stabilisé, à son tour, attache un type spécifique de chaîne d’ubiquitine à ULK1. Plutôt que d’envoyer ULK1 à la destruction, cette chaîne agit comme un amplificateur, renforçant la capacité d’ULK1 à déclencher l’autophagie. Lorsque les scientifiques ont soit supprimé TRIM32 chez la souris soit l’ont silencé dans des cellules rénales, la fibrose et l’autophagie excessive ont toutes deux diminué. La réintroduction de TRIM32 dans des cellules où P4HA2‑AS1 avait été bloqué a partiellement restauré la réponse fibrosante, montrant que cette enzyme est un maillon intermédiaire clé de la chaîne. 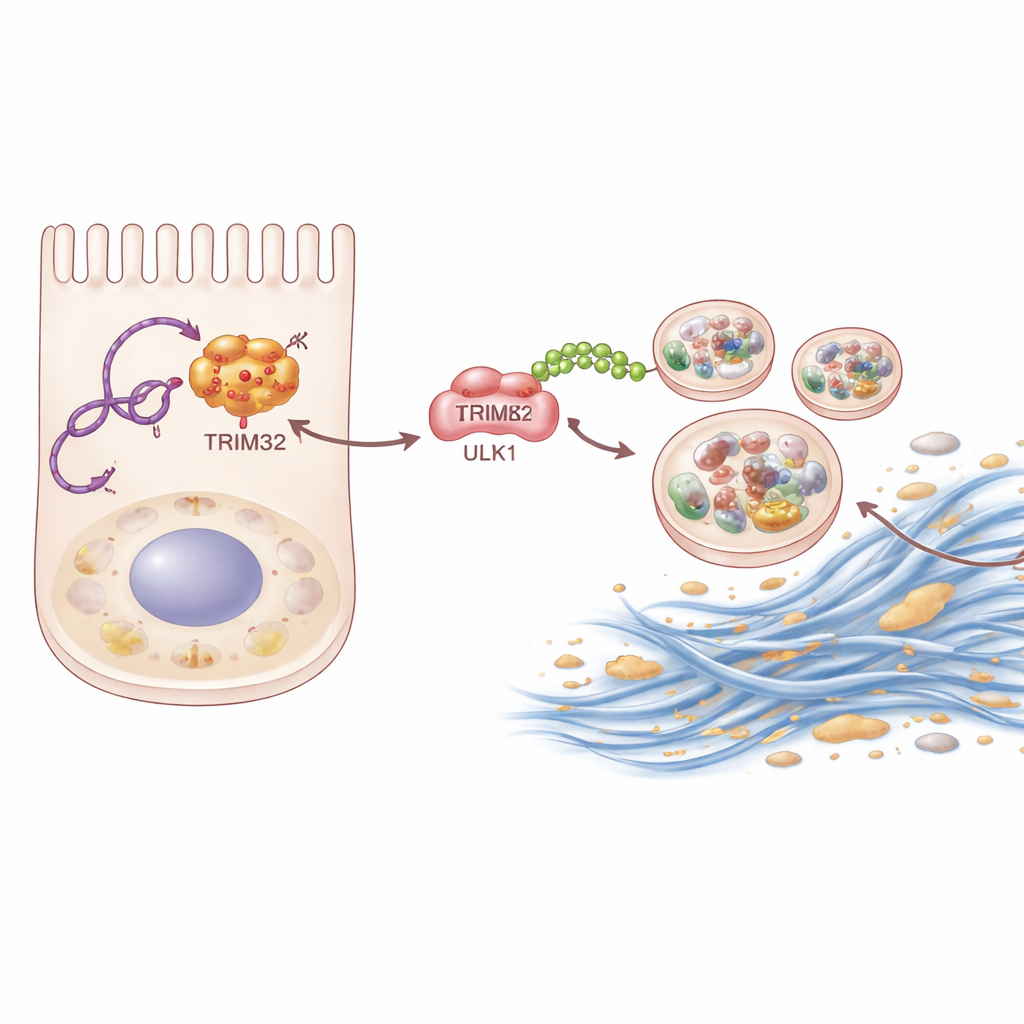
De nouvelles voies vers des reins plus souples
Pris ensemble, ces travaux révèlent une voie moléculaire jusqu’ici inconnue qui relie ARN long non codant, marquage protéique et recyclage cellulaire à l’accumulation de tissu cicatriciel rénal. Dans les reins lésés, P4HA2‑AS1 augmente, stabilise TRIM32, suractive ULK1 et pousse l’autophagie au‑delà de son rôle bénéfique, favorisant finalement l’accumulation de protéines fibrosantes et la perte de fonction. Pour un public non spécialiste, l’essentiel est que la cicatrisation rénale n’est pas une boîte noire inévitable : elle est pilotée par des interrupteurs identifiables et potentiellement ciblables par des traitements. Cibler cet axe P4HA2‑AS1–TRIM32–ULK1 — en abaissant l’ARN fautif, en modérant TRIM32 ou en ajustant l’activité d’ULK1 — pourrait un jour offrir de nouvelles thérapies pour ralentir ou prévenir la progression de la maladie rénale chronique.
Citation: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Mots-clés: maladie rénale chronique, fibrose rénale, autophagie, ARN long non codant, tubules rénaux