Clear Sky Science · fr
Les inhibiteurs de la transcriptase inverse permettent la production de spermatides fertiles à partir de testicules fœtaux de souris in vitro
Transformer des cellules germinales précoces en spermatozoïdes fonctionnels
Les traitements de l’infertilité et la recherche fondamentale dépendent tous deux de la compréhension de la façon dont les cellules germinales immatures du testicule se transforment en spermatozoïdes. Cette étude montre qu’il est désormais possible d’amener de très jeunes testicules fœtaux de souris, prélevés juste après la détermination du sexe de l’embryon, à accomplir entièrement cette transformation en culture. En ajustant soigneusement l’environnement chimique et le niveau d’oxygène, les chercheurs ont non seulement produit des cellules ressemblant à des spermatozoïdes matures, mais les ont aussi utilisées pour engendrer une descendance saine et fertile.
Pourquoi la maturation précoce du testicule est difficile à reproduire
La production de spermatozoïdes hors du corps a déjà été réalisée en utilisant des tissus testiculaires de souriceaux nouveau-nés ou plus âgés, mais l’efficacité restait faible, et les tentatives avec des tissus fœtaux beaucoup plus précoces échouaient largement. À ce stade précoce, le testicule est encore en train d’assembler son architecture interne, et les cellules germinales connaissent des remaniements profonds de la manière dont leur ADN est empaqueté et marqué. Reproduire cette chorégraphie complexe en culture est délicat, et les cultures antérieures progresaient rarement au-delà des premières étapes lorsqu’on partait de testicules collectés autour du jour embryonnaire 12,5, peu après la détermination du sexe de l’embryon.
Emprunter des antiviraux pour protéger les cellules en développement
L’équipe s’est intéressée à un obstacle caché : des éléments d’ADN mobiles appelés rétrotransposons, capables de se copier et de s’insérer à de nouveaux endroits du génome. Dans les testicules in vivo, ces éléments sont strictement contrôlés, en particulier dans les cellules germinales. En culture, toutefois, les auteurs ont constaté une activité des rétrotransposons beaucoup plus élevée, tandis que les gènes de défense des cellules étaient moins actifs. Ce déséquilibre corrélait avec un mauvais développement spermatique. Parce que les rétrotransposons utilisent une enzyme transcriptase inverse, semblable à celle de certains virus, les chercheurs ont testé plusieurs médicaments initialement conçus comme inhibiteurs de la transcriptase inverse. Un mélange spécifique de trois médicaments, appelé AEC, a à peu près doublé la fraction de cellules spermatogéniques et triplé plus de trois fois la part de cellules haploïdes ressemblant à des spermatozoïdes dans des testicules néonataux cultivés par rapport aux témoins non traités.
Des minuscules testicules fœtaux à des spermatozoïdes fonctionnels
Muni de ce cocktail médicamenteux, le groupe s’est tourné vers des testicules fœtaux. Dans des tissus prélevés un peu avant la naissance, les inhibiteurs ont favorisé l’apparition de spermatides avancées. Plus frappant encore, lorsqu’ils ont cultivé des testicules d’embryons au jour 12,5, un stade jamais auparavant montré capable d’achever la spermatogenèse in vitro, ils ont pu générer des spermatides rondes et allongées. Les gains les plus importants sont apparus lorsqu’ils ont combiné le mélange d’inhibiteurs avec une atmosphère à faible teneur en oxygène qui mimait mieux les conditions du développement in utero. Dans ces conditions hypoxiques, environ un tiers de la surface tissulaire présentait des marqueurs de développement germinal avancé, et des spermatozoïdes pourvus d’un flagelle ont pu être récupérés des cultures.
Vérifier si les spermatides fabriquées en laboratoire fonctionnent réellement
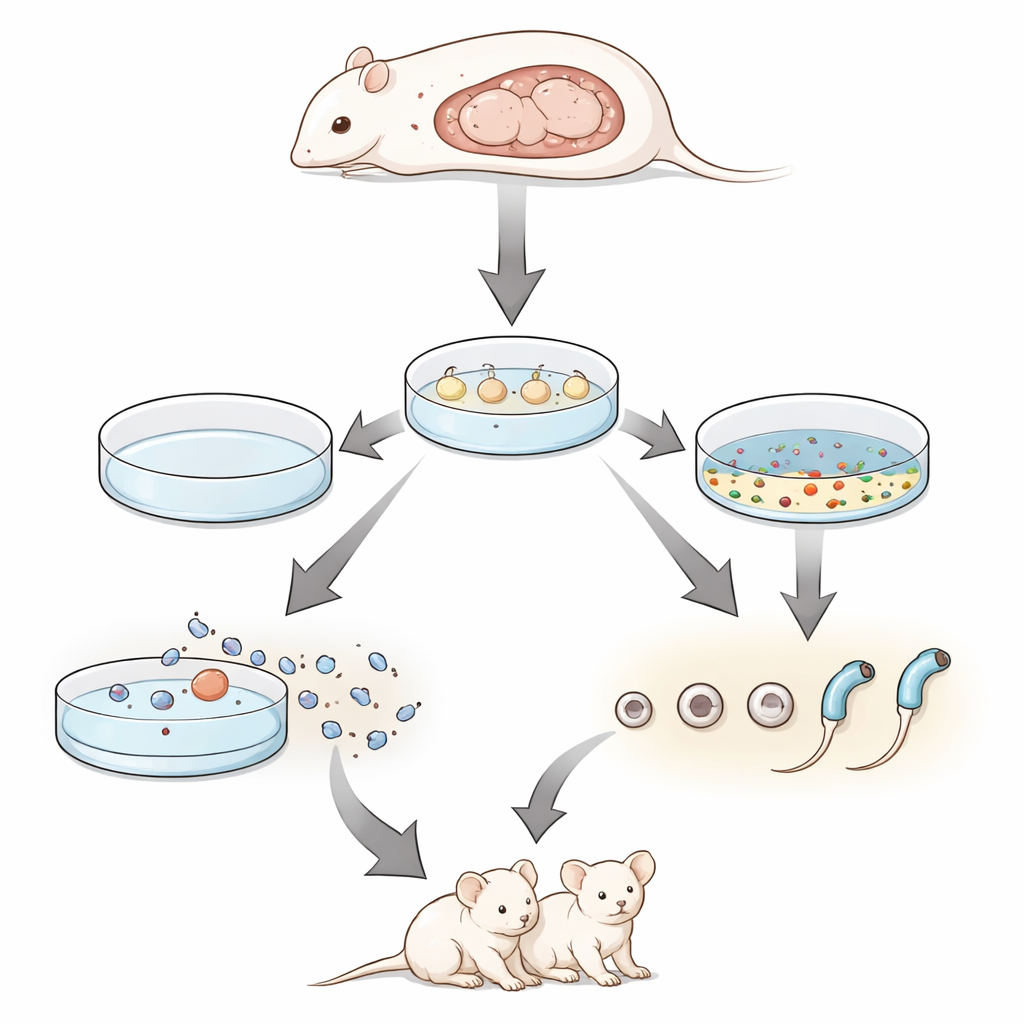
Pour savoir si ces cellules issues de cultures in vitro étaient vraiment fonctionnelles, l’équipe a utilisé une technique appelée injection de spermatide ronde. Ils ont isolé des spermatides rondes à partir des testicules fœtaux cultivés et les ont injectées dans des ovocytes de souris préalablement activés légèrement. Les embryons obtenus ont été transférés chez des mères porteuses. À partir de seulement deux fragments testiculaires cultivés, la procédure a donné plusieurs souriceaux vivants, dont beaucoup portaient un gène marqueur fluorescent confirmant leur origine en culture. Lorsque ces animaux de première génération ont été laissés s’accoupler, ils ont produit des portées de taille normale de descendants en bonne santé de deuxième génération, démontrant que les spermatides dérivées en laboratoire pouvaient soutenir non seulement le développement jusqu’à la naissance mais aussi la pleine fertilité.
Comment le blocage de l’ADN mobile peut permettre de futures thérapies
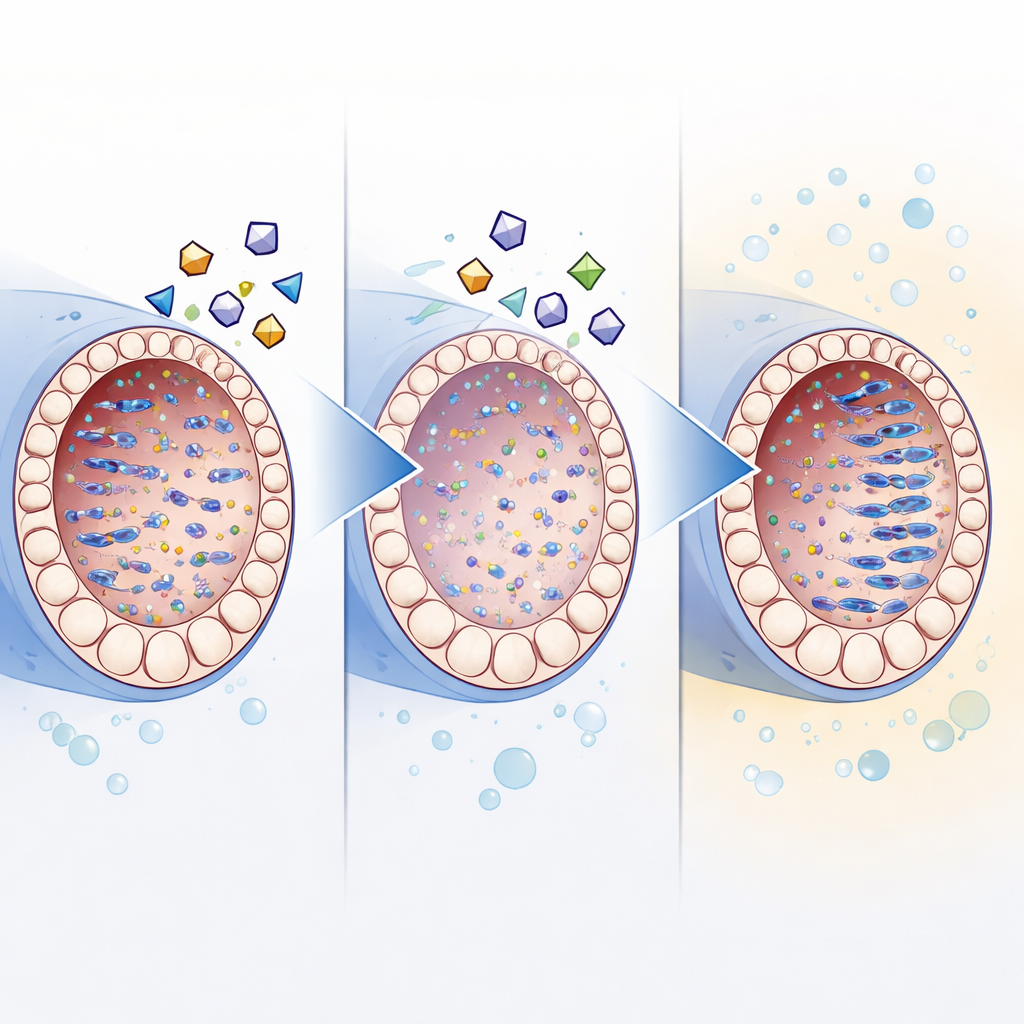
Des expériences supplémentaires ont soutenu l’idée que les inhibiteurs de la transcriptase inverse aident principalement en maîtrisant l’activité de l’ADN mobile. Par rapport à des testicules du même âge in vivo, les testicules en culture présentaient des niveaux plus élevés de protéines de rétrotransposons et des copies supplémentaires de leur ADN, ainsi qu’une expression réduite des mécanismes naturels de mise en silence des cellules. L’ajout du cocktail d’inhibiteurs a réduit cette accumulation, tout en améliorant la maturation des cellules germinales. Bien que les médicaments aient légèrement ralenti la croissance tissulaire globale, les tentatives de compenser cet effet par des additifs à base de sérum n’ont pas amélioré la production de spermatozoïdes, ce qui suggère que la croissance et la différenciation correcte doivent être soigneusement équilibrées.
Ce que cela signifie pour la science de la reproduction
Ce travail montre que des testicules fœtaux très immatures contiennent déjà tous les ingrédients nécessaires pour construire une usine à spermatozoïdes fonctionnelle, à condition que l’environnement protège leur génome et reproduise des aspects clés de la vie in utero. En combinant des médicaments de type antiviral avec une faible teneur en oxygène, les chercheurs ont créé un système de culture qui reconstitue la spermatogenèse complète à partir d’un des stades les plus précoces testés à ce jour et produit des descendants qui grandissent et se reproduisent normalement. Bien que l’étude concerne des souris et soit encore loin d’une application clinique, elle ouvre une fenêtre puissante sur les tout premiers pas du développement des cellules germinales mâles et fournit des indices qui pourraient un jour aider à préserver ou restaurer la fertilité chez des patients dont les cellules reproductrices ont été endommagées tôt dans la vie.
Citation: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Mots-clés: spermatogenèse in vitro, culture de testicule fœtal, inhibiteurs de la transcriptase inverse, rétrotransposons, fertilité masculine