Clear Sky Science · fr
L’obésité nuit à la spermatogenèse via la ferroptose des cellules de Leydig induite par le miR-122-5p exosomal d’origine hépatique
Pourquoi le poids et la fertilité sont liés
L’obésité est le plus souvent abordée sous l’angle des maladies cardiovasculaires et du diabète, mais elle peut aussi saper discrètement la fertilité masculine. Cette étude menée chez la souris révèle une manière surprenante par laquelle un régime riche en graisses peut réduire la testostérone et altérer la production de spermatozoïdes : le foie envoie dans le sang de minuscules « bulles de message » qui déclenchent un type particulier de mort cellulaire dans les cellules productrices d’hormones des testicules. Comprendre cette communication cachée du foie vers les testicules peut aider à expliquer pourquoi les hommes en surpoids souffrent souvent d’un faible taux de testostérone et d’infertilité, et orienter vers de nouvelles cibles thérapeutiques.
Courrier caché entre organes
Nos organes communiquent en permanence entre eux par des hormones et d’autres messagers chimiques. Une forme de cette communication utilise les exosomes — des vésicules de taille nanométrique libérées par les cellules, transportant lipides, protéines et matériel génétique. Les chercheurs ont commencé par des souris nourries soit avec un régime normal, soit avec un régime riche en graisses induisant obésité, résistance à l’insuline et dysrégulation de la glycémie. Les souris obèses avaient des testicules plus petits et moins actifs : leur nombre de spermatozoïdes, leurs taux de testostérone, ainsi que la taille et le nombre des tubes séminifères producteurs de spermatozoïdes étaient réduits. L’examen des marqueurs cellulaires clés dans les testicules montrait moins de cellules de Leydig productrices de testostérone et moins de cellules spermatiques aux stades précoces et tardifs, confirmant que toute la chaîne de fabrication des spermatozoïdes était compromise. 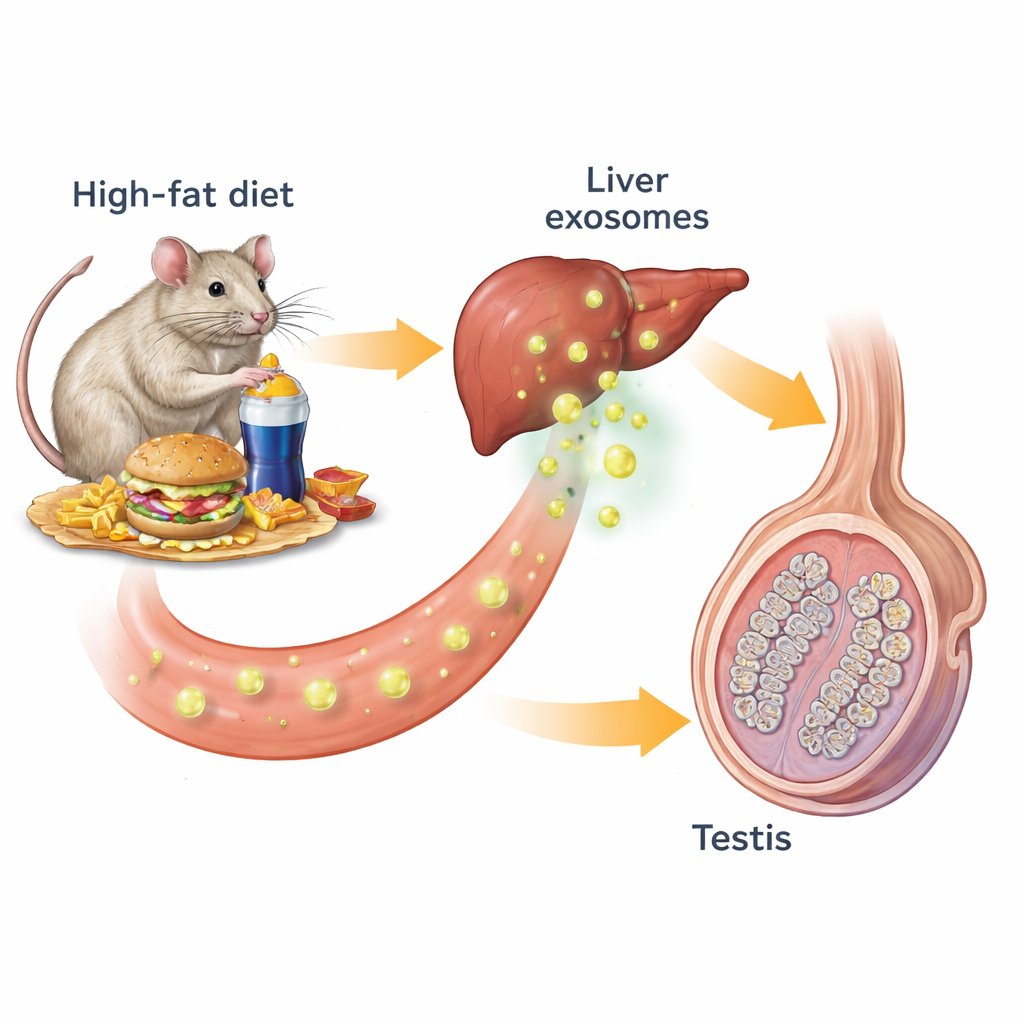
Les exosomes propagent les dégâts
Pour tester si les exosomes circulants contribuent à ces dommages, les scientifiques ont purifié des exosomes issus du sang de souris obèses et maigres. L’injection d’exosomes provenant de souris obèses à des souris saines et maigres suffisait à reproduire de nombreux troubles : les receveuses développaient des signes de perturbation métabolique, leurs taux de testostérone diminuaient, et leur compte de spermatozoïdes ainsi que l’architecture testiculaire se détérioraient. Bloquer la libération d’exosomes chez les souris obèses avec un médicament appelé GW4869 a largement inversé ces changements, restaurant les chiffres de spermatozoïdes, la testostérone et une architecture testiculaire normale. Ces résultats montrent que les exosomes dans le sang ne sont pas de simples témoins ; ils véhiculent activement des signaux délétères de l’obésité vers le système reproducteur.
Une forme toxique de mort cellulaire
L’équipe a ensuite cherché ce que faisaient précisément les exosomes aux cellules de Leydig. Ils se sont concentrés sur la ferroptose, une forme de mort cellulaire dépendante du fer, caractérisée par une accumulation de fer, des dommages oxydatifs aux lipides et des mitochondries endommagées — les centrales énergétiques de la cellule. Chez les souris obèses et chez les souris saines ayant reçu des exosomes issus d’animaux obèses, les testicules présentaient des niveaux plus élevés de fer et de malonaldéhyde (un produit dérivé de la peroxydation lipidique), ainsi que des lésions mitochondriales nettes à l’électromicroscope. Le traitement des souris obèses avec un composé bloquant la ferroptose, le Ferrostatin‑1, a préservé les cellules de Leydig, augmenté la testostérone et le nombre de spermatozoïdes, et amélioré la santé mitochondriale. En culture cellulaire, le même composé a protégé des cellules de Leydig isolées contre la mort et le stress oxydatif induits par des exosomes d’animaux obèses. Ensemble, ces expériences identifient la ferroptose comme un maillon clé entre l’obésité et l’effondrement de la production de testostérone.
Le message hépatique et l’interrupteur SCD2
Pour repérer le message contenu dans les exosomes, les chercheurs ont séquencé leur cargaison en petits ARN et ont trouvé qu’un microARN particulier, le miR‑122‑5p, était fortement augmenté dans les exosomes des souris obèses. Ce microARN était particulièrement abondant dans le foie et dans les exosomes d’origine hépatique, et ces exosomes hépatiques pouvaient être tracés jusqu’aux testicules. Lorsque les niveaux de miR‑122‑5p étaient diminués expérimentalement dans les exosomes, les cellules de Leydig étaient moins susceptibles de subir la ferroptose et la production de testostérone s’améliorait, même si les animaux restaient métaboliquement malades. Des tests supplémentaires ont montré que le miR‑122‑5p réprime directement un gène appelé Scd2, qui aide à convertir certaines graisses en formes protégeant les cellules des dommages oxydatifs. La réduction de Scd2 dans les cellules de Leydig les rendait plus vulnérables à la ferroptose et abaissait la testostérone, tandis que l’augmentation de Scd2 chez les souris obèses rétablissait partiellement les niveaux hormonaux, la production de spermatozoïdes et la structure mitochondriale. 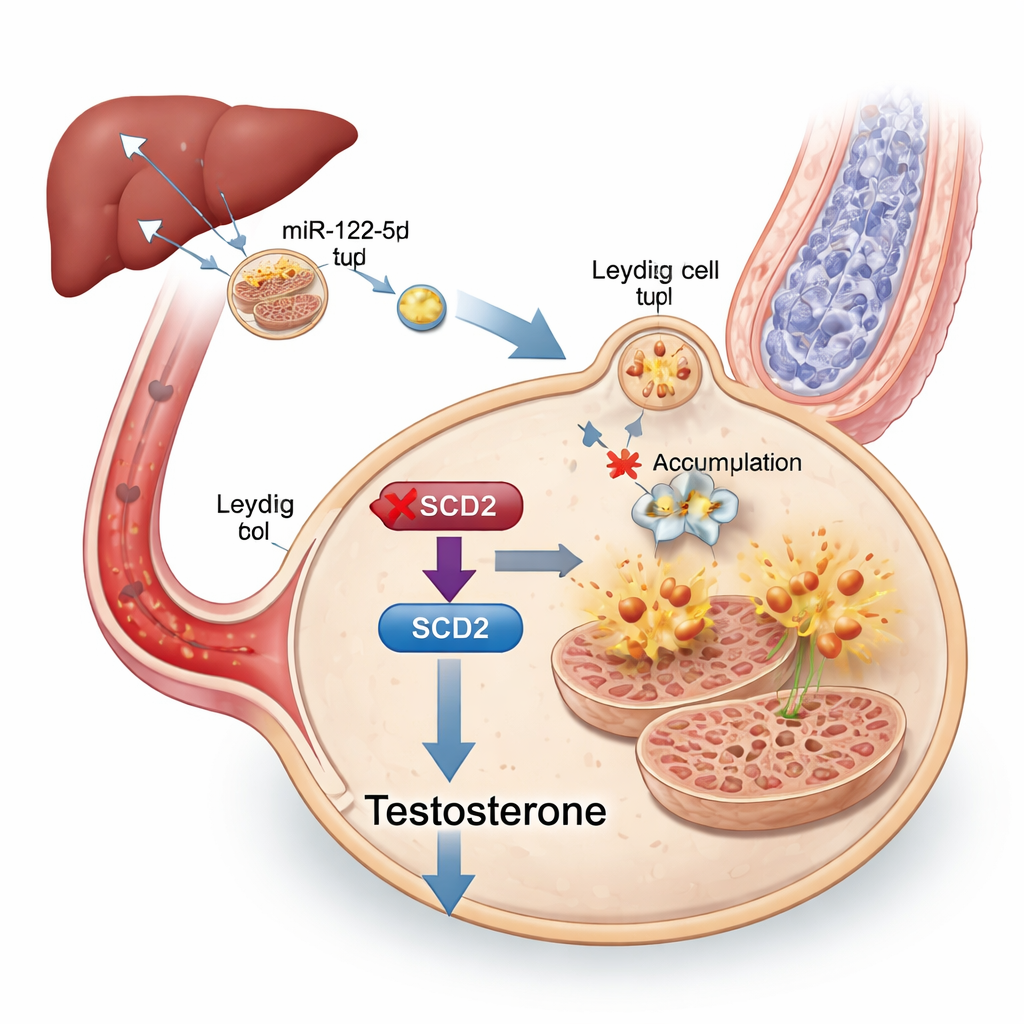
Ce que cela signifie pour la santé humaine
En termes clairs, ce travail montre qu’un régime riche en graisses peut amener le foie à charger les exosomes d’un excès de miR‑122‑5p. Ces exosomes voyagent dans le sang jusqu’aux testicules, où le microARN coupe l’interrupteur Scd2 de la gestion des lipides dans les cellules de Leydig. Sans Scd2, ces cellules accumulent des dommages oxydatifs liés au fer, subissent la ferroptose, produisent moins de testostérone et finissent par soutenir moins de spermatozoïdes sains. Bien que ces recherches aient été menées chez la souris et doivent encore être confirmées chez l’homme, elles identifient les exosomes d’origine hépatique, le miR‑122‑5p, la ferroptose et Scd2 comme des biomarqueurs prometteurs et des cibles médicamenteuses potentielles pour traiter l’infertilité masculine liée à l’obésité — et soulignent une raison de plus pour laquelle des régimes riches en graisses à long terme peuvent progressivement éroder la santé reproductive.
Citation: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Mots-clés: obésité et fertilité masculine, testostérone, exosomes, cellules de Leydig, ferroptose