Clear Sky Science · fr
Une étiquette protéique deux-en-un permet l’expression soluble et la purification dépendante du calcium des fragments d’anticorps en chaîne unique
Rendre la fabrication d’anticorps puissants plus simple
Les médicaments modernes reposent de plus en plus sur des fragments d’anticorps — de petites « armes guidées » précises capables de cibler des cellules cancéreuses, des tissus enflammés ou des molécules responsables de maladies. Pourtant, ces médicaments prometteurs sont étonnamment difficiles à produire : dans des usines bactériennes, ils ont tendance à s’agréger, à mal se replier et à résister aux méthodes de purification classiques. Cette étude décrit un nouvel appendice protéique, appelé étiquette CSQ, qui s’attaque simultanément à ces deux problèmes, rendant ces fragments plus faciles à produire et à purifier de façon simple et peu coûteuse.
Pourquoi les anticorps « réduits » comptent
Les anticorps complets ont transformé le traitement du cancer, des maladies auto-immunes et des affections oculaires, mais leur grande taille et leur structure complexe présentent des inconvénients. Ils peuvent être lents à éliminer de l’organisme, ne pas pénétrer efficacement les tumeurs ou les tissus, et sont coûteux à produire. Les fragments variables en chaîne unique, ou scFv, ne conservent que l’extrémité fonctionnelle d’un anticorps — la partie qui reconnaît la cible — reliée en une seule chaîne. Ces molécules compactes pénètrent plus facilement les tissus et peuvent être conçues pour des thérapies et des diagnostics sophistiqués. Cependant, lorsqu’ils sont fabriqués dans des bactéries communes comme Escherichia coli, de nombreux scFv s’accumulent en agrégats insolubles appelés corps d’inclusion, et il n’existe pas de méthode universelle et simple pour les purifier.
Une étiquette aide-deux-en-un
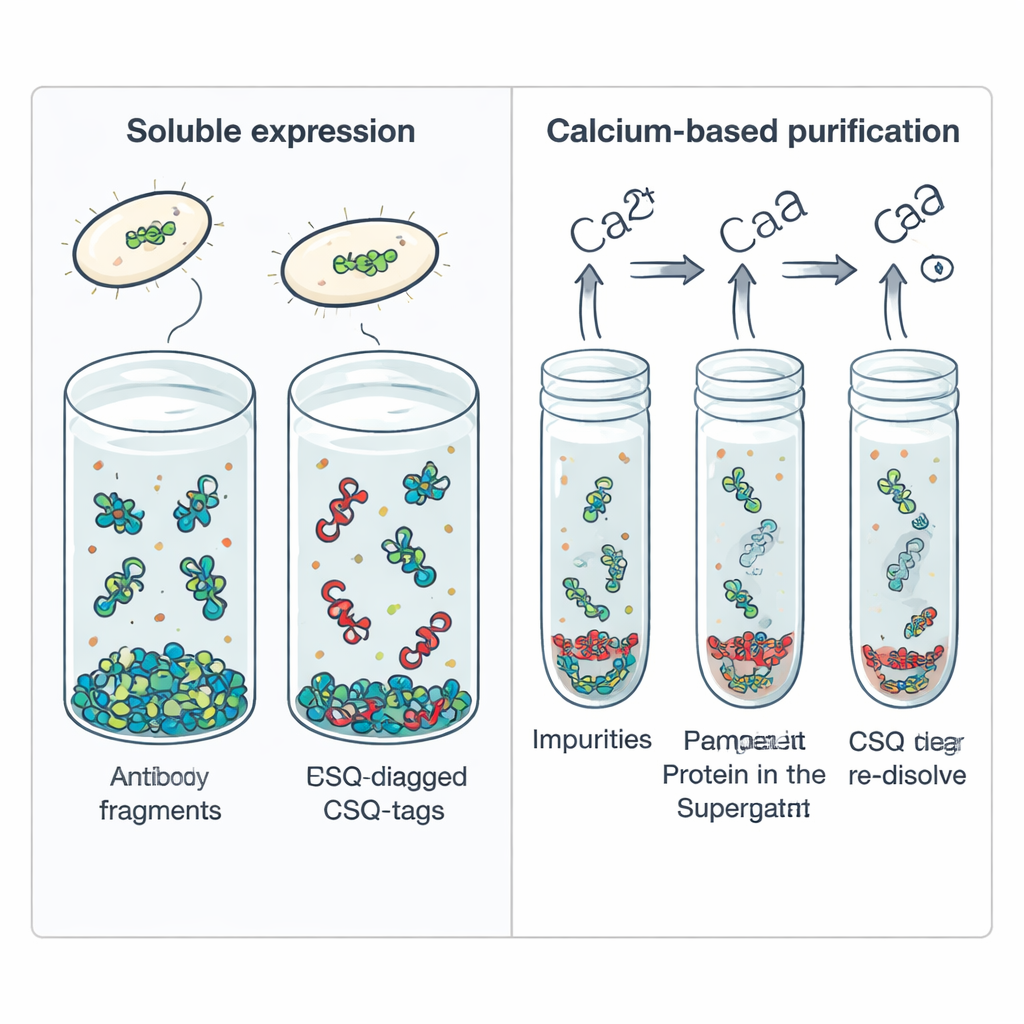
Les chercheurs se sont tournés vers la calséquestrine, une protéine naturelle de stockage du calcium présente dans les cellules musculaires, pour concevoir une étiquette auxiliaire qu’ils appellent CSQ-tag. Cette étiquette est inhabituellement acide et très flexible, avec de longues régions désordonnées qui agissent comme des « brosses entropiques » balayant l’espace autour de la protéine attachée. Fusionnée à quatre scFv thérapeutiques différents qui s’agrègent normalement, la CSQ-tag a considérablement augmenté la proportion restant soluble à l’intérieur de cellules E. coli standard. Alors que les mêmes scFv munis uniquement d’une simple étiquette His étaient presque entièrement insolubles, les versions porteurs de la CSQ-tag ont atteint une solubilité moyenne d’environ 84 % — même dans une souche bactérienne qui fournit habituellement un environnement chimiquement difficile pour un repliement correct.
Surclasser les technologies d’étiquetage établies
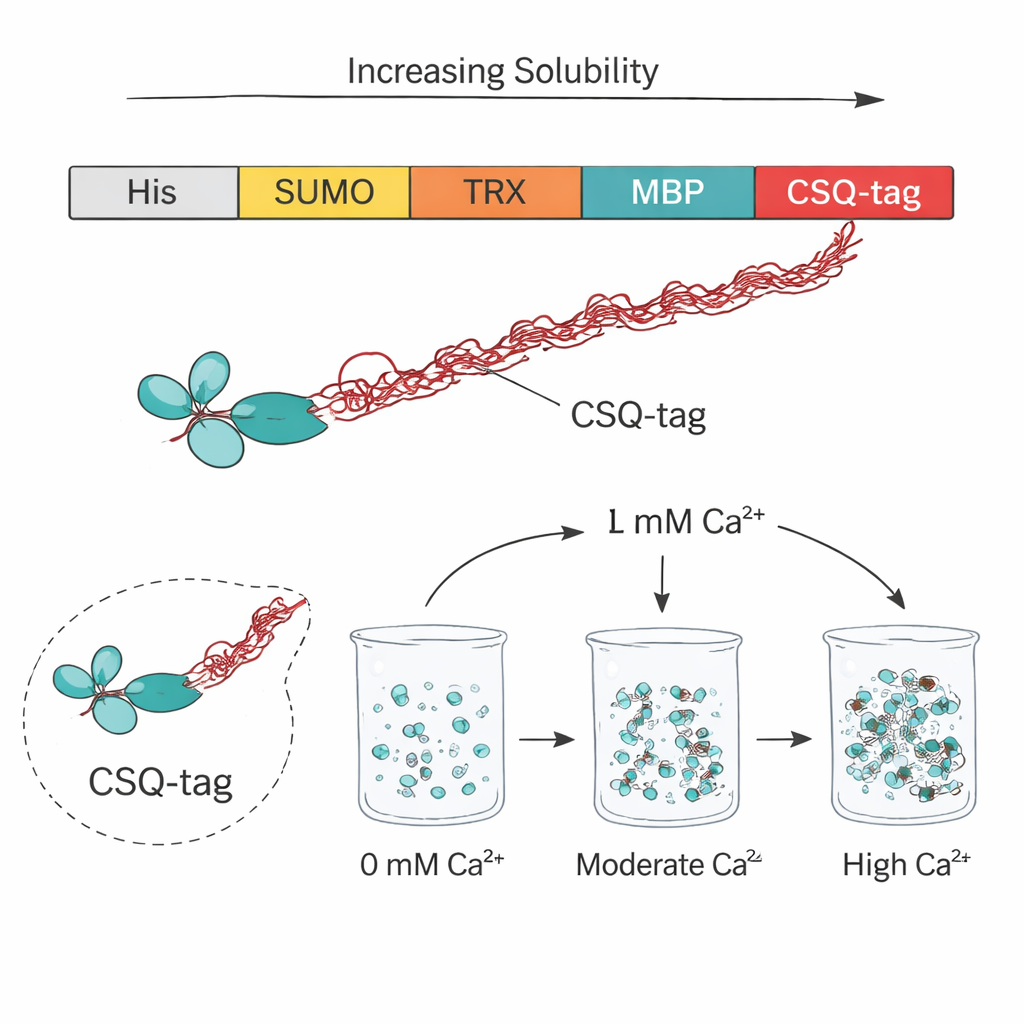
Pour évaluer la performance de la CSQ-tag par rapport aux étiquettes protéiques populaires, l’équipe l’a comparée à SUMO, thioredoxine, GST et MBP, largement utilisées pour encourager les protéines problématiques à rester en solution. Dans ce test direct avec un fragment scFv anti-VEGF (à la base du médicament oculaire brolucizumab), seuls MBP et CSQ ont notablement amélioré la solubilité, et CSQ s’est clairement démarquée. Sur quatre scFv différents, CSQ a augmenté la production soluble d’environ 1,8 fois de plus que MBP, longtemps considéré comme l’une des meilleures options. Des expériences complémentaires ont montré que la portion la plus acide et la plus désordonnée de la calséquestrine, connue sous le nom de domaine 3, était cruciale pour cet effet : son retrait réduisait fortement la solubilité, soulignant comment la charge négative et la souplesse structurale de l’étiquette empêchent les protéines associées de s’agglomérer.
Utiliser le calcium comme un interrupteur de purification simple
Outre son rôle pour la solubilité, la CSQ-tag offre un astuce de purification intégrée. La calséquestrine s’agrège naturellement lorsqu’elle lie le calcium puis se dissocie quand le calcium est retiré. Les auteurs ont exploité ce comportement en ajoutant du calcium à un extrait cellulaire contenant le scFv fusionné à la CSQ-tag, ce qui a provoqué l’agrégation des protéines fusionnées tandis que la plupart des contaminants bactériens restaient en solution. Une brève centrifugation a ramené la protéine CSQ-tagée ; l’ajout de l’agent chélateur d’ions calcium EDTA l’a ensuite redissoute avec une pureté élevée, supérieure à 95 %, sans résines chromatographiques coûteuses. Cette transition de phase pilotée par le calcium pouvait être répétée sans endommager la protéine, ce qui la rend attrayante pour la production à grande échelle.
Préserver la puissance du médicament
Pour tout produit thérapeutique, augmenter la production n’a d’intérêt que si le produit final conserve son activité. Après avoir utilisé une enzyme standard pour couper la CSQ-tag et une étape de polissage finale, l’équipe a testé le scFv anti-VEGF libéré. Il a lié sa cible avec une affinité essentiellement identique à celle du médicament approuvé brolucizumab, et des analyses chimiques détaillées ont confirmé la formation correcte des liaisons internes et l’absence d’agrégats nuisibles. Un second scFv, particulièrement difficile et ciblant le récepteur CD3, a montré une préservation d’activité similaire. Les rendements globaux obtenus avec le processus CSQ-tag étaient plusieurs fois supérieurs à ceux rapportés pour les méthodes classiques de refolding, tout en utilisant des équipements plus simples et des réactifs moins coûteux.
Ce que cela pourrait signifier pour les traitements futurs
En combinant une meilleure solubilité et une poignée de purification facile dans une seule étiquette, le système CSQ résout deux goulots d’étranglement de longue date dans la production de fragments d’anticorps. Il permet aux développeurs de médicaments d’utiliser des souches d’E. coli à croissance rapide et peu coûteuses tout en obtenant des scFv de haute qualité qui conservent leur pouvoir de liaison. Bien que des optimisations restent nécessaires, notamment pour réduire les pertes après le retrait de l’étiquette, cette étiquette modulable par le calcium pourrait rationaliser la fabrication non seulement des fragments d’anticorps mais aussi d’autres protéines thérapeutiques sensibles. Pour les patients, cela pourrait à terme se traduire par une gamme plus large de médicaments biologiques ciblés produits de manière plus efficace et à moindre coût.
Citation: Lee, J., Park, H., Jeong, S. et al. Two-in-one protein tag enables the soluble expression and calcium-dependent purification of single-chain antibody fragments. Commun Biol 9, 326 (2026). https://doi.org/10.1038/s42003-026-09611-0
Mots-clés: fragments d’anticorps en chaîne unique, expression protéique, étiquette calséquestrine, purification dépendante du calcium, anticorps thérapeutiques