Clear Sky Science · fr
La reconnaissance et la liaison des glycolipides par Siglec-6 reposent sur des interactions avec la membrane cellulaire
Comment nos cellules distinguent l’ami de l’ennemi
Le système immunitaire scrute en permanence nos propres cellules, décidant quand rester calme et quand attaquer. Une partie essentielle de cette surveillance consiste à reconnaître des structures sucrées à la surface des cellules. Cette étude révèle qu’un récepteur immunitaire humain, nommé Siglec-6, n’utilise pas seulement ces sucres mais aussi la membrane cellulaire environnante pour prendre des décisions de liaison particulièrement précises. Cette stratégie inhabituelle pourrait aider à expliquer comment notre organisme ajuste finement les signaux immunitaires et ouvrir de nouvelles voies pour des thérapies ciblées.
Un gardien sensible aux sucres sur les cellules immunitaires
Les Siglecs forment une famille de récepteurs présents sur les cellules immunitaires qui reconnaissent des sucres contenant de l’acide sialique, aidant le système immunitaire à distinguer le « soi » du « non‑soi ». La plupart des Siglecs s’appuient sur un seul élément très conservé — un résidu d’arginine — pour se fixer à ces sucres. Si cette arginine est supprimée, la liaison échoue généralement. Siglec‑6, toutefois, fait exception : des travaux antérieurs ont montré qu’il peut encore lier certains lipides portant des sucres même quand cette arginine clé est mutée. La nouvelle étude visait à comprendre comment Siglec‑6 parvient à enfreindre cette règle apparente et ce que cela signifie pour son rôle sur les mastocytes, les lymphocytes B mémoires et les cellules placentaires humaines.
Les lipides particuliers que cherche Siglec‑6
À la surface des cellules, les sucres pertinents peuvent être affichés sur des protéines comme sur des lipides. Ce travail se concentre sur un groupe de lipides sucrés appelés gangliosides, en particulier trois très proches nommés GM1, GM2 et GM3. Les trois présentent une « tête » terminée par un acide sialique qui émerge de la membrane. Des expériences antérieures ont montré que Siglec‑6 se lie fortement au GM1 lorsqu’il fait partie d’une membrane, mais quasiment pas au GM2 ou au GM3, bien que leurs têtes sucrées soient très similaires. En utilisant des simulations informatiques détaillées de membranes réalistes, les auteurs ont confirmé que l’acide sialique du GM1 et du GM3 est tout aussi exposé et accessible. Autrement dit, l’accès physique simple n’explique pas le statut particulier du GM1. À la place, un sucre additionnel à l’extrémité du GM1 — la galactose terminale — apparaît comme un élément critique qui aide à positionner correctement Siglec‑6 contre la membrane.
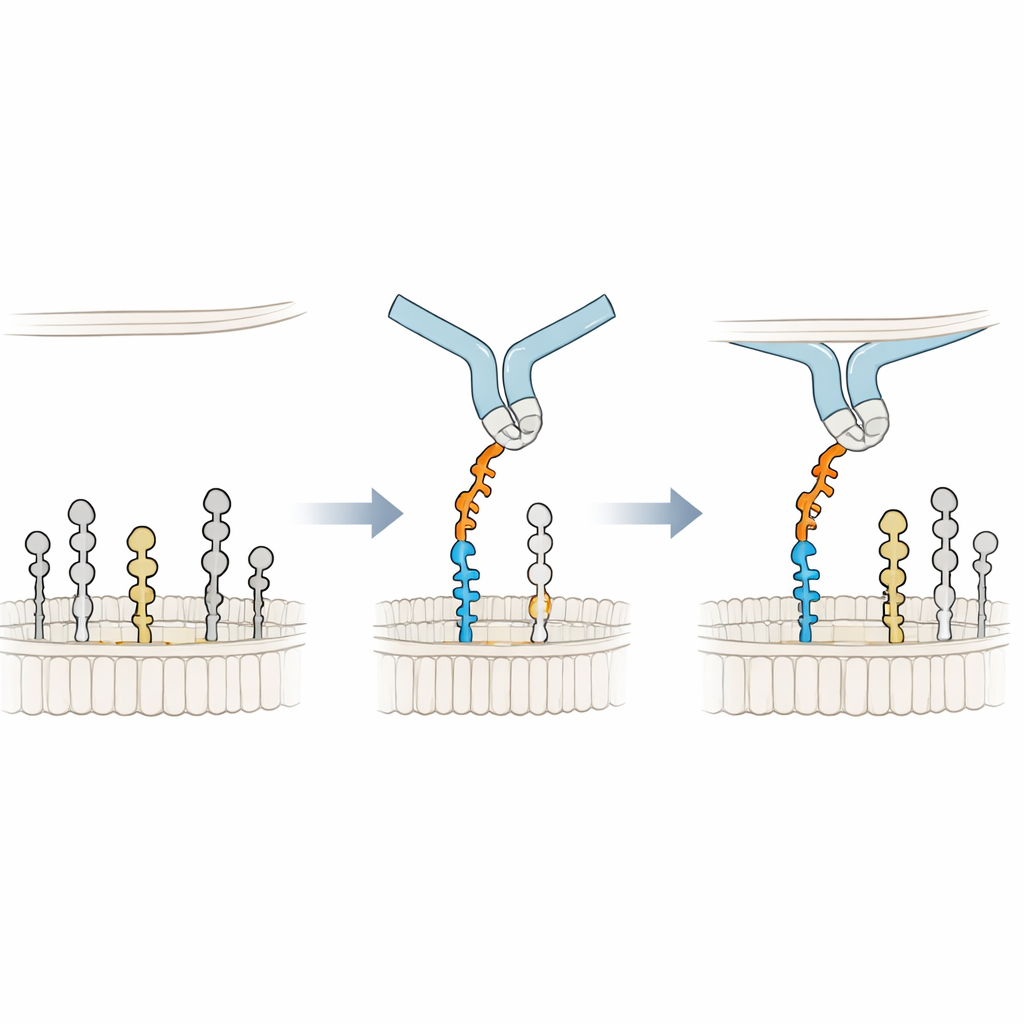
S’appuyer sur la membrane pour une meilleure prise
Pour comprendre le mécanisme de liaison à l’échelle atomique, les chercheurs ont construit des modèles 3D de Siglec‑6 en interaction avec le GM1 dans une membrane et ont réalisé de longues simulations de dynamique moléculaire. Ils ont constaté que Siglec‑6 utilise toujours son arginine canonique (Arg122) pour contacter l’acide sialique, mais que ce contact vacille au fil du temps. Ce qui stabilise le complexe est quelque chose de nouveau : un tryptophane voisin (Trp127) s’enfonce dans la partie grasse de la membrane, tandis qu’une lysine adjacente (Lys126) interagit avec les têtes chargées des lipides environnants. Cette « cale » dans la membrane complète l’interaction habituelle sucre–arginine, empruntant en quelque sorte de l’énergie de liaison à l’environnement lipidique. Lorsque la galactose terminale du GM1 est retirée pour imiter le GM2, une boucle flexible de Siglec‑6 se replie dans l’espace vacant, écarte le récepteur de la membrane et perturbe cette prise assistée par la membrane, expliquant la perte de liaison stable.
Des expériences qui vérifient le mécanisme
L’équipe a ensuite testé ces hypothèses issues des simulations dans des essais cellulaires et biochimiques. Ils ont modifié génétiquement des cellules pour exprimer Siglec‑6 normal ou muté et mesuré la capacité de liaison de ces cellules à des liposomes fluorescents et à de petits disques lipidiques portant du GM1. La mutation de l’arginine canonique réduisait seulement modestement la liaison lorsque le GM1 était en membrane, confirmant que Siglec‑6 ne dépend pas uniquement de ce résidu dans ce contexte. En revanche, la mutation de Trp127 abolissait presque complètement la liaison aux liposomes contenant du GM1, et la mutation conjointe de Trp127 et Lys126 supprimait presque entièrement la liaison. Les mêmes mutants, toutefois, se liaient normalement à des sucres de type GM1 présentés hors membrane, montrant que la structure de base de Siglec‑6 restait intacte. Des expériences de spectrométrie de masse native ont révélé en outre que Siglec‑6 peut se lier non seulement au GM1 mais aussi à des phospholipides ordinaires, et que cette interaction lipidique disparaît lorsque Trp127 est supprimé. Fait remarquable, Siglec‑6 adhère même à des liposomes « nus » dépourvus de GM1, là encore d’une manière dépendante de Trp127, suggérant qu’il peut d’abord explorer la membrane puis se verrouiller lorsqu’il rencontre du GM1.
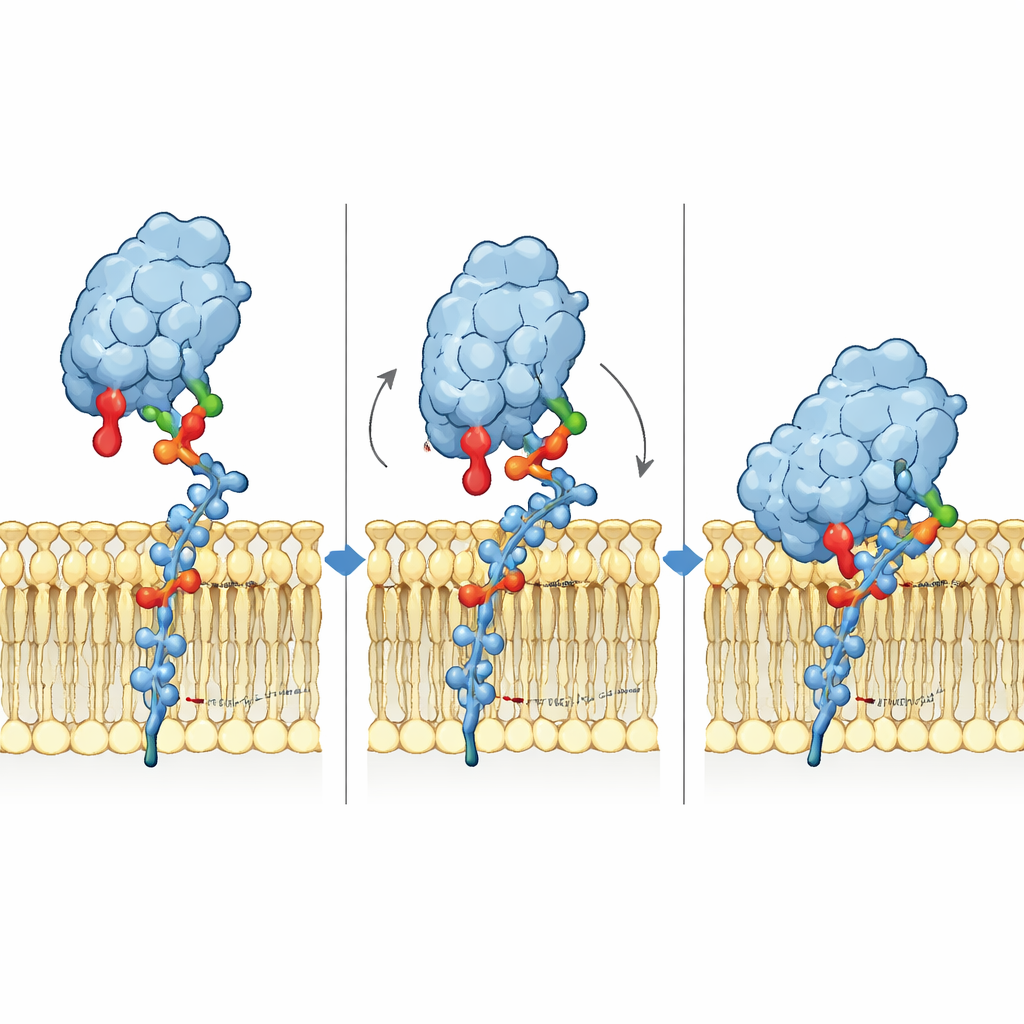
Les sucres libres racontent une autre histoire
Quand les mêmes trois gangliosides ont été testés comme fragments sucrés libres en solution plutôt que comme partie d’une membrane, Siglec‑6 s’est comporté davantage comme ses homologues. En solution, il liait GM1, GM2 et GM3 avec une affinité faible et similaire, et l’arginine canonique devenait essentielle : la mutation d’Arg122 réduisait fortement la liaison, tandis que la mutation de Trp127 avait peu d’effet. Ce contraste montre que Siglec‑6 change effectivement de mécanisme selon qu’il rencontre des sucres en membrane ou sous forme libre. Dans les membranes, il s’appuie sur un partenariat coopératif entre la tête sucrée, la galactose terminale du GM1 et le contact direct avec la membrane ; en solution, il revient au motif classique centré sur l’arginine pour la reconnaissance.
Pourquoi cela compte pour le contrôle immunitaire
Dans l’ensemble, l’étude révèle Siglec‑6 comme un capteur finement accordé qui utilise le contexte physique de la membrane pour affiner sa spécificité. En s’ancrant partiellement dans les lipides environnants, il peut reconnaître sélectivement le GM1 parmi des gangliosides très similaires, transformant de fait un « lecteur d’acide sialique » général en un détecteur de haute précision d’un motif de surface particulier. Cette stratégie assistée par la membrane semble unique parmi les Siglecs étudiés à ce jour et pourrait aider Siglec‑6 à scruter les surfaces cellulaires à la recherche de signatures glycolipidiques spécifiques qui régulent les réponses immunitaires ou marquent des tissus particuliers, comme le placenta humain. Comprendre ce double mode de reconnaissance pourrait faciliter la conception de thérapies et d’outils diagnostiques exploitant la combinaison inhabituelle de sensibilité aux sucres et à la membrane de Siglec‑6.
Citation: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Mots-clés: Siglec-6, gangliosides, membrane cellulaire, reconnaissance des glycolipides, régulation immunitaire