Clear Sky Science · fr
Analyse intégrée des GWAS et des molQTLs révèle des variants génétiques spécifiques aux cellules dans le système immunitaire porcin
Pourquoi l’immunité porcine nous concerne tous
Les porcs contribuent à nourrir une grande partie de la planète et servent aussi de modèles importants pour la recherche médicale humaine. Pour autant, les maladies infectieuses chez les porcs coûtent aux éleveurs des milliards de dollars chaque année et entraînent un usage intensif d’antibiotiques. Cette étude pose une question simple mais puissante : comment de petites différences d’ADN façonnent-elles le fonctionnement des cellules immunitaires porcines, et peut-on relier ces effets au comportement de types cellulaires individuels dans le sang ? Comprendre cette chaîne de cause à effet pourrait orienter des programmes de sélection pour des cheptels plus sains et fournir des indices sur notre propre système immunitaire.
Observation rapprochée de deux familles cellulaires sanguines clés
Les chercheurs se sont concentrés sur deux groupes majeurs de globules blancs qui patrouillent en permanence dans le sang porcin : les cellules mononucléées du sang périphérique, qui comprennent les lymphocytes et les monocytes impliqués dans des défenses plus lentes et ciblées, et les neutrophiles, qui assurent des attaques rapides et de première ligne contre les microbes. À partir de 134 porcelets Yorkshire, ils ont purifié chaque type cellulaire séparément et obtenu à la fois des données génomiques complètes et des instantanés détaillés de l’ARN, les molécules portant les instructions génétiques à l’intérieur des cellules. Cela leur a permis de voir non seulement quels gènes étaient activés, mais aussi comment la cellule coupait et terminait ces messages avant de les utiliser.
Relier les variants d’ADN aux commutateurs moléculaires
Plutôt que de se limiter à rechercher quels variants d’ADN s’associent au risque de maladie, l’équipe a cartographié comment les variants influencent trois types de caractéristiques moléculaires dans chaque type cellulaire. Certains variants modifiaient la quantité d’ARN produite par un gène. D’autres changeaient l’épissage de l’ARN, tronquant ou réarrangeant des segments. Une troisième classe affectait la manière dont l’ARN était terminé à son extrémité, un processus appelé polyadénylation qui peut influencer la stabilité du message. Ces paires variant–effet sont appelées loci de caractères quantitatifs moléculaires, ou molQTLs. Les cartes ont révélé des milliers de tels sites dans chaque type cellulaire et, de manière frappante, plus de quatre sur cinq étaient spécifiques soit aux cellules mononucléées mixtes, soit aux neutrophiles, soulignant à quel point le même génome peut être lu différemment selon les cellules immunitaires.
Trouver des réseaux qui relient les gènes aux traits immunitaires réels
Pour comprendre comment ces commutateurs moléculaires se rapportent à l’immunité de l’animal entier, les scientifiques ont combiné les cartes de molQTLs avec des tests sanguins standard et des mesures de protéines de signalisation immunitaire. Ils ont construit des réseaux de co‑expression—groupes de gènes qui tendent à augmenter ou diminuer ensemble—et ont examiné lesquels suivaient des traits tels que la proportion de neutrophiles ou de lymphocytes, le nombre de globules blancs, ou les niveaux d’interférons et du facteur de nécrose tumorale. Les modules associés aux traits des lymphocytes étaient enrichis en voies de l’immunité adaptative, tandis que ceux liés aux neutrophiles mettaient en évidence des défenses innées rapides et la signalisation inflammatoire. De nombreux gènes clés dans ces modules étaient directement régulés par des molQTLs spécifiques au type cellulaire, suggérant des trajectoires claires du variant d’ADN à la modification de la composition ou de la fonction cellulaire.
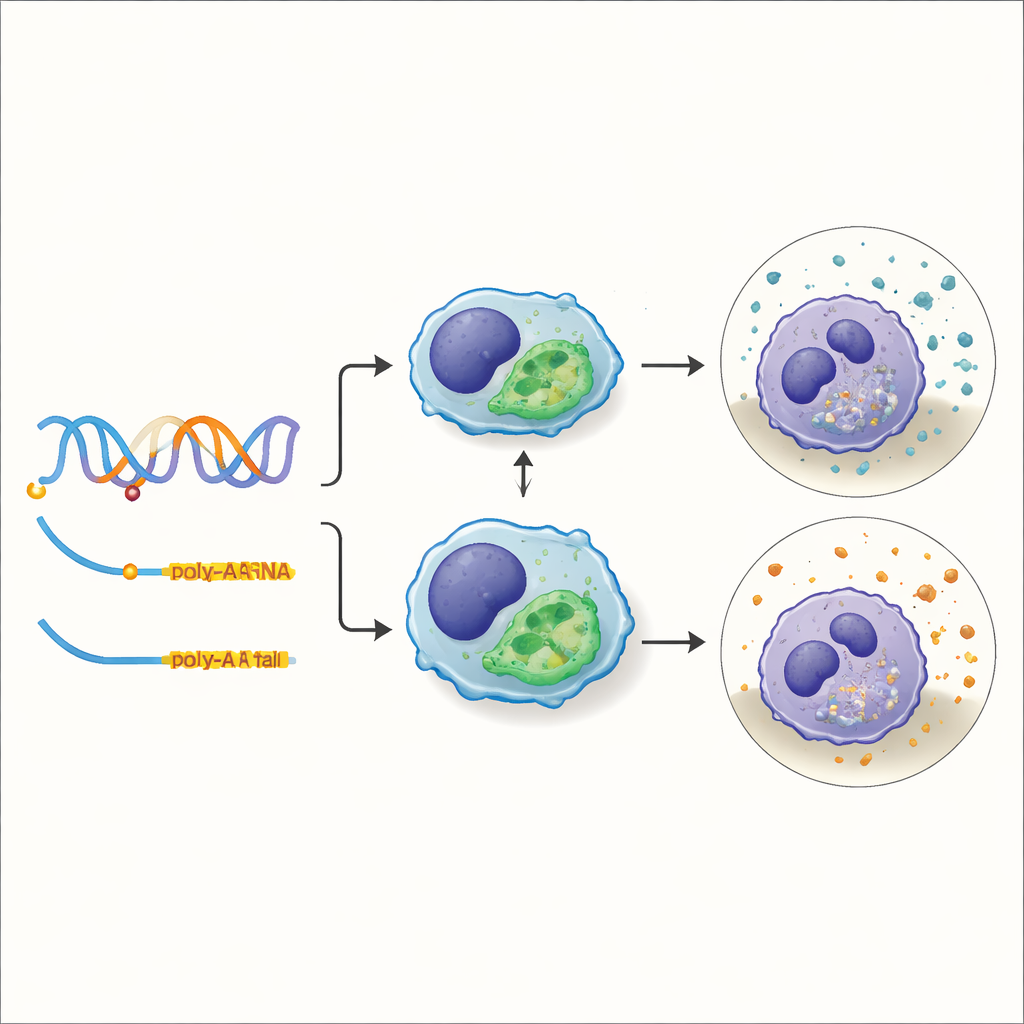
Approche détaillée d’un variant qui module la capacité de « nettoyage » cellulaire
Un des traits les plus concrets examinés par l’équipe était la capacité phagocytaire—la faculté des cellules immunitaires d’englober et d’éliminer débris ou agents pathogènes. En superposant leurs molQTLs aux résultats d’études d’association pangénomique antérieures sur la phagocytose, ils ont identifié 588 régions où le même changement d’ADN est probablement responsable à la fois d’un changement moléculaire et d’une variation de la performance de nettoyage cellulaire. Un exemple marquant était un variant situé dans un gène appelé TXNDC15. Ce changement n’a pas simplement activé ou désactivé le gène ; il a modifié le choix du site de polyadénylation pour l’ARN de ce gène. Les porcs portant une version du variant privilégiaient une queue d’ARN plus courte, qui s’est avérée plus stable et s’accumulait à des niveaux plus élevés, et ces animaux présentaient une activité phagocytaire plus forte dans leurs cellules immunitaires.
Ce que cela signifie pour des porcs plus sains et au‑delà
Concrètement, ce travail montre comment de petites différences d’ADN peuvent reprogrammer les « instructions » à l’intérieur de types cellulaires immunitaires spécifiques et, par ce biais, influencer combien de ces cellules existent et à quel point elles accomplissent leurs fonctions. En séparant soigneusement les types cellulaires et en suivant non seulement l’activité génique mais aussi la façon dont les messages sont découpés et terminés, l’étude révèle des points de contrôle cachés que les analyses sur tissus mixtes ne détectent pas. La carte génétique résultante fournit une base pour sélectionner des porcs naturellement plus résistants aux maladies, réduisant potentiellement le recours aux antibiotiques. Parallèlement, parce que l’immunité porcine ressemble étroitement à celle de l’humain, ces découvertes peuvent aussi aider les scientifiques à comprendre comment des mécanismes similaires opèrent en santé et en maladie humaines.
Citation: Yang, J., Chen, S., Tang, Y. et al. Integrated analysis of GWAS and molQTLs reveals cell-specific genetic variants in the porcine immune system. Commun Biol 9, 408 (2026). https://doi.org/10.1038/s42003-026-09605-y
Mots-clés: immunité porcine, variants génétiques, cellules immunitaires, phagocytose, QTLs moléculaires