Clear Sky Science · fr
L’inhibition d’ATM améliore l’efficacité des knock-ins en supprimant l’activation des voies apoptotiques induite par l’AAV
Améliorer l’efficacité de l’édition génique
L’édition génique par CRISPR promet des traitements pour les maladies génétiques, des cultures plus résistantes et des outils puissants pour la recherche. Mais l’une de ses capacités les plus précieuses — l’insertion précise d’un nouvel ADN en un endroit choisi du génome, appelée « knock-in » — reste peu efficace. Cette étude explore pourquoi certaines cellules acceptent l’ADN exogène plus facilement que d’autres et révèle une méthode pour inciter les cellules à réaliser des modifications précises plus souvent, en particulier lorsqu’on utilise le virus adéno-associé (AAV), un vecteur de premier plan pour la thérapie génique.
Observer la réparation de l’ADN en temps réel
Pour comprendre ce qui favorise ou entrave l’insertion précise de gènes, les chercheurs ont construit un « tableau de bord » sophistiqué à l’intérieur de cellules souches embryonnaires de souris. Ce système à triple rapporteur utilise trois marqueurs fluorescents pour suivre, dans les mêmes cellules, si CRISPR a coupé l’ADN, si un knock-in précis a eu lieu, ou si la cellule a plutôt inséré l’ADN donneur par une méthode de réparation plus grossière. En lisant les différentes combinaisons de couleurs par cytométrie en flux, ils ont pu séparer les éditions propres fondées sur un modèle des insertions sujettes à erreurs et des cellules non éditées. Ce suivi côte à côte leur a permis de cartographier la contribution des différentes voies de réparation de l’ADN à chaque issue avec beaucoup plus de résolution que les tests PCR classiques.
Deux donneurs d’ADN, deux réponses très différentes
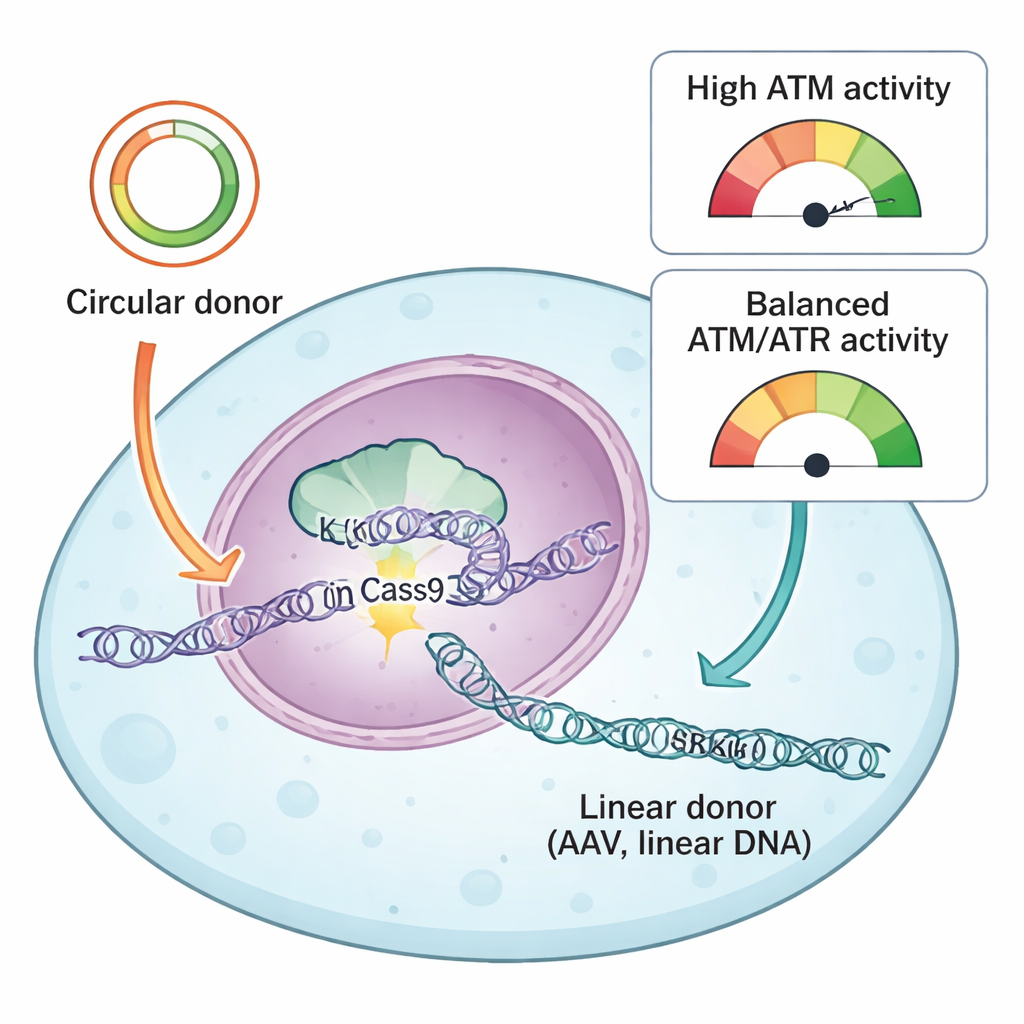
L’équipe a comparé deux types courants d’ADN donneur utilisés pour guider les réparations CRISPR : des plasmides circulaires et de l’ADN linéaire dérivé d’AAV. Les deux portent des « bras d’homologie » assortis qui indiquent à la cellule où insérer la nouvelle séquence, mais ils pénètrent dans la cellule sous des formes physiques différentes. Les plasmides circulaires sont des boucles fermées d’ADN double brin, tandis que les donneurs AAV arrivent typiquement sous forme de molécules linéaires simples. En utilisant leur système rapporteur et une bibliothèque de molécules ciblant des protéines de la réponse aux dommages de l’ADN, les auteurs ont constaté qu’une protéine clé, ATR, était uniformément essentielle pour des knock-ins réussis avec les deux types de donneurs. L’inhibition d’ATR réduisait fortement l’insertion précise, tandis qu’une stimulation modérée d’ATR via la voie KEAP1–NRF2 rendait les knock-ins plus efficaces, en particulier avec des donneurs AAV.
Quand la protection de l’ADN se retourne contre la cellule
Un autre capteur des dommages de l’ADN, ATM, s’est avéré avoir un comportement étonnamment dépendant du type de donneur. Avec des plasmides circulaires, le blocage d’ATM réduisait à la fois le knock-in précis et les insertions médiées par le liguage des extrémités, correspondant à son rôle classique d’aide à la réparation des cassures double brin. Mais avec de l’ADN linéaire — qu’il provienne d’AAV, d’AAV auto-complémentaire ou de plasmides découpés en fragments droits — l’inhibition d’ATM avait l’effet inverse : elle augmentait l’efficacité du knock-in. Les chercheurs ont relié cet effet à la façon dont les cellules interprètent des afflux d’ADN linéaire. De fortes doses d’AAV activaient fortement ATM, qui activait à son tour p53 et la caspase 3, des acteurs centraux de la mort cellulaire programmée. Les cellules ayant capté de nombreuses copies de l’ADN donneur, et donc celles ayant la plus grande probabilité d’un knock-in réussi, étaient aussi les plus susceptibles d’être éliminées par ce système d’alerte.
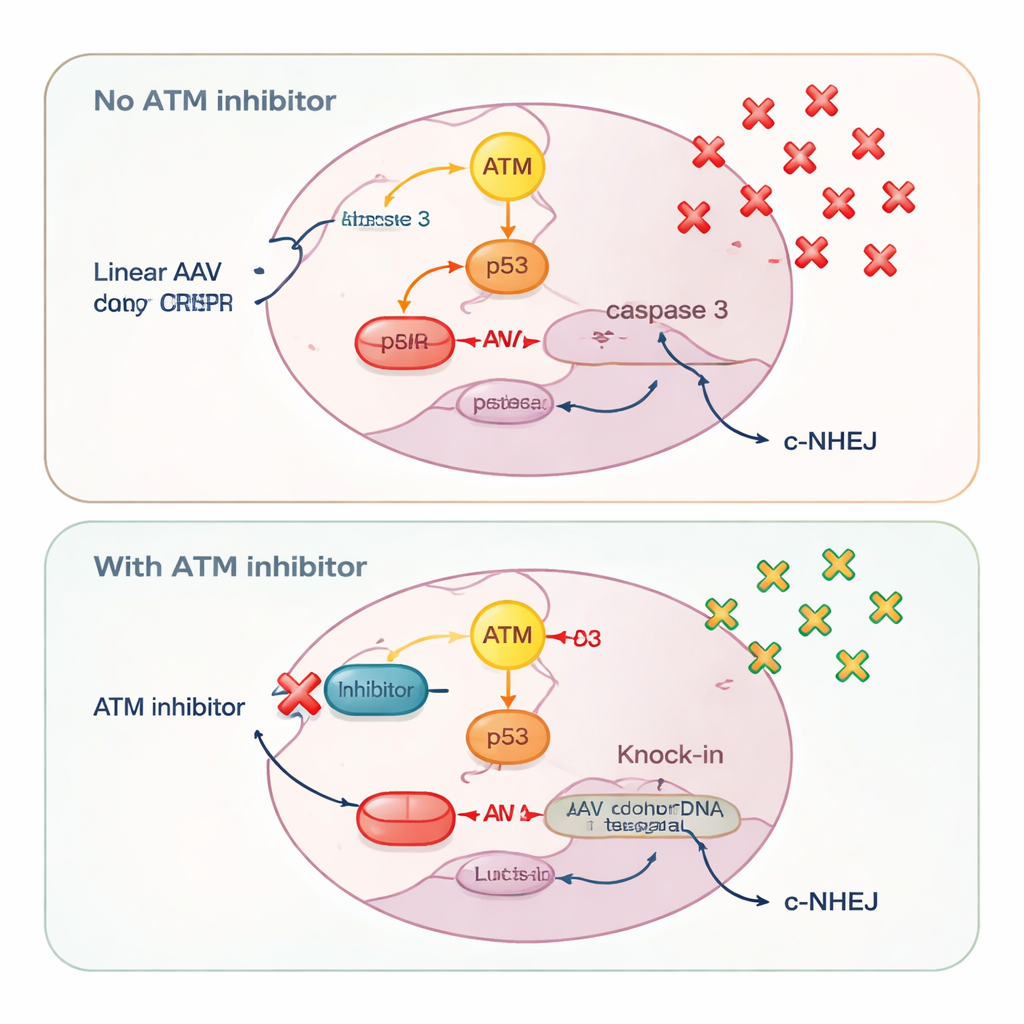
Sauver les cellules les mieux équipées
En ajoutant des inhibiteurs d’ATM, les scientifiques ont calmé la voie mortelle ATM–p53–caspase 3. Cela a épargné les cellules contenant de fortes quantités d’ADN donneur, permettant à davantage d’entre elles de survivre assez longtemps pour réaliser un knock-in précis. Des mesures du nombre de génomes viraux ont confirmé que l’inhibition d’ATM augmentait le nombre de molécules AAV conservées dans les cellules. Parallèlement, le blocage d’ATM atténuait légèrement une voie de réparation rapide et brutale appelée jonction non homologue classique, comme l’illustre la réduction de l’activation de DNA‑PK, une enzyme centrale de cette voie. L’affaiblissement de cette option de réparation concurrente a orienté davantage de coupures CRISPR vers le knock-in fondé sur l’homologie plutôt que vers des rustines rapides qui ignorent le modèle donneur.
Ce que cela signifie pour les thérapies géniques à venir
Pour les non-spécialistes, le message est que les mêmes mécanismes cellulaires qui nous protègent des dommages à l’ADN peuvent involontairement saboter l’édition génique précise, en particulier lorsque de grandes quantités d’ADN donneur viral sont utilisées. Ce travail montre qu’ajuster finement ces garde-fous — maintenir ATR actif tout en restreignant temporairement ATM lorsque des donneurs linéaires comme l’AAV sont présents — peut rendre les knock-ins CRISPR plus fiables et plus efficaces. Une telle stratégie pourrait améliorer les thérapies géniques, l’ingénierie cellulaire et les modèles de maladie en aidant davantage de cellules à accepter la modification prévue tout en évitant des pertes cellulaires inutiles.
Citation: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Mots-clés: Knock-in CRISPR, Édition génique AAV, Réponse aux dommages de l’ADN, Inhibition d’ATM, Ingénierie du génome