Clear Sky Science · fr
STING contrôle la glycolyse et la lactylation des histones pour piloter le reprogrammation métabolique des macrophages dans l’iléus postopératoire
Quand la chirurgie met l’intestin en pause
Après une intervention abdominale, de nombreux patients constatent que leurs intestins refusent tout simplement de reprendre leur activité. Ce ralentissement, appelé iléus postopératoire, peut signifier des jours de nausées, de ballonnements et un rétablissement retardé. L’étude résumée ici pose une question apparemment simple : pourquoi certaines cellules immunitaires de l’intestin maintiennent-elles l’arrêt du transit, et diminuer un seul interrupteur moléculaire pourrait-il aider l’intestin à se remettre en mouvement ?
Comment une opération de routine déclenche l’inflammation intestinale
La chirurgie abdominale perturbe inévitablement les intestins. Chez la souris, une manipulation douce de l’intestin suffit à provoquer un gonflement, une accumulation de liquide et un blocage du contenu de l’intestin grêle. Lorsqu’ils ont suivi la distance parcourue par un colorant fluorescent sans danger à travers le tube digestif, les chercheurs ont constaté que la chirurgie ralentissait fortement sa progression, signe d’une motricité altérée. L’examen microscopique de la paroi intestinale a montré que la couche musculaire — le tissu qui se contracte pour propulser les aliments — devenait enflammée et envahie par des cellules immunitaires entrant en grand nombre, en particulier des macrophages et des neutrophiles. Ces observations suggèrent que l’enveloppe musculaire de l’intestin devient un champ de bataille inflammatoire après la chirurgie, et que cette inflammation locale est étroitement liée à la paralysie du transit.
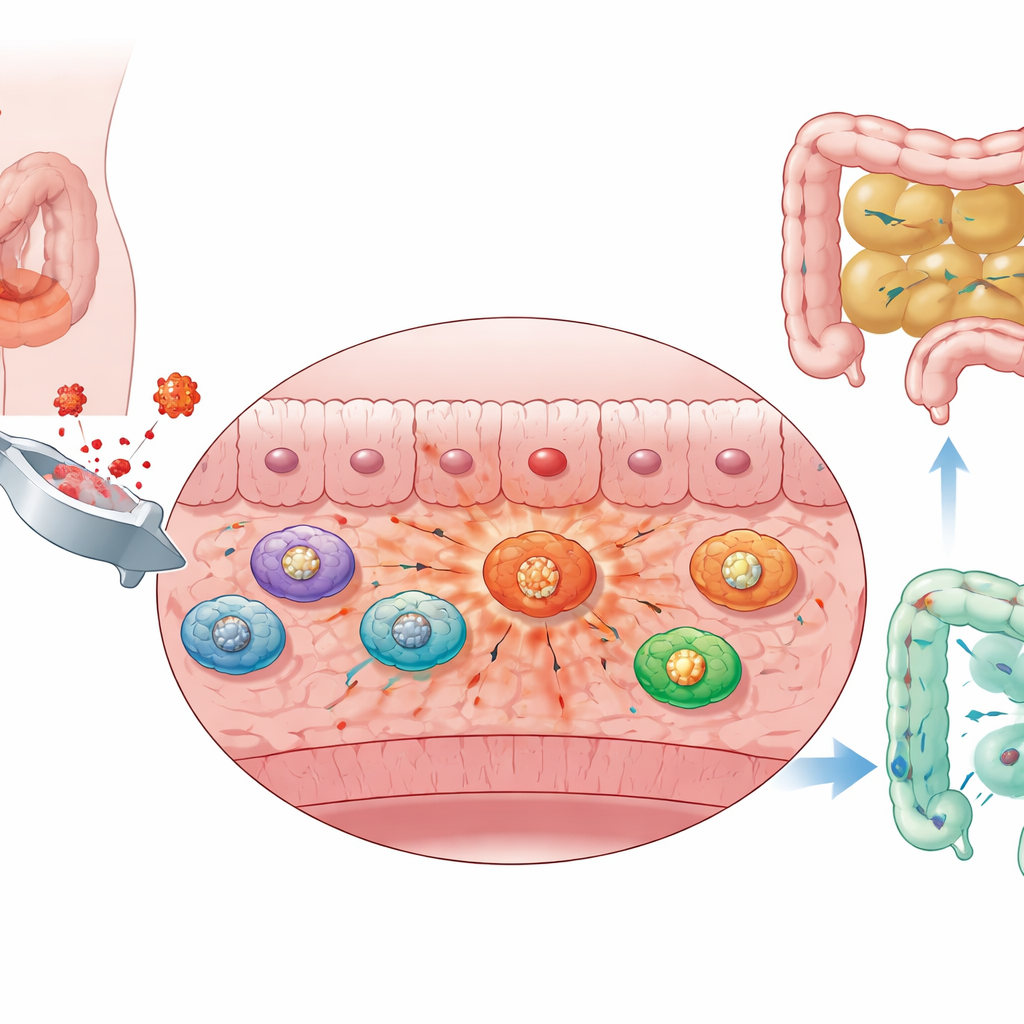
Les macrophages changent de carburant et attisent l’inflammation
Pour comprendre ce que faisaient ces macrophages infiltrants, l’équipe a exploité des données d’ARN à grande échelle et de séquençage unicellulaire provenant de la couche musculaire intestinale. Ils ont découvert que les macrophages chez les animaux opérés augmentaient fortement une voie rapide de consommation du glucose connue sous le nom de glycolyse. Comparés aux autres cellules immunitaires du même tissu, les macrophages infiltrants présentaient les scores de glycolyse les plus élevés et exprimaient des niveaux accrus des principales enzymes glycolytiques. Un sous-ensemble distinct de ces cellules dépendait fortement de la glycolyse, portait de forts signaux inflammatoires et répondait vigoureusement à des composants bactériens tels que le lipopolysaccharide. En substance, les macrophages étaient passés à un mode « haute consommation de sucre, haute inflammation » qui semble aggraver l’inflammation de la couche musculaire et maintenir l’intestin immobile.
Un interrupteur moléculaire qui couple la détection du danger à la combustion du sucre
Les chercheurs se sont ensuite concentrés sur STING, une protéine surtout connue comme système d’alarme pour l’ADN étranger mais de plus en plus reconnue comme régulateur métabolique. Dans la paroi musculaire intestinale enflammée, le sous-ensemble de macrophages hautement glycolytique présentait des niveaux de STING nettement plus élevés, un schéma confirmé par des marquages tissulaires. En culture cellulaire, l’exposition des macrophages au lipopolysaccharide bactérien augmentait à la fois l’activité de STING et l’expression des enzymes glycolytiques qui convertissent le glucose en énergie et en lactate. Lorsque les scientifiques ont supprimé le gène STING, cette poussée de consommation de sucre s’est effondrée : les intermédiaires glycolytiques ont diminué, l’acidification du milieu de culture a régressé et la production d’espèces réactives de l’oxygène a été réduite. Ces cellules déficientes en STING produisaient également moins de lactate, ce qui implique que la voie d’alarme et le moteur métabolique sont étroitement couplés.
Du déchet sucré à la mémoire épigénétique
Le lactate est souvent considéré comme un déchet métabolique, mais ici il joue un rôle plus subtil. L’équipe a montré que chez les macrophages normaux, le flux de lactate sert à modifier chimiquement les histones — les protéines qui emballent l’ADN — via un processus appelé lactylation. Cette modification était particulièrement marquée au site H4K8 sur des histones proches du gène codant HK2, une enzyme clé de la glycolyse. Dans les cellules déficientes en STING, la lactylation des histones et l’accessibilité de la chromatine au niveau du promoteur de HK2 étaient toutes deux réduites, et des méthodes de séquençage spécialisées ont confirmé que ces changements limitaient l’activation de HK2. Parallèlement, un facteur de transcription en aval, IRF3, se liait directement au promoteur de HK2 plus facilement lorsque cette marque de lactylation était présente. Ensemble, ces étapes créent une boucle autorenforçante : STING stabilise des facteurs qui stimulent la glycolyse, la glycolyse produit du lactate, le lactate modifie les histones pour ouvrir le gène HK2, et IRF3 augmente l’expression de HK2, alimentant encore la glycolyse et l’inflammation.
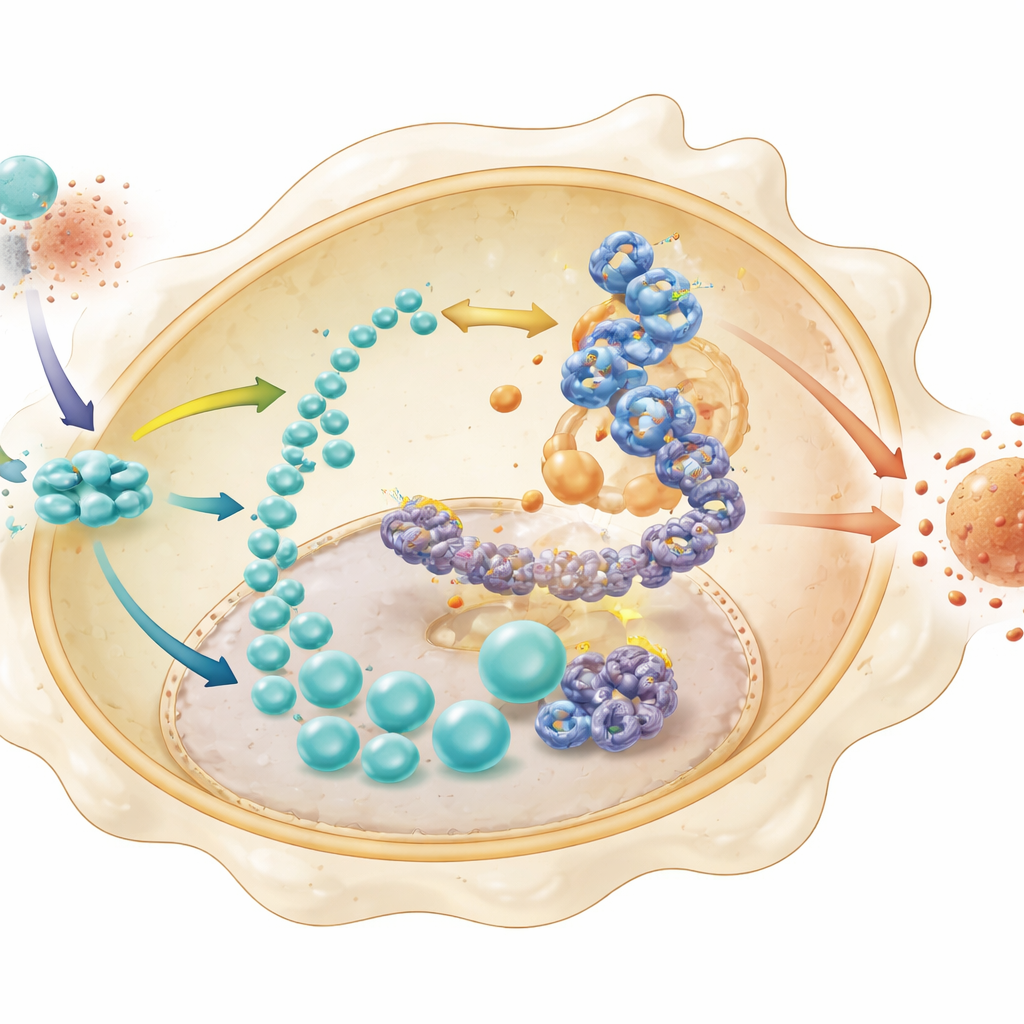
Rompre la boucle pour permettre la récupération intestinale
Enfin, l’équipe a testé si rompre cette boucle pouvait réellement aider les animaux à se remettre de l’iléus postopératoire. Chez les souris dépourvues de STING, le tissu musculaire intestinal exprimait moins d’enzymes glycolytiques, contenait moins de macrophages inflammatoires et présentait un basculement d’un état macrophagique agressif et pro-inflammatoire vers un profil plus résolutif. L’infiltration de neutrophiles était moindre et le transit intestinal s’améliorait. Le blocage pharmacologique de STING chez des souris normales produisait des bénéfices similaires, tandis que la réactivation de l’enzyme HK2 chez des animaux déficients en STING rétablissait partiellement l’inflammation et les troubles de la motricité. Pour un lecteur non spécialiste, le message est clair : un seul interrupteur de détection du danger dans les macrophages intestinaux peut reconfigurer leur métabolisme d’une manière qui verrouille l’intestin dans une pause prolongée après une chirurgie. Cibler STING — ou la boucle de rétroaction qui lie combustion du sucre et marquage lactylé des histones — offre une voie prometteuse pour accélérer la récupération et atténuer l’une des complications les plus tenaces des interventions abdominales.
Citation: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Mots-clés: iléus postopératoire, métabolisme des macrophages, voie STING, glycolyse, inflammation intestinale