Clear Sky Science · fr
Caractérisation de la développabilité des nanocorps pour améliorer la conception thérapeutique à l’aide du Therapeutic Nanobody Profiler
Pourquoi les petits cousins des anticorps comptent pour les médicaments de demain
Beaucoup des médicaments phares d’aujourd’hui sont des anticorps — des protéines qui s’attachent aux cibles de maladie avec une grande précision. Une nouvelle classe de liaisons encore plus petites, appelées nanocorps, peut se faufiler dans des poches difficiles d’accès sur des virus, des tumeurs et d’autres molécules. Mais la capacité à se lier à une cible ne suffit pas : un candidat médicament doit aussi être facile à produire, stable en flacon et sûr dans l’organisme. Cet article présente le Therapeutic Nanobody Profiler, un outil computationnel conçu pour aider les scientifiques à juger, tôt et à partir de la seule séquence, quels nanocorps sont les plus susceptibles de devenir des médicaments pratiques.
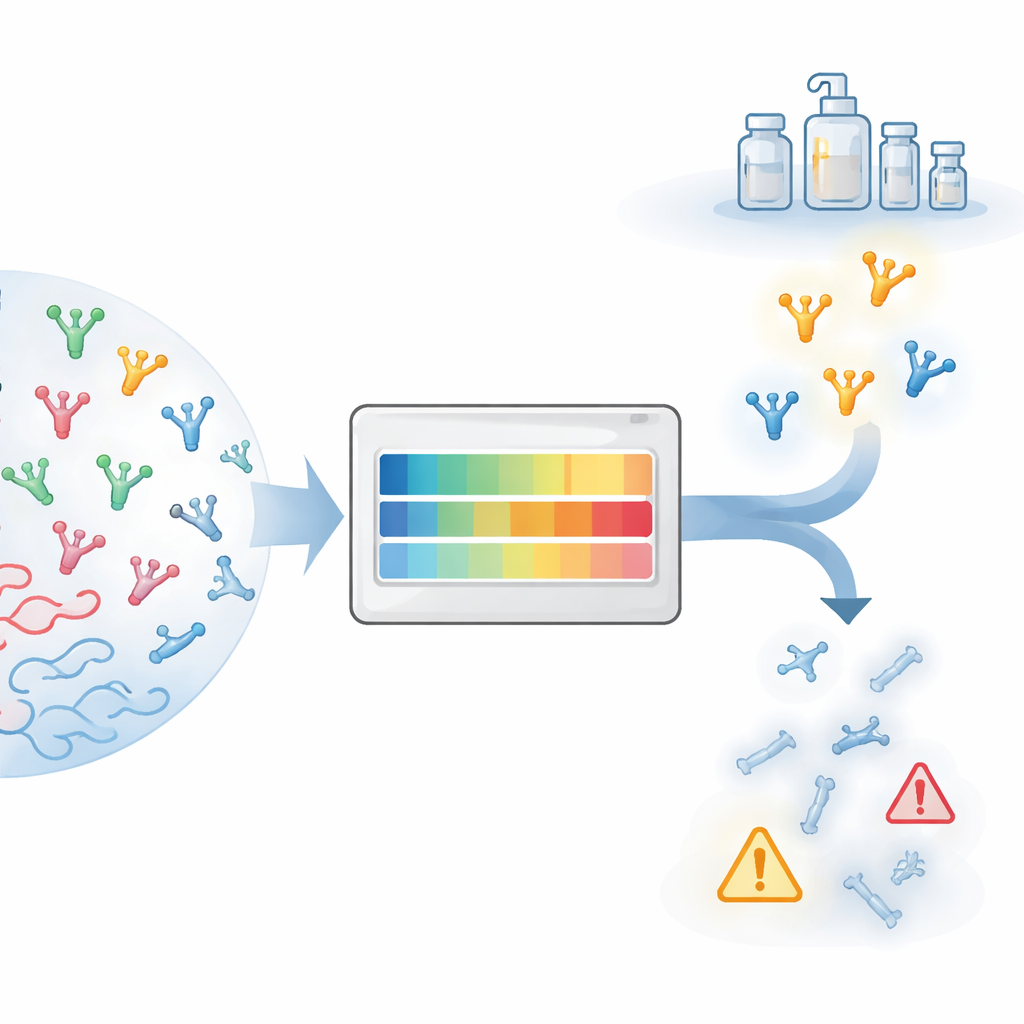
De l’idée prometteuse au médicament pratique
Transformer une protéine en thérapie réelle implique toute une série d’obstacles pratiques regroupés sous le terme « développabilité ». Les protéines doivent être produites en grande quantité, rester solubles, éviter de s’agréger et conserver leur stabilité pendant le transport et le stockage. Au cours de la dernière décennie, les chercheurs ont appris à prédire beaucoup de ces traits pour les anticorps monoclonaux de taille normale, soutenus par des données cliniques abondantes et des tests en laboratoire spécialisés. Les nanocorps, en revanche, sont structurellement différents : ils consistent en un seul domaine plutôt qu’en une paire de chaînes, ont souvent des boucles de liaison plus longues et exposent des régions de surface qui sont enfouies dans les anticorps conventionnels. En conséquence, des méthodes adaptées aux anticorps classiques peuvent donner des résultats trompeurs lorsqu’elles sont appliquées aux nanocorps.
Un profileur conçu pour les particularités des nanocorps
Pour résoudre ce décalage, les auteurs ont conçu le Therapeutic Nanobody Profiler (TNP), inspiré d’un outil antérieur pour anticorps standards mais ré‑ingénieré autour de la biologie des nanocorps. Ils ont compilé des séquences de nanocorps provenant de nombreuses sources : essais cliniques, répertoires immunitaires naturels, brevets, articles scientifiques et structures cristallographiques connues. En utilisant des prédicteurs de structure par apprentissage profond adaptés aux anticorps monodomaines, ils ont généré des modèles 3D pour ces séquences. À partir de chaque modèle, ils ont mesuré la longueur des boucles de liaison, la distance que parcourt une boucle clé par rapport au corps de la protéine, et la façon dont des amas de résidus hydrophobes et chargés sont arrangés à la surface — des caractéristiques qui influencent fortement la solubilité, l’agrégation et l’adhérence non spécifique.
Deux styles structuraux, tous deux viables
Une des observations les plus marquantes concerne la boucle de liaison principale, connue sous le nom de CDR3. Lorsque l’équipe a quantifié le caractère « compact » de cette boucle — en comparant sa longueur à l’étendue de son saillie depuis la protéine — elle a trouvé une nette division en deux styles structuraux. Dans un sous‑type, la boucle est plus longue et se replie sur le côté de la protéine, formant de nombreux contacts stabilisateurs avec un ensemble de résidus caractéristiques. Dans l’autre, la boucle ressort davantage, comme dans un fragment d’anticorps conventionnel. Les nanocorps en phase clinique occupent les deux sous‑types, et lorsque les chercheurs ont comparé des dizaines de mesures de laboratoire pratiques — telles que l’agrégation, l’auto‑association et la stabilité thermique — ils n’ont observé aucune pénalité systématique pour l’un ou l’autre style. Cela signifie que les concepteurs de médicaments n’ont pas besoin de privilégier une forme globale de boucle plutôt qu’une autre, tant que les autres propriétés sont acceptables.
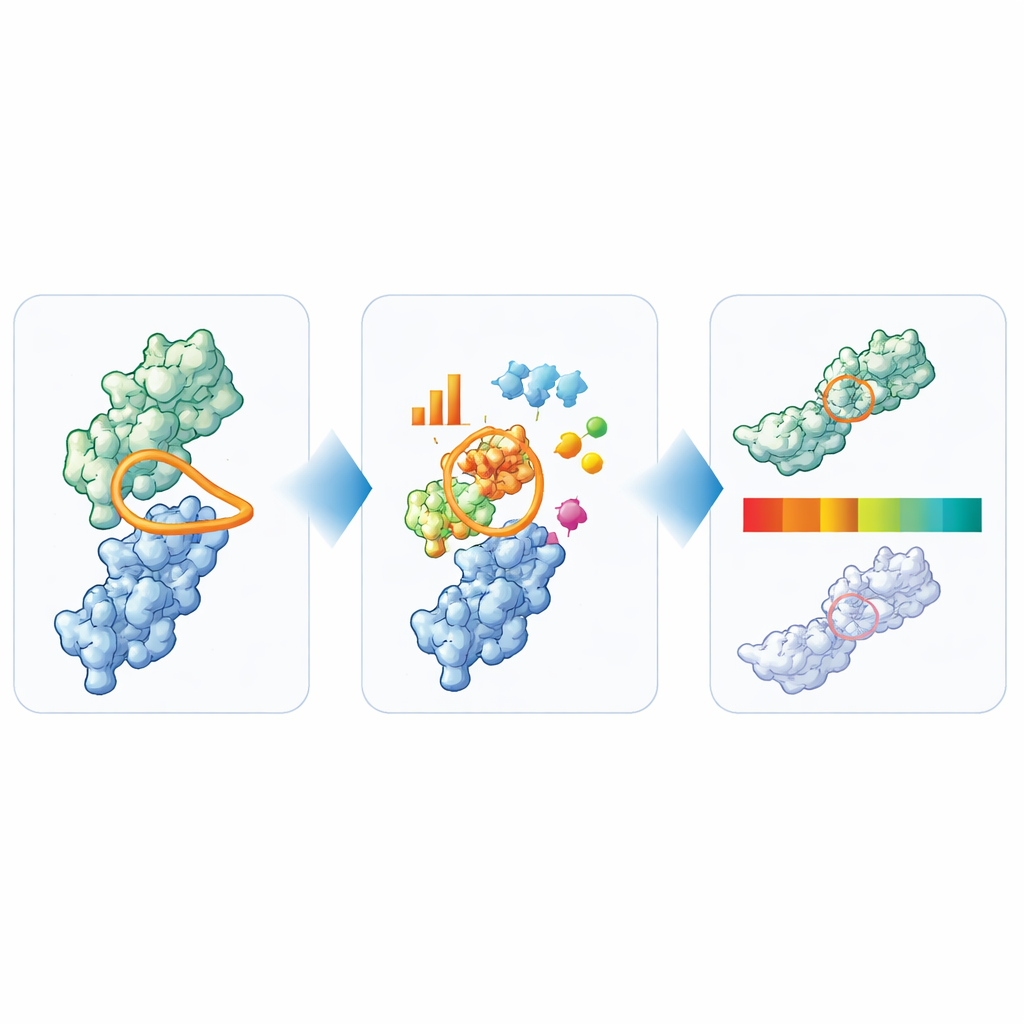
Transformer la structure en feux tricolores simples
À partir de leur large analyse, les auteurs ont distillé six caractéristiques clés qui ensemble captent les principales préoccupations de développabilité pour les nanocorps : longueur totale des boucles, longueur spécifique et compacité du CDR3, et tailles des patches de surface hydrophobes, positivement chargés et négativement chargés autour du site de liaison. Ils ont ensuite utilisé les 36 nanocorps ayant atteint les essais cliniques pour fixer des limites pratiques pour chaque mesure. Les valeurs dans la zone centrale, bien fréquentée, sont étiquetées « vert », les valeurs limitrophes « ambre » et les valeurs clairement atypiques « rouge ». Pour tester l’utilité de ces signaux, ils ont appliqué le TNP à 72 autres nanocorps propriétaires et ont comparé les indicateurs à un large panel de tests de laboratoire. Les nanocorps que le TNP marquait comme outliers clairs présentaient généralement aussi plusieurs signes d’alerte expérimentaux, tandis que ceux qui paraissaient propres en calculatoire se comportaient plus souvent bien en laboratoire.
Ce que cela signifie pour les traitements de demain
Pour les non‑spécialistes, le message central est que la forme et le motif de surface d’un nanocorps peuvent désormais être convertis en un profil de développabilité simple avant de lancer des travaux de laboratoire coûteux. Le Therapeutic Nanobody Profiler ne remplace pas les expériences, et des discordances entre prédictions et essais subsistent, notamment parce que les tests en laboratoire ont été effectués sur des nanocorps fusionnés à des fragments d’anticorps plus volumineux. Mais en signalant rapidement les candidats qui ont des boucles exceptionnellement longues ou très repliées, ou des patches de surface problématiques, le TNP aide à orienter l’attention vers les nanocorps qui ont le plus de chances de devenir des médicaments fiables. Au fur et à mesure que davantage de nanocorps entreront en essais cliniques et élargiront l’ensemble de référence, cet outil devrait gagner en précision, accélérant la conception de médicaments de type anticorps, petits et robustes, pour un large éventail de maladies.
Citation: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Mots-clés: nanocorps, développabilité des médicaments biologiques, profilage computationnel, ingénierie des anticorps, stabilité des protéines