Clear Sky Science · fr
La dégradation de TUBB3 médiée par DTX1 dans les cellules de Kupffer atténue la progression du carcinome hépatocellulaire en régulant la polarisation M1/M2
Pourquoi les « voisins » immunitaires du foie comptent
La plupart des gens considèrent le cancer comme une maladie de cellules déchaînées qui prolifèrent sans contrôle. Mais les tumeurs vivent dans un voisinage animé d’immunocytes, de vaisseaux sanguins et de tissu de soutien qui peuvent soit lutter contre le cancer, soit l’aider discrètement à croître. Cette étude se penche sur le cancer du foie — plus précisément le carcinome hépatocellulaire — et révèle comment une protéine à l’intérieur de cellules immunitaires spécialisées du foie peut faire basculer l’équilibre entre une réponse anti‑cancer et un environnement favorable à la tumeur. Comprendre ce « commutateur » caché pourrait ouvrir de nouvelles voies pour améliorer les immunothérapies actuelles.
Un cancer du foie façonné par son microenvironnement
Le foie est riche en cellules immunitaires, dont une population résidente appelée cellules de Kupffer qui contribue normalement à l’homéostasie de l’organe. Dans le cancer du foie, nombre de ces cellules se transforment en macrophages associés à la tumeur qui peuvent soit attaquer le cancer (état de type M1), soit le protéger (état de type M2). Les patients dont les tumeurs sont envahies de macrophages de type M2 ont en général un pronostic moins bon et répondent souvent mal aux traitements qui libèrent les freins immunitaires, comme les inhibiteurs de PD‑1. Les auteurs ont commencé par exploiter des bases de données génomiques publiques et des échantillons de patients pour rechercher des molécules liées à la fois au cancer du foie et à ces macrophages, et ont identifié une protéine structurale appelée TUBB3 qui était, de façon inattendue, abondante dans les tissus tumoraux.
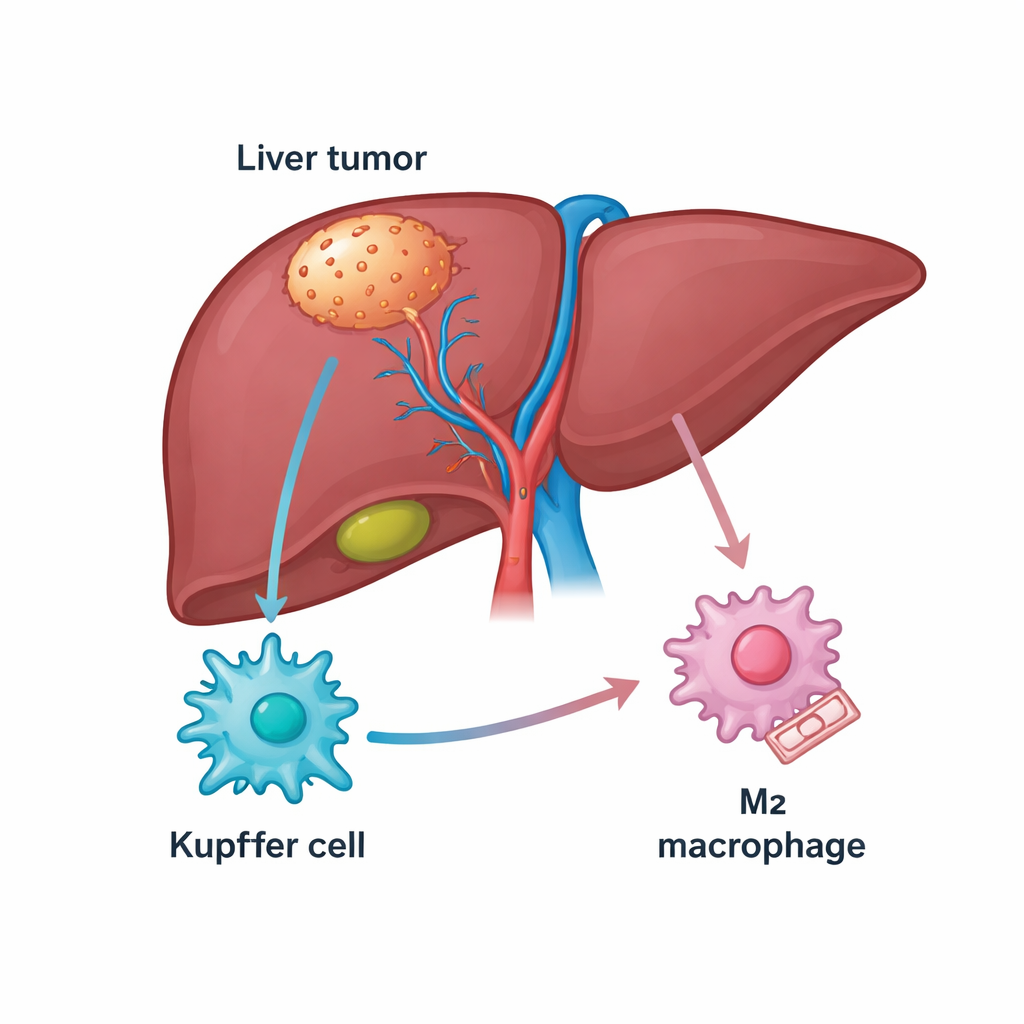
Une protéine surprenante qui pousse les cellules immunitaires à aider la tumeur
TUBB3 est surtout connue comme composant des « rails » microscopiques à l’intérieur des cellules, mais elle a aussi été associée à des comportements agressifs et à la résistance aux médicaments dans plusieurs cancers. Ici, les chercheurs ont observé des niveaux de TUBB3 beaucoup plus élevés dans les tumeurs hépatiques que dans le tissu sain adjacent, et les patients présentant une expression plus élevée de TUBB3 avaient tendance à avoir une survie réduite. Par immunomarquage, ils ont montré que TUBB3 était particulièrement enrichie dans les cellules de Kupffer intratumorales, et sa présence corrélait fortement avec des marqueurs de l’état M2, pro‑tumoral. Autrement dit, les cellules de Kupffer riches en TUBB3 étaient plus susceptibles d’adopter des comportements qui atténuent l’attaque immunitaire et favorisent la croissance tumorale.
Reprogrammer les macrophages pour freiner les tumeurs hépatiques
Pour tester la relation de cause à effet, l’équipe a réduit l’expression de TUBB3 dans les cellules de Kupffer en expérimentations in vitro. Lorsque TUBB3 était éliminée, ces cellules produisaient moins de signaux de type M2, davantage de signaux de type M1, et sécrétaient moins de molécules immunosuppressives. Les cellules de carcinome hépatocellulaire exposées à ces macrophages reprogrammés croissaient plus lentement, se divisaient moins et avaient une capacité réduite de migration et d’invasion. Chez la souris, le mélange de cellules tumorales hépatiques avec des cellules de Kupffer déficientes en TUBB3 conduisait à des tumeurs plus petites, à davantage de mort cellulaire tumorale et à une plus forte infiltration de lymphocytes CD8 cytotoxiques équipés de protéines destructrices. Si les macrophages étaient supprimés chez les animaux, le bénéfice lié au blocage de TUBB3 disparaissait pour l’essentiel, soulignant que l’effet passe par ces cellules immunitaires et non uniquement par les cellules tumorales.
Mettre au jour un frein interne sur une voie de signalisation clé
L’étude a aussi exploré comment TUBB3 exerce cette influence. Les auteurs se sont concentrés sur une voie bien connue de croissance et de survie contrôlée par PTEN et AKT, qui module également l’adoption d’un profil M1 ou M2 par les macrophages. Ils ont découvert que la diminution de TUBB3 augmentait PTEN, ce qui réduisait ensuite les « étiquettes » phosphate activatrices sur AKT, poussant les macrophages vers l’état anti‑tumoral M1. Lorsque AKT était réactivé artificiellement, les macrophages revenaient à un profil M2 et les cellules cancéreuses retrouvaient leur comportement agressif, même en l’absence de TUBB3. Cela place TUBB3 en amont de PTEN et AKT, comme une sorte de cadran interne contrôlant le comportement des macrophages.
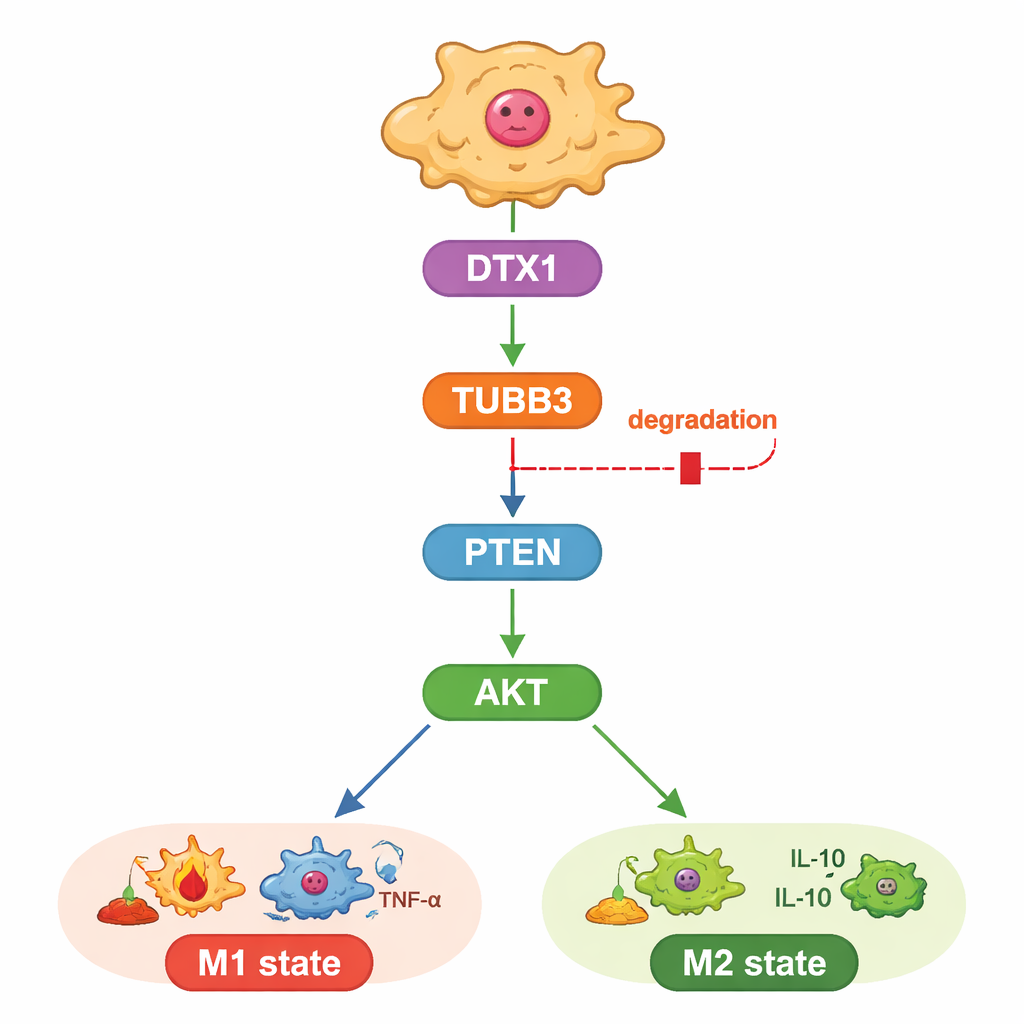
Une étiquette de mise au rebut intégrée qui pourrait être réactivée
Enfin, les chercheurs ont cherché pourquoi TUBB3 est si abondante dans les tumeurs hépatiques. En combinant prédictions bioinformatiques et données d’expression, ils ont identifié une enzyme appelée DTX1, membre d’une famille qui marque les protéines pour leur élimination, comme régulatrice probable. Les niveaux de DTX1 étaient plus faibles dans les tumeurs hépatiques que dans le tissu sain et corrélaient avec de meilleurs résultats cliniques et une plus grande présence de macrophages de type M1. In vitro, l’augmentation de DTX1 accélérera la dégradation de TUBB3, atténua l’activité d’AKT et orienta les macrophages vers l’état anti‑tumoral, limitant la croissance des cellules cancéreuses. Réintroduire massivement TUBB3 annulait les bénéfices de DTX1, tant en culture qu’en tumeurs murines. Ensemble, ces résultats tracent une ligne claire reliant DTX1 à TUBB3 puis à PTEN/AKT et, in fine, au ton immunitaire de la tumeur.
Implications pour le traitement futur du cancer du foie
Pour les non‑spécialistes, le message principal est que ce travail identifie un système de contrôle jusque‑là caché à l’intérieur des cellules immunitaires résidentes du foie qui détermine si elles aident ou entravent le cancer. Quand l’enzyme d’étiquetage pour la mise au rebut DTX1 est faible, TUBB3 s’accumule, une voie de croissance s’active et les cellules de Kupffer glissent vers un mode pro‑tumoral qui réduit l’efficacité des immunothérapies. Restaurer cette voie — en diminuant TUBB3, en augmentant DTX1 ou en modulant finement le signal PTEN/AKT — pourrait réveiller les défenses immunitaires locales et rendre des traitements comme les inhibiteurs de PD‑1 plus efficaces. Bien que ces stratégies en soient encore au stade expérimental, elles soulignent l’intérêt de traiter non seulement les cellules tumorales, mais aussi les « voisins » immunitaires qui influencent fortement le comportement du cancer du foie.
Citation: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Mots-clés: carcinome hépatocellulaire, macrophages associés aux tumeurs, cellules de Kupffer, immunothérapie, signalisation AKT