Clear Sky Science · fr
Sparsification et décorrélation de l’activité des cellules granulaires dans le gyrus denté par la noradrénaline
Pourquoi une poussée d’éveil peut affiner les souvenirs
Les moments qui nous réveillent soudainement — une quasi-collision en voiture, une remarque inattendue, un rebondissement surprenant dans un film — restent souvent en mémoire bien mieux qu’une journée ordinaire. Cette étude explore une raison majeure : un messager chimique lié à l’éveil, la noradrénaline, reconfigure discrètement la façon dont une porte d’entrée importante de la mémoire dans l’hippocampe filtre et sépare les expériences, aidant des événements semblables à être plus faciles à distinguer par la suite.
Le gardien du cerveau pour les expériences proches
À l’intérieur de l’hippocampe se trouve le gyrus denté, une région qui joue le rôle de gardien pour les nouveaux souvenirs. Il reçoit des informations riches en provenance du cortex entorhinal — des signaux sur notre position et ce qui se passe autour de nous — et les convertit en motifs d’activité dans les cellules granulaires, ses neurones principaux. La théorie et les expériences suggèrent que ces motifs doivent être « clairsemés » (seules quelques cellules actives à la fois) et « décorrélés » (des expériences différentes activent des ensembles de cellules différents) afin que les souvenirs ne se confondent pas. Pourtant, comment cette transformation s’opère au niveau des cellules et circuits spécifiques restait flou.
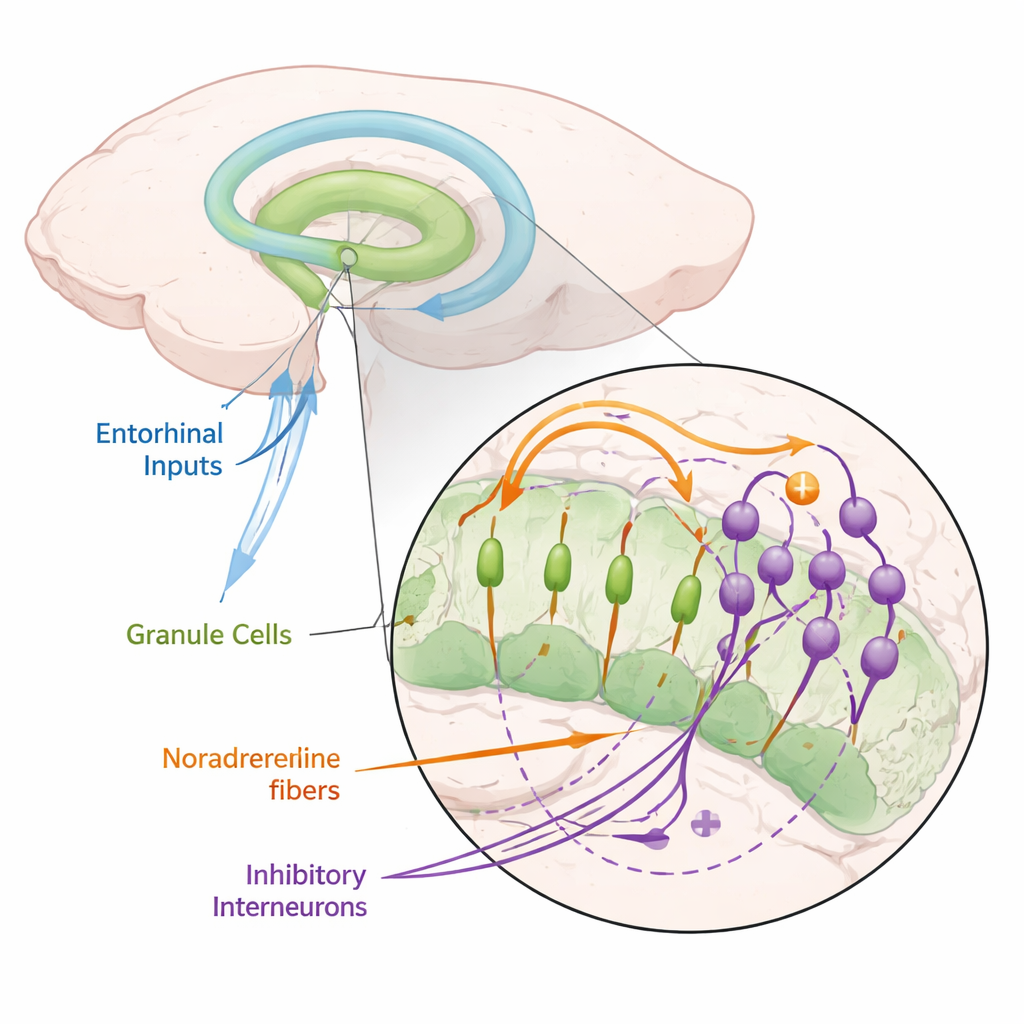
Un produit de l’éveil qui calme des cellules clés de la mémoire
Les auteurs se sont concentrés sur la noradrénaline, un neuromodulateur libéré par des neurones d’une petite zone du tronc cérébral appelée locus coeruleus, qui s’active pendant l’attention, la nouveauté et le stress. Chez la souris, ils ont exprimé des protéines sensibles à la lumière dans ces neurones noradrénergiques, leur permettant de libérer de la noradrénaline sur commande par de brefs éclairs lumineux. Lorsqu’ils ont stimulé la principale voie d’entrée du gyrus denté et enregistré l’activité des cellules granulaires, ils ont constaté que la libération de noradrénaline réduisait fortement la propension de ces cellules à déclencher des potentiels d’action. Cette suppression s’observait tant au niveau des neurones individuels que des signaux de population, et elle était reproduite en plongeant simplement des coupes dans une solution contenant de la noradrénaline. Le blocage des récepteurs de la noradrénaline éliminait l’effet, montrant qu’il dépendait bien de ce messager chimique.
Pas une excitation plus faible, mais des freins renforcés
Pour comprendre comment la noradrénaline silencait les cellules granulaires, l’équipe a vérifié les explications évidentes. Elle ne modifiait pas de façon significative le potentiel de repos ni la résistance d’entrée des cellules granulaires, ce qui signifie que leur excitabilité de base restait à peu près la même. Elle n’affaiblissait pas non plus les courants excitateurs que ces cellules reçoivent du cortex entorhinal. En revanche, lorsque les chercheurs ont bloqué les récepteurs GABAA, qui médiatisent l’inhibition, la noradrénaline n’a plus pu supprimer le déclenchement des cellules granulaires. Des mesures détaillées de courants ont montré que la noradrénaline renforçait sélectivement une forme rapide d’inhibition feedforward : les signaux excitateurs entrants activaient d’abord un ensemble d’interneurones, lesquels inhibaient rapidement les cellules granulaires avant qu’elles ne puissent émettre des spikes. Les analyses temporelles ont révélé que ce courant inhibiteur sensible à la noradrénaline arrivait juste après l’excitation directe, mais avant que la population principale de cellules granulaires ne tire, caractéristique d’un frein feedforward.
Cellules inhibitrices spécialisées qui imposent le timing
Quels interneurones fournissaient cette inhibition cruciale ? De manière surprenante, les cellules exprimant la parvalbumine, longtemps considérées comme dominantes pour le contrôle feedforward rapide, n’étaient pas responsables — la noradrénaline les rendait même moins actives. Les acteurs clés étaient plutôt des interneurones exprimant la cholécystokinine (cellules CCK). Ces cellules reçoivent une entrée directe des mêmes fibres corticales qui excitent les cellules granulaires et tirent juste avant ces dernières, ce qui indique un rôle feedforward. La noradrénaline dépolarise les cellules CCK, les rendant plus facilement recrutables, et augmente la probabilité que les signaux d’entrée les déclenchent, sans changer la force de chaque connexion inhibitrice individuelle. Lorsque les chercheurs ont pharmacologiquement bloqué la sortie des cellules CCK, la noradrénaline n’a plus pu supprimer l’activité des cellules granulaires. En pratique, la noradrénaline active un circuit d’interneurones CCK qui impose une fenêtre temporelle très étroite pendant laquelle les pics excitateurs entrants peuvent effectivement déclencher les cellules granulaires.
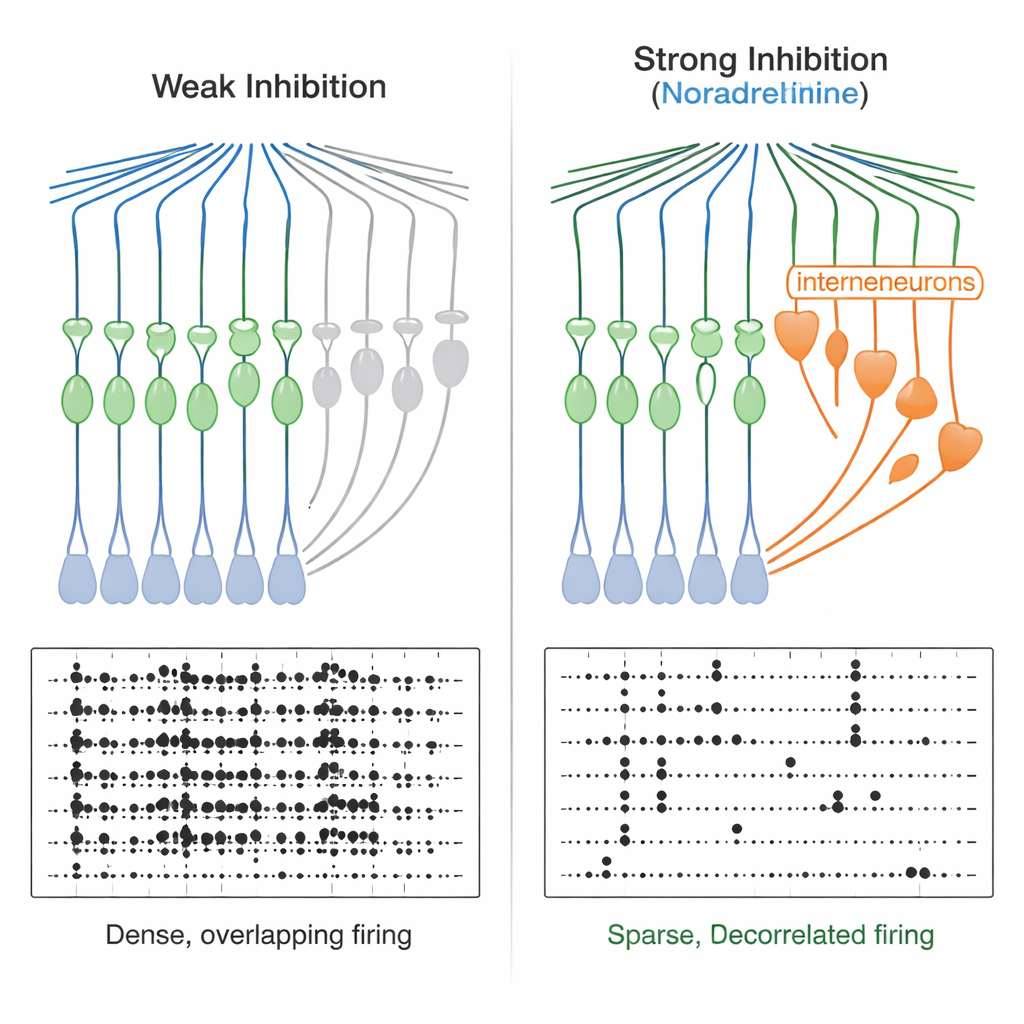
De fenêtres étroites à des codes mnésiques plus propres
Ce resserrement du timing a des conséquences puissantes. Lorsque l’équipe a délivré des paires d’entrées excitatrices brèves, ils ont constaté que, en conditions normales, les cellules granulaires pouvaient intégrer des entrées espacées de dizaines de millisecondes pour produire un spike. En présence de noradrénaline, la fenêtre se réduisait à seulement quelques millisecondes — les cellules granulaires répondaient désormais presque exclusivement à des entrées hautement synchronisées. Des modèles de réseau computationnel ont confirmé que renforcer et accélérer l’inhibition feedforward produisait une sortie plus clairsemée et réduisait les recouvrements entre motifs d’activité, améliorant la « décorrélation ». Expérimentalement, lorsque les chercheurs ont injecté deux motifs d’entrée similaires mais non identiques dans le gyrus denté, les cellules granulaires ont répondu par des motifs de tir plus distincts en présence de noradrénaline, aussi bien dans des enregistrements de cellules uniques que dans l’imagerie calcique de nombreuses cellules. Parallèlement, l’activité globale des cellules granulaires devenait plus clairsemée.
Comment l’éveil peut nous aider à séparer des souvenirs semblables
Pour le lecteur non spécialiste, la conclusion est que la noradrénaline, libérée lorsque nous sommes alertes ou émotionnellement engagés, aide un filtre mnésique clé de l’hippocampe à devenir plus sélectif. En dynamisant une classe spécifique de cellules nerveuses inhibitrices, elle rétrécit la fenêtre temporelle pendant laquelle les entrées peuvent déclencher les cellules granulaires, de sorte que seuls des signaux étroitement synchronisés et significatifs passent. Cela réduit le déclenchement global, diminue le chevauchement des motifs d’activité et aide le cerveau à stocker des expériences semblables — par exemple deux salles de classe ou deux conversations — comme des souvenirs distincts plutôt qu’un flou. Le travail révèle un mécanisme de circuit concret reliant un éveil instantané à des souvenirs plus précis et moins confus.»
Citation: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Mots-clés: noradrénaline, gyrus denté, interneurones inhibiteurs, séparation de motifs, mémoire épisodique