Clear Sky Science · fr
Aperçus structurels de l’hélicase WRN révèlent des états conformationnels et des opportunités pour la découverte de médicaments contre les cancers MSI‑H
Pourquoi c’est important pour le traitement du cancer
Certaines tumeurs possèdent une faiblesse intrinsèque : elles ont du mal à réparer les erreurs de leur ADN. Une protéine nommée hélicase WRN joue le rôle d’un outil moléculaire de réparation qui maintient ces tumeurs fragiles en vie. Cette étude révèle, au niveau atomique, comment WRN se déplace le long de l’ADN et comment des composés expérimentaux peuvent bloquer ce mouvement — offrant une feuille de route pour de nouveaux traitements visant à tuer sélectivement ces cellules cancéreuses vulnérables tout en épargnant les tissus sains.
Le« bricoleur » de l’ADN sous le microscope
L’hélicase WRN fait partie de l’équipe d’entretien de la cellule, aidant à dérouler l’ADN pour que les dommages puissent être détectés et réparés. Les personnes nées sans WRN fonctionnelle développent le syndrome de Werner, une maladie rare caractérisée par un vieillissement prématuré, ce qui montre l’importance cruciale de cette protéine pour la maintenance du génome. Les tumeurs présentant une instabilité des microsatellites élevée (MSI‑H) — défaut fréquent dans le cancer colorectal et certains autres cancers — s’avèrent particulièrement dépendantes de WRN. Lorsque WRN est inactivée dans ces cellules, leur ADN déjà fragile se désintègre rapidement et les cellules cancéreuses meurent. Cela fait de WRN une cible médicamenteuse intéressante, mais jusqu’à présent les scientifiques manquaient d’une vision claire de la façon dont la protéine change de conformation lorsqu’elle saisit l’ADN, consomme son carburant chimique et se déplace le long de la molécule génétique.
Observer WRN se contracter et respirer
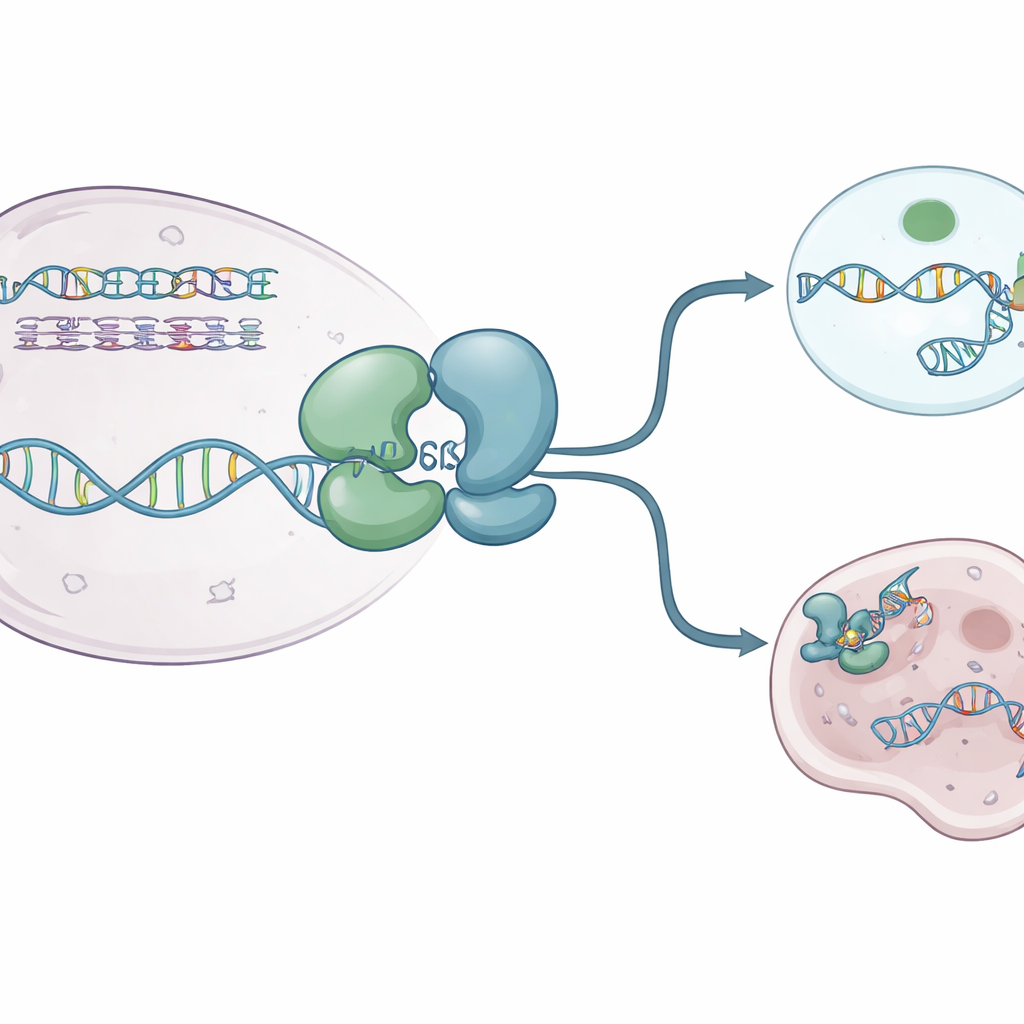
Les auteurs ont utilisé la cristallographie aux rayons X pour capturer plusieurs « instantanés » haute résolution du cœur de l’hélicase humaine WRN. Ils ont résolu des structures de WRN seule et de WRN liée à de l’ADN simple brin et à une molécule de type ATP non hydrolysable. Ces vues ont révélé que la protéine est constituée de deux lobes principaux reliés par une charnière flexible qui se comporte comme une articulation respirante. À l’état au repos, sans carburant, WRN adopte une forme compacte « fermée » dans laquelle les lobes sont rapprochés. En présence d’un analogue d’ATP et d’ADN, les lobes s’écartent pour former une configuration plus « ouverte » capable d’accueillir l’ADN dans une gouttière chargée positivement. Une petite boucle aromatique à l’intérieur de WRN se reconfigure en une courte hélice et s’insère entre les bases de l’ADN, agissant comme un cliquet qui aide la protéine à avancer sans reculer.
Comment les médicaments actuels inactivent WRN
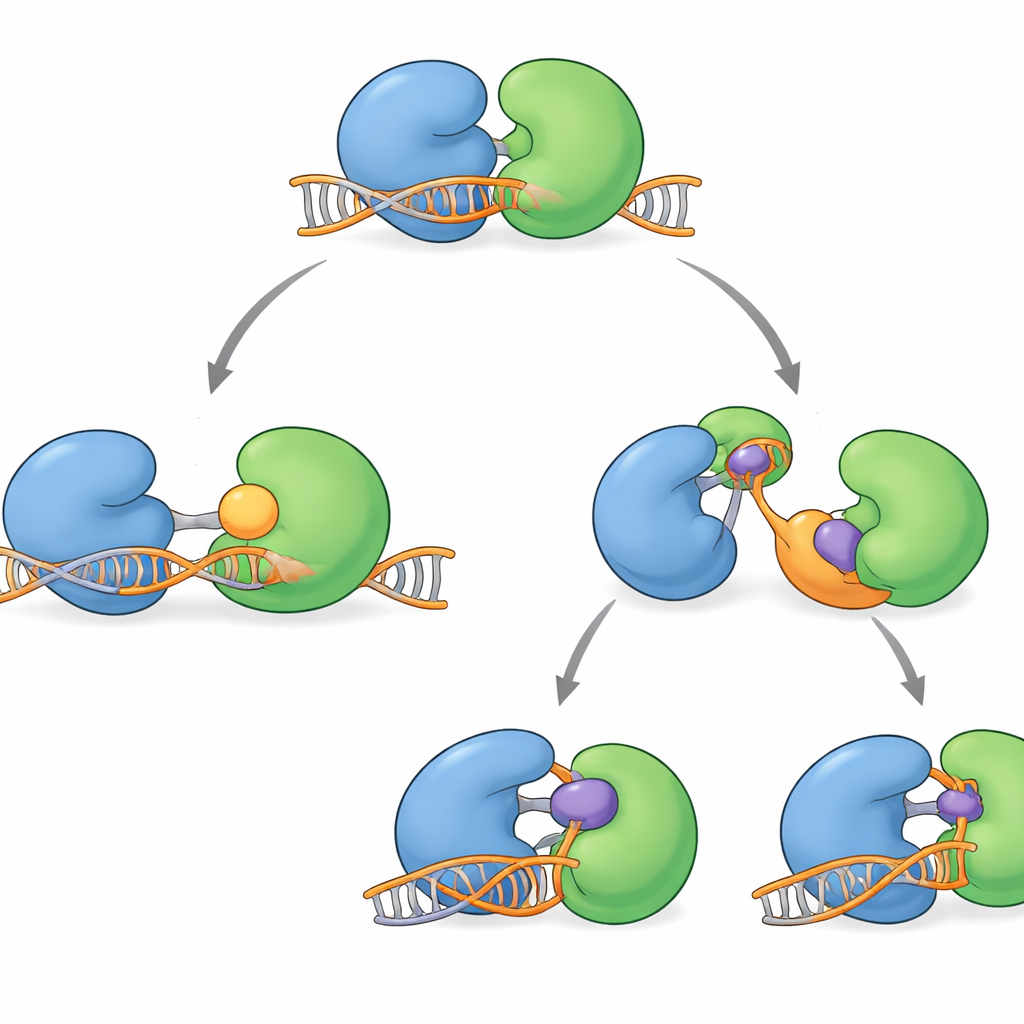
Plusieurs composés bloquant WRN sont récemment entrés en essais cliniques. Ils ne bouchent pas directement la gouttière active de la protéine. Au contraire, ils agissent à distance, en saisissant la région de la charnière et en verrouillant WRN dans des conformations incapables d’interagir correctement avec l’ADN. Certaines molécules, telles que HRO761 et un candidat clinique apparenté de GSK, pivottent un lobe d’environ 180 degrés par rapport à l’autre, créant une forme « tordue » spectaculaire qui se situe en dehors de l’ADN. D’autres, dont VVD‑133214 et un composé étroitement apparenté étudié ici, maintiennent WRN dans une configuration fortement « fermée » qui n’expose pas les surfaces clés de liaison à l’ADN. Des expériences biophysiques ont confirmé que, lorsque ces médicaments sont liés, WRN ne peut plus former un complexe stable avec l’ADN simple brin, rompant ainsi efficacement le lien entre l’utilisation d’ATP et le déroulement de l’ADN.
Comment les cellules cancéreuses apprennent à échapper
Pour comprendre comment les tumeurs pourraient échapper à ces médicaments, l’équipe a cultivé des cellules de cancer colorectal MSI‑H en présence d’inhibiteurs de WRN pendant plusieurs semaines à mois. Des populations résistantes sont apparues rapidement. L’analyse génétique a montré que, dans chaque cas, les cellules avaient acquis un changement unique et précis dans le gène WRN près de la charnière de liaison au médicament. Une mutation a atténué l’effet de l’inhibiteur favorisant l’état « tordu » HRO761, tandis qu’une autre mutation a réduit la sensibilité à VVD‑133214, qui favorise l’état fermé. De plus, de nombreuses cellules résistantes ont augmenté la production de WRN, s’octroyant davantage de copies de la cible et diluant partiellement l’effet du médicament. Ces observations reflètent des schémas de résistance déjà vus avec d’autres médicaments ciblés, où de petites modifications structurelles de la protéine cible ou une surexpression peuvent amoindrir l’efficacité du traitement.
Vers des bloqueurs de WRN plus intelligents
Pris ensemble, les nouvelles structures cartographient un cycle de fonctionnement complet pour WRN lorsqu’elle se fixe à l’ADN, progresse puis se réinitialise. Elles montrent aussi que les composés cliniques actuels stabilisent principalement des formes de la protéine « hors de l’ADN ». Pour le lecteur général, le point clé est que nous comprenons désormais où WRN est vulnérable et comment les tumeurs peuvent s’adapter. Cela suggère une nouvelle génération d’inhibiteurs qui se lient à WRN lorsqu’elle est verrouillée sur l’ADN, la piégeant potentiellement dans un état toxique — à l’instar de médicaments efficaces qui piègent d’autres enzymes de réparation de l’ADN. De tels bloqueurs « sur ADN » de WRN, utilisés seuls ou en association avec des agents existants, pourraient offrir des moyens plus durables d’exploiter la faiblesse cachée des cancers MSI‑H.
Citation: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Mots-clés: hélicase WRN, instabilité des microsatellites, réparation de l’ADN, inhibiteurs allostériques, résistance aux médicaments