Clear Sky Science · fr
PiR48444 inhibe la différenciation ostéogénique des CSM et la régénération osseuse en ciblant la méthylation m6A de BMP2 médiée par METTL7A/eIF4E
Pourquoi de minuscules molécules comptent pour les os cassés
Les fractures et la perte osseuse liée à l’âge sont des problèmes fréquents, et les médecins cherchent à utiliser des cellules souches pour aider l’organisme à reconstruire le squelette endommagé. Pourtant, ces cellules souches ne forment pas toujours de l’os aussi efficacement qu’on le souhaiterait, en particulier chez les personnes âgées ou dans des tissus inflammés. Cette étude met en évidence une petite molécule d’ARN, nommée piR48444, qui agit comme un frein moléculaire sur les cellules souches formant l’os. En relâchant ce frein, les chercheurs montrent qu’il pourrait être possible de stimuler la réparation osseuse et de protéger contre la perte de masse osseuse.
Un frein caché dans de nombreux types de cellules souches
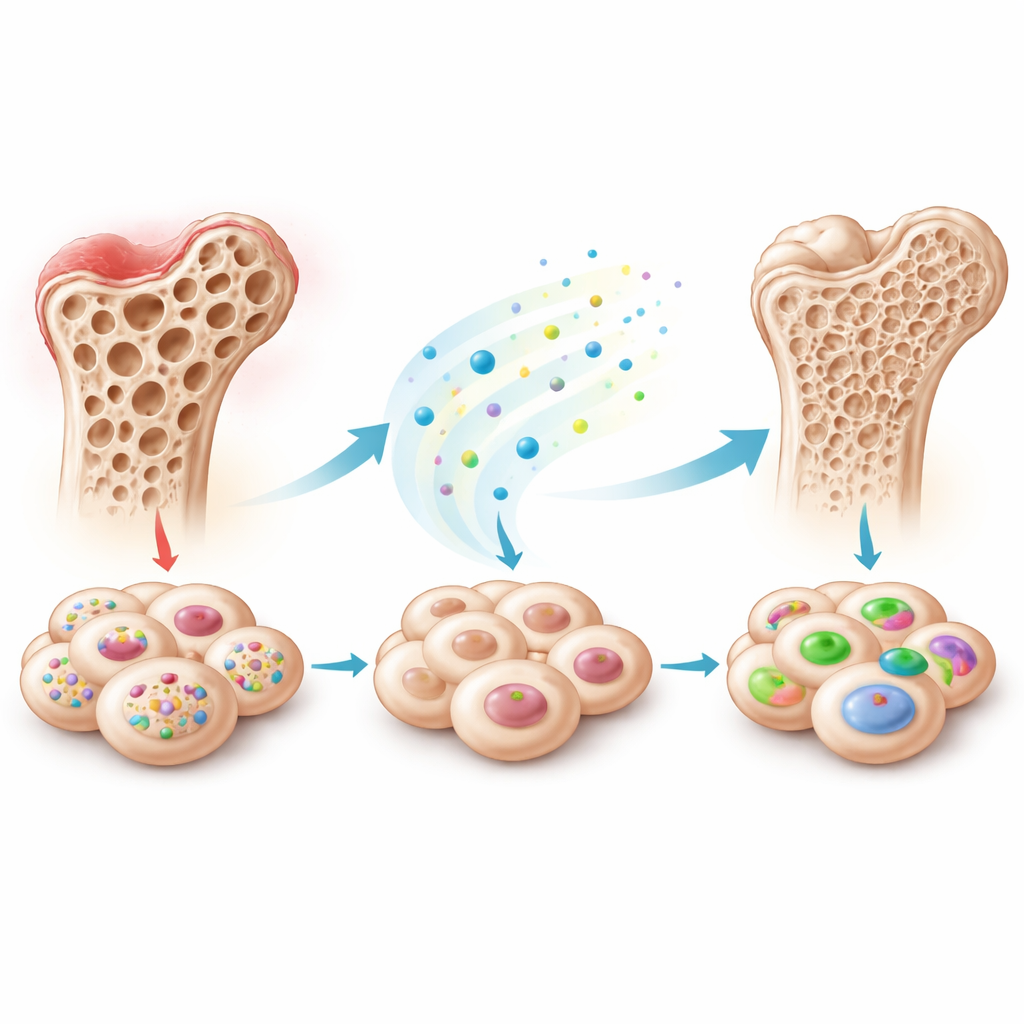
L’équipe s’est concentrée sur les cellules souches mésenchymateuses, des cellules polyvalentes pouvant donner de l’os, du cartilage, de la graisse, et plus encore, et qui sont isolées de nombreux tissus comme la moelle osseuse, les dents de lait et le tissu adipeux. Lorsque ces cellules sont incitées à devenir os en laboratoire, des milliers de gènes et de petits ARNs modifient leur activité. En séquençant ces molécules dans des cellules souches issues de dents de lait exfoliées, les chercheurs ont trouvé qu’un ARN particulier, piR48444, diminuait régulièrement à mesure que les cellules se dirigeaient vers le phénotype osseux. Ils ont ensuite vérifié d’autres types de cellules souches et observé le même schéma : les cellules produisant davantage d’os présentaient moins de piR48444, ce qui suggère que cette molécule limite normalement leur capacité à former du tissu osseux.
Des plats de laboratoire aux os vivants
Pour tester cette hypothèse, les scientifiques ont modifié les niveaux de piR48444 dans plusieurs types de cellules souches. Lorsqu’ils ont réduit piR48444, les cellules ont déposé plus de calcium, activé des gènes liés à l’os et pris sous le microscope une apparence plus proche d’un tissu osseux immature. Lorsqu’ils ont forcé la production supplémentaire de piR48444, l’effet inverse est apparu : l’activité liée à l’os a diminué. L’équipe est ensuite passée à des modèles animaux. Des cellules souches avec piR48444 désactivé ont été utilisées pour combler de petits défauts crâniens chez la souris. Ces cellules modifiées ont généré beaucoup plus de nouvel os que les cellules témoins, comme le montrent des reconstructions 3D par rayons X et des colorations tissulaires, suggérant que bloquer piR48444 peut améliorer de façon tangible la réparation osseuse in vivo.
Protéger les os fragiles en cas de maladie et de vieillissement
La perte osseuse est déclenchée non seulement par les blessures, mais aussi par l’inflammation et le vieillissement. Dans des cellules souches de moelle osseuse exposées à des toxines bactériennes, et dans des cellules souches provenant d’animaux âgés, les niveaux de piR48444 étaient anormalement élevés tandis que les marqueurs de formation osseuse étaient faibles. Les chercheurs ont conçu un « antagomir » — une courte molécule destinée à neutraliser piR48444 dans la circulation — et l’ont injecté à des souris présentant une perte osseuse induite par l’inflammation ou à des souris naturellement âgées. Dans les deux modèles, les animaux traités ont conservé une bien plus grande partie de leur os spongieux interne, avec des trabécules plus denses et plus nombreuses, tandis que la corticale externe restait inchangée. Cela indique que bloquer piR48444 peut protéger sélectivement la partie fragile et métaboliquement active du squelette la plus vulnérable pendant le vieillissement et l’inflammation chronique.
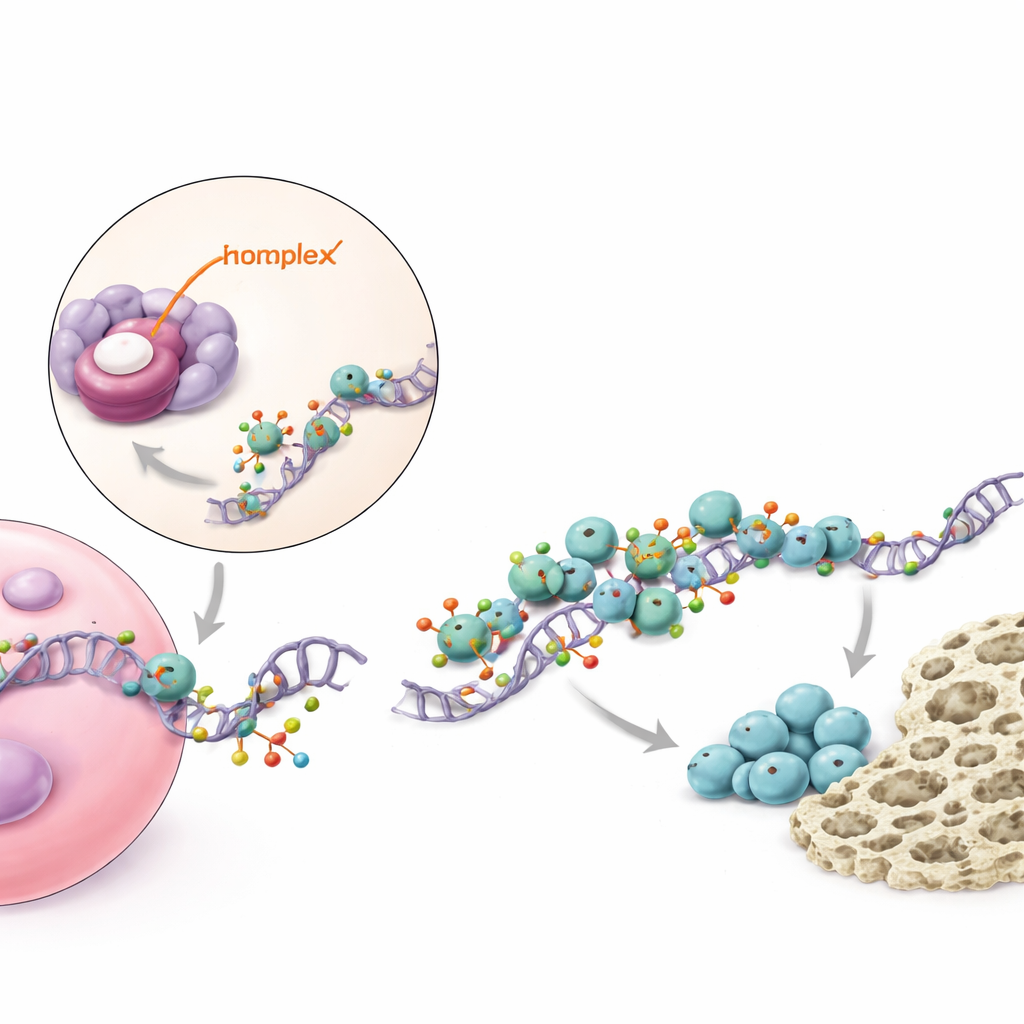
Un relais moléculaire qui amplifie un signal clé pour l’os
En approfondissant, l’étude a cartographié comment piR48444 exerce ses effets à l’intérieur des cellules. Ce petit ARN se lie à une protéine appelée METTL7A et l’inhibe : METTL7A agit comme une enzyme qui modifie les ARNm portant le plan de BMP2, un facteur de croissance bien connu qui favorise fortement la formation osseuse. METTL7A ajoute de petites marques chimiques aux messages de BMP2, les rendant plus stables et plus faciles à traduire par la machinerie de synthèse protéique. METTL7A coopère également avec une autre protéine, eIF4E, qui aide à initier la production protéique. Lorsque piR48444 est abondant, METTL7A est réprimé, moins de messages BMP2 sont marqués et traduits, et moins de protéine BMP2 est produite, si bien que les cellules souches ont moins tendance à devenir os. Lorsqu’on bloque piR48444, METTL7A et BMP2 augmentent, poussant les cellules vers l’ostéogenèse.
Ce que cela signifie pour la réparation osseuse future
En termes simples, les auteurs révèlent une chaîne de contrôle dans laquelle un petit ARN (piR48444) atténue une enzyme auxiliaire (METTL7A), qui à son tour limite un signal puissant de construction osseuse (BMP2). En interrompant cette chaîne au niveau de piR48444, ils parviennent à améliorer la capacité de diverses cellules souches à former de l’os et à diminuer la perte osseuse chez la souris. Si la sécurité, les effets hors cible et les conséquences à long terme doivent encore être rigoureusement évalués, ces travaux positionnent piR48444 à la fois comme un marqueur sanguin potentiel du risque d’ostéoporose et comme une cible prometteuse pour des médicaments destinés à améliorer la régénération osseuse basée sur les cellules souches en clinique.
Citation: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Mots-clés: régénération osseuse, cellules souches mésenchymateuses, ostéoporose, ARN non codant, signalisation BMP2