Clear Sky Science · fr
Le pincement local par cations déforme et ramollit le duplex d’ARN
Pourquoi ce petit pli de l’ARN compte
À l’intérieur de chaque cellule, l’ADN et l’ARN sont en permanence pliés, étirés et torsadés lorsqu’ils stockent et utilisent l’information génétique. Ces mouvements ne sont pas de simples détails mécaniques : ils régulent la lecture des gènes, la réplication des virus et le fonctionnement des futurs médicaments et nanodispositifs à base d’ARN. Cette étude montre que de simples sels composés d’ions positifs et négatifs peuvent modifier de façon spectaculaire la rigidité ou la souplesse de l’ARN, et que l’ARN réagit très différemment de l’ADN. Comprendre cette subtile alternance « ramollissement et raideur » pourrait aider les scientifiques à mieux concevoir des médicaments à base d’ARN, des vaccins et des outils moléculaires.
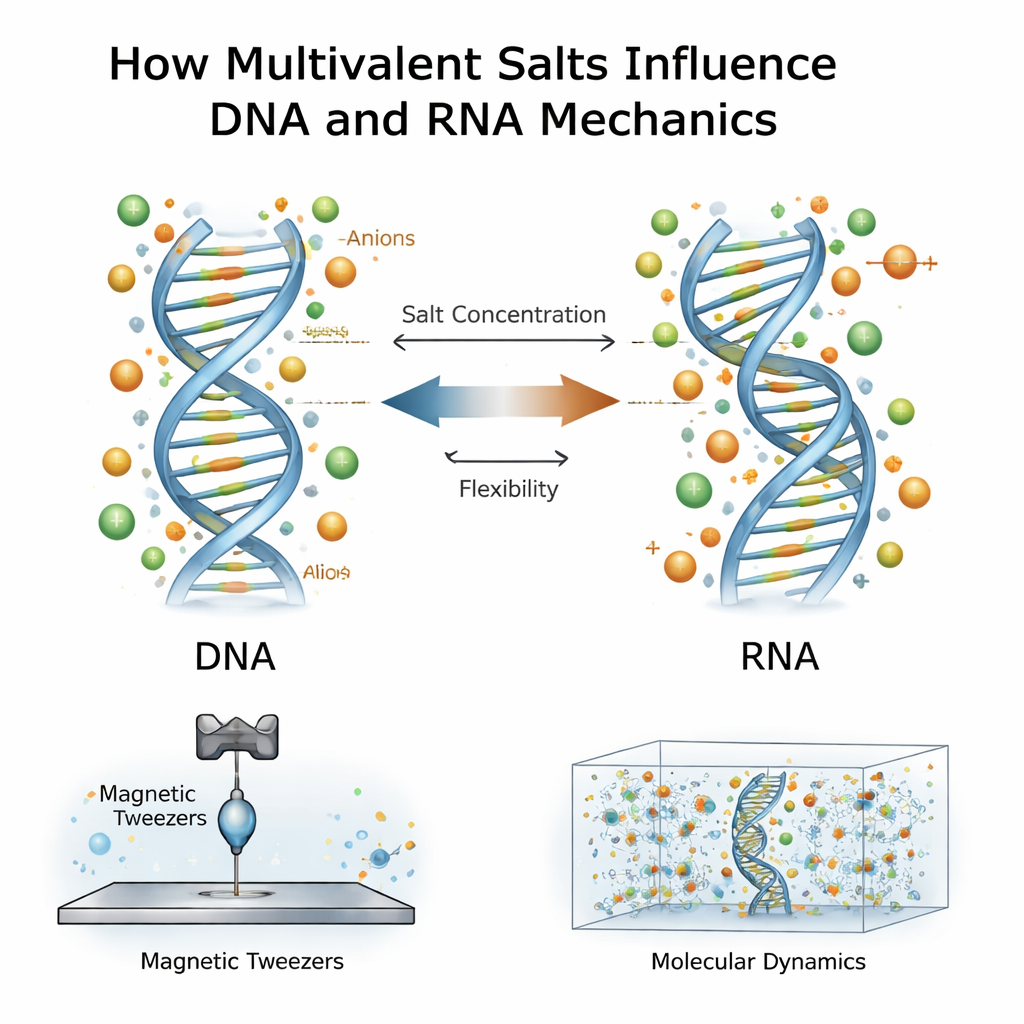
Milieux salés et molécules génétiques
L’ADN et l’ARN portent une forte charge électrique négative, et sont donc entourés en solution de nuages d’ions de charge opposée. Les travaux antérieurs se sont surtout concentrés sur les ions positifs, en particulier les ions multivalents portant deux ou trois charges positives, comme le magnésium ou la spermidine. On sait que ces ions maintiennent les brins d’ADN ensemble, les condensent ou modifient leur facilité à se plier. L’ARN, bien que chimiquement proche de l’ADN, se comporte différemment : il est généralement plus difficile à plier mais plus facile à étirer. Le travail nouveau pose une question plus profonde : que se passe-t-il lorsque non seulement les ions positifs, mais aussi leurs partenaires négatifs — les anions — interagissent avec l’ADN et l’ARN à des concentrations de sel très élevées, bien supérieures à celles d’une cellule typique ?
Tirer sur des molécules uniques pour mesurer la rigidité
Les chercheurs ont utilisé une technique appelée pinces magnétiques pour étirer individuellement des hélices doubles d’ADN ou d’ARN, une par une. Chaque molécule était ancrée d’un côté à une surface de verre et de l’autre à une minuscule bille magnétique. En déplaçant des aimants au-dessus de l’échantillon, ils pouvaient exercer des forces contrôlées et enregistrer l’extension de chaque molécule et sa torsion sous tension. À partir de ces courbes force–extension, ils ont extrait quatre caractéristiques mécaniques clés : la résistance au pliage, la résistance à l’étirement, la longueur effective par paire de bases et la façon dont la torsion modifie la longueur. Ils ont répété ces mesures sur une large plage de concentrations d’ions multivalents pour plusieurs sels différents, y compris la spermidine et le chlorure de calcium.
L’ADN se raidit à nouveau, mais l’ARN s’adoucit brutalement
Pour l’ADN, le comportement correspondait en grande partie aux attentes. À mesure que la concentration d’ions positifs multivalents augmentait, l’ADN devenait d’abord plus facile à plier — sa rigidité diminuait — parce que les ions neutralisaient sa charge négative. À des niveaux encore plus élevés, l’excès d’ions positifs surcompensait, inversant effectivement la charge nette de l’ADN. Cette « inversion de charge » rendait l’ADN de nouveau plus difficile à plier, et sa rigidité augmentait. De façon surprenante, l’ARN montrait un schéma opposé et plus spectaculaire. À faibles et moyennes concentrations de sel, sa rigidité au pliage augmentait : le duplex d’ARN devenait plus droit et plus rigide. Mais à des concentrations très élevées, la rigidité au pliage de l’ARN chutait de plus de moitié, et d’autres propriétés, comme son élasticité à l’étirement et le couplage torsion–extension, se renversaient de manière inattendue.
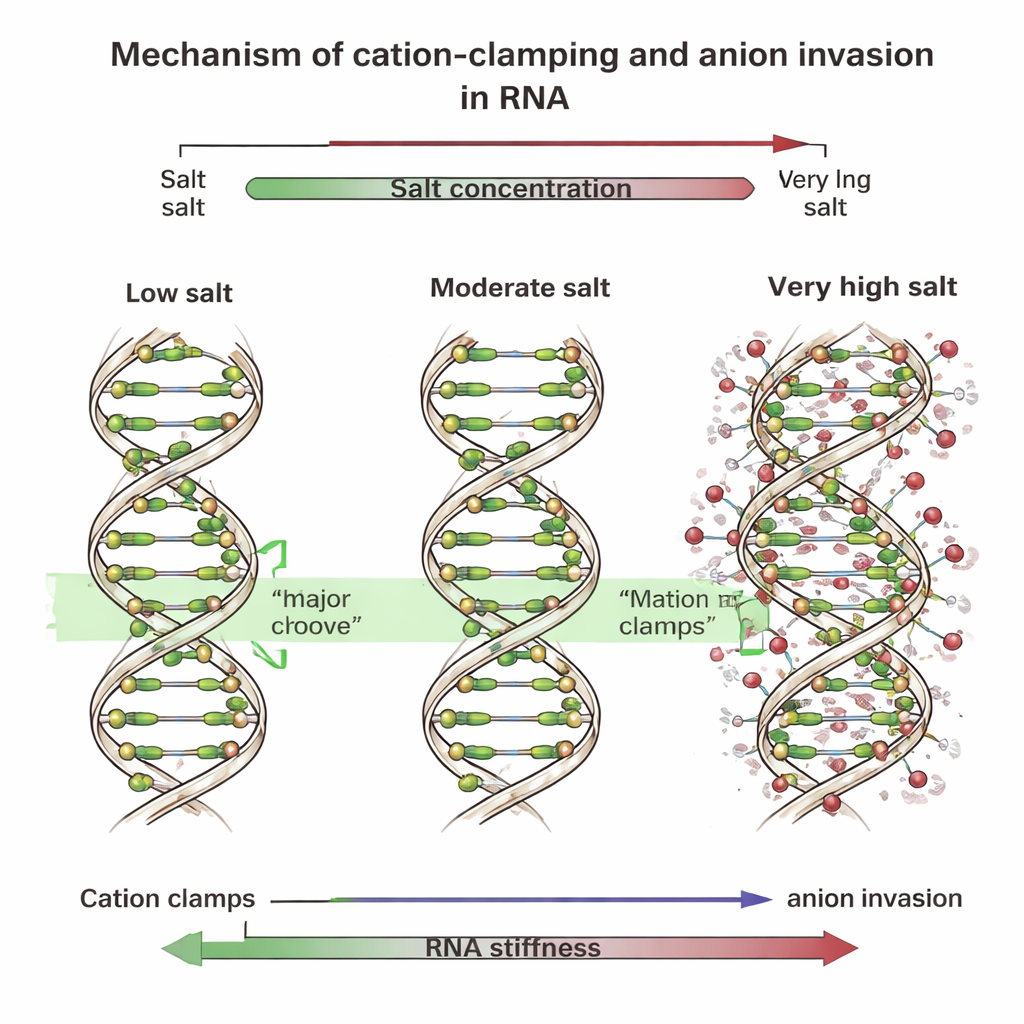
Pinceaux, sillons et ions envahissants
Pour en déterminer la cause, l’équipe a exécuté des simulations informatiques détaillées suivant chaque atome de courts fragments d’ADN et d’ARN en milieu salin. Ces simulations ont révélé qu’à faibles et moyennes concentrations, les ions positifs multivalents se logent dans une large surface de l’ARN appelée grand sillon. Là, ils forment des « pinces cationiques » qui font le pont à travers le sillon, rapprochant ses parois, redressant l’hélice et la rigidifiant. L’ADN, dont la géométrie des sillons est différente, lie principalement ces ions le long de son squelette externe. À des niveaux de sel très élevés, cependant, de nombreux ions négatifs — comme le chlorure — se rapprochent du squelette de l’ARN et pénètrent même dans le grand sillon. Leur présence perturbe les pinces ordonnées, les transformant en « pinces locales » irrégulières et parsemées qui déforment l’hélice. Lorsque les chercheurs ont reproduit cet effet en ajoutant des ressorts artificiels ou en plaçant des ions négatifs supplémentaires près de l’ARN dans les simulations, le squelette de l’ARN se pliait davantage et sa rigidité globale s’effondrait, exactement comme observé expérimentalement.
Ce que cela signifie pour les technologies ARN de demain
En termes simples, l’étude montre que l’ARN peut devenir soit plus droit et plus raide, soit plus plié et plus souple simplement en changeant le type et la concentration des sels environnants. À des niveaux modestes d’ions multivalents, les charges positives serrent proprement la surface de l’ARN et le consolident ; à des niveaux extrêmes, des ions négatifs envahissants brisent ce renfort uniforme et créent des régions déformées et plus molles. L’ADN ne présente pas ce ramollissement net parce qu’il lie les ions différemment et subit plutôt une inversion de charge nette. Ces résultats soulignent que non seulement les ions positifs, mais aussi leurs partenaires négatifs jouent un rôle crucial dans le contrôle de la forme de l’ARN. Cette connaissance aidera les chercheurs à ajuster délibérément la mécanique de l’ARN en laboratoire — par exemple pour stabiliser des médicaments à base d’ARN, contrôler le repliement de l’ARN dans des capteurs biologiques ou concevoir des nanostructures à base d’ARN plus fiables.
Citation: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Mots-clés: Mécanique de l’ARN, ions multivalents, pincement cationique, ADN versus ARN, effets du sel