Clear Sky Science · fr
CISH, un point de contrôle intracellulaire clé, en comparaison et en combinaison avec les points de contrôle immunitaires existants et émergents contre le cancer
Relâcher les freins des cellules anti-cancer
Les immunothérapies contre le cancer ont changé le pronostic de nombreux patients, mais une grande partie d’entre eux n’en retirent encore que peu ou pas de bénéfice. Cette étude explore une nouvelle façon de suralimenter les propres lymphocytes T du corps — les exécuteurs du système immunitaire — en désactivant un « frein » interne appelé CISH. Contrairement aux médicaments actuels qui agissent sur des interrupteurs à la surface cellulaire, cette stratégie cible un système de contrôle enfoui à l’intérieur de la cellule, avec pour objectif de rendre les lymphocytes T modifiés beaucoup plus efficaces pour repérer et détruire les tumeurs, même lorsque les cancers cherchent à se cacher.
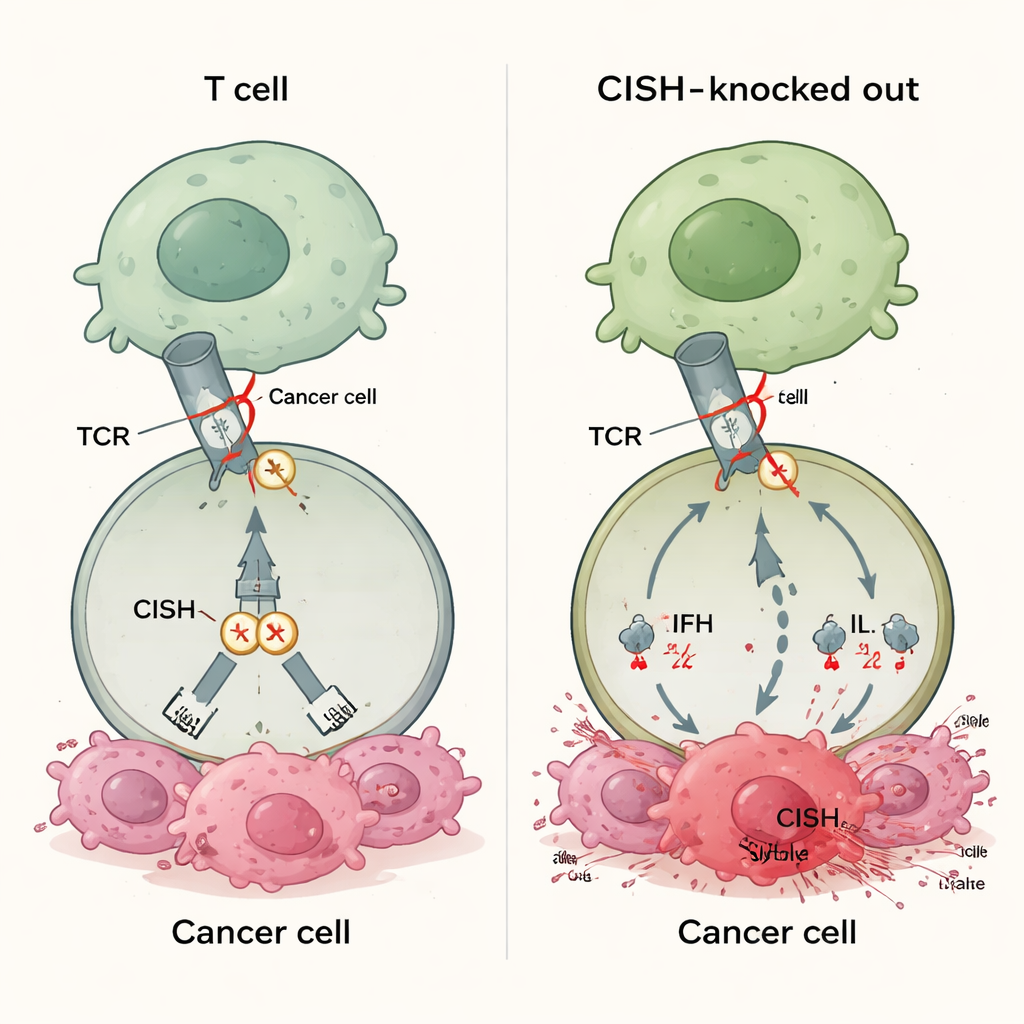
Un nouveau type de frein immunitaire
La plupart des médicaments d’immunothérapie approuvés bloquent des protéines comme PD-1 à la surface des lymphocytes T. Ces médicaments ne fonctionnent que lorsque les tumeurs affichent des molécules partenaires correspondantes comme PD-L1, et de nombreux cancers n’expriment soit jamais suffisamment ces partenaires, soit les perdent au fil du temps. Cela explique en partie pourquoi 30 à 60 % des patients ne répondent pas aux thérapies par points de contrôle actuelles. CISH appartient à une classe différente de freins qui siègent à l’intérieur du lymphocyte T. Il est activé lorsque le récepteur des lymphocytes T détecte une cible, puis atténue le signal en favorisant la destruction d’une protéine clé de signalisation. Parce que cette action ne dépend pas de ligands exprimés par la tumeur, désactiver CISH pourrait, en principe, renforcer les réponses des lymphocytes T dans de nombreux types de cancers, indépendamment du statut PD-L1 ou d’autres biomarqueurs.
Face à face avec les points de contrôle existants
Les chercheurs ont utilisé l’édition génique CRISPR pour supprimer CISH et ont comparé les lymphocytes T obtenus avec des cellules dépourvues de PD-1 ou d’autres freins intracellulaires. Lorsqu’ils ont stimulé faiblement les lymphocytes T — situation destinée à imiter des tumeurs n’exprimant que de faibles quantités d’antigène — les cellules sans CISH ont produit bien plus de messagers immunitaires clés, notamment l’interféron-gamma, le TNF-alpha et l’IL‑2. Ces cellules étaient aussi plus « polyfonctionnelles », c’est-à-dire que des lymphocytes T individuels pouvaient accomplir plusieurs tâches à la fois, signe d’une forte activité anti-tumorale. En revanche, la simple suppression de PD-1 n’a pas aidé dans ces conditions de signal faible. À travers de multiples tests, la perte de CISH a stimulé plus fortement l’activation, la capacité de tuer et la formation de lymphocytes T à mémoire durable que l’inactivation d’autres points de contrôle internes candidats tels que RASA2, CBLB, SOCS1, REGNASE1, HPK1 ou PTPN1/2.
Travailler de concert avec d’autres interrupteurs internes
Étant donné que la signalisation des lymphocytes T est contrôlée par de nombreuses voies qui se recoupent, l’équipe s’est demandé si la combinaison de la suppression de CISH avec l’élimination d’autres freins pourrait produire des bénéfices additifs. En utilisant une édition CRISPR multiplex, ils ont constaté que la suppression conjointe de CISH avec SOCS1, HPK1 ou RASA2 augmentait encore la production de cytokines utiles sous stimulation faible. Dans un modèle tumoral centré sur une mutation KRAS fréquente, des lymphocytes T dotés d’un récepteur spécifique de KRAS tuaient mieux les cellules cancéreuses lorsque CISH était supprimé, et cet effet s’accentuait lorsque la perte de CISH était associée à la suppression de SOCS1 ou RASA2. Ces résultats suggèrent que CISH contrôle un nœud non redondant de la biologie des lymphocytes T et peut coopérer avec des partenaires sélectionnés pour affiner la destruction tumorale spécifique.
Renforcer les cellules CAR-T contre les tumeurs sournoises
Les auteurs se sont ensuite intéressés à un contexte cliniquement important : les cellules CAR-T ciblant le marqueur des cellules B CD19. Ils ont créé des cellules leucémiques exprimant différents niveaux de CD19 pour imiter des tumeurs qui perdent ou réduisent leurs cibles pour échapper à la thérapie. Les CAR-T privés de CISH étaient nettement meilleurs pour détruire les cellules cancéreuses, même lorsque CD19 était peu abondant, et sécrétaient davantage de signaux d’activation et de recrutement. Parallèlement, ils libéraient en moindre quantité des molécules connues pour affaiblir les lymphocytes T ou favoriser la croissance tumorale, telles que Galectin‑1, Galectin‑3, le 4‑1BB soluble, l’IL‑1α et la glycoprotéine EMMPRIN/CD147. Ensemble, ces changements indiquent des CAR‑T plus agressifs et moins facilement supprimables, particulièrement adaptés à des environnements tumoraux hostiles à faible charge antigénique.
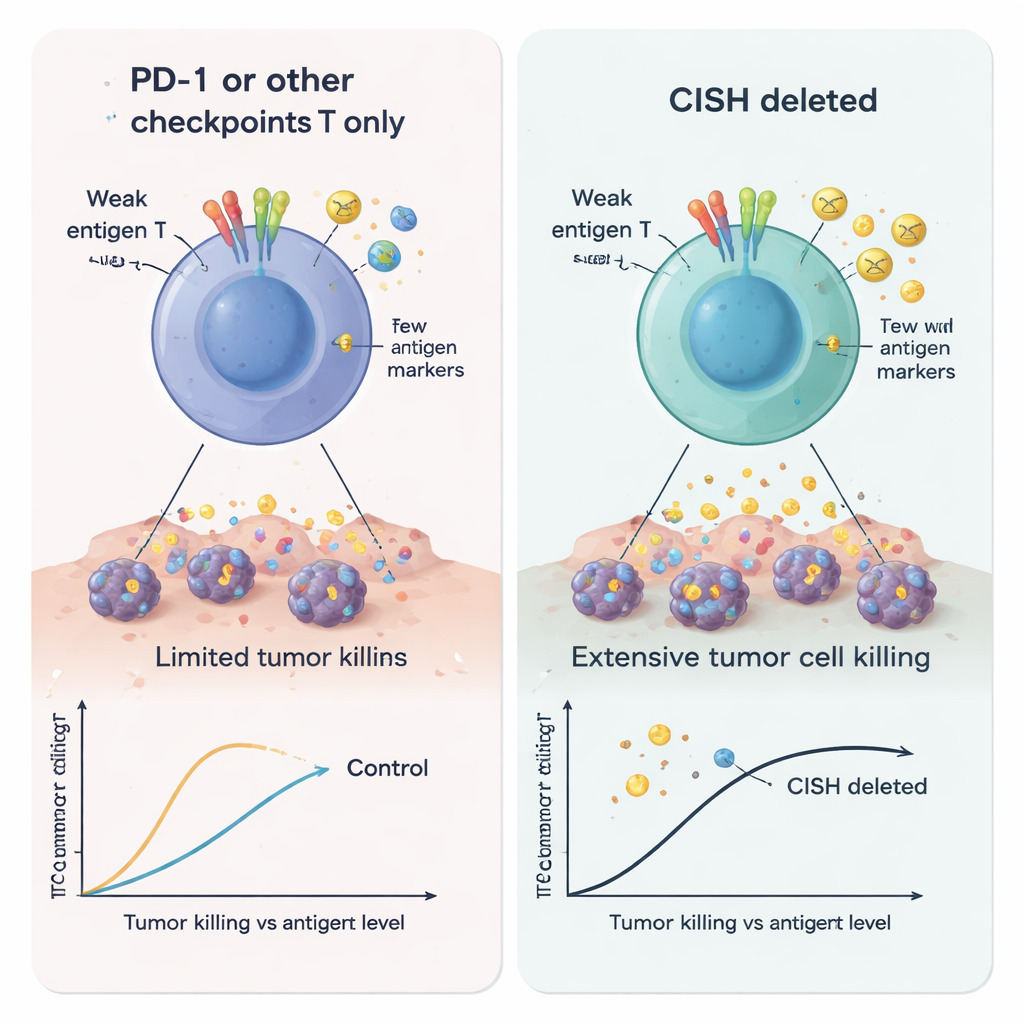
Du banc de laboratoire aux patients
Au‑delà des tubes à essai et des boîtes de culture, l’idée de cibler CISH a déjà atteint les patients. Un essai de phase I chez l’homme utilisant des lymphocytes infiltrant la tumeur édités pour supprimer CISH chez une personne atteinte d’un cancer colorectal avancé a produit une réponse complète qui a duré plus de deux ans, malgré la résistance de la tumeur à de multiples traitements antérieurs. En démontrant que CISH est un point de contrôle interne puissant et « druggable » qui augmente la sensibilité des lymphocytes T aux signaux tumoraux même faibles, cette étude aide à expliquer ce résultat clinique remarquable et soutient les efforts visant à développer des thérapies futures — qu’il s’agisse de cellules génétiquement modifiées ou de pilules — qui desserrent en toute sécurité ce frein interne et élargissent le champ de l’immunothérapie anticancéreuse.
Citation: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Mots-clés: immunothérapie du cancer, lymphocytes T, thérapie CAR-T, points de contrôle immunitaires, édition génique CRISPR