Clear Sky Science · fr
Une mutation pathogène d’α‑SNAP compromet la liaison aux lipides membranaires en cachant une boucle hydrophobe critique
Comment un tout petit changement protéique peut perturber le développement du cerveau
Les cellules cérébrales transportent en permanence des cargaisons dans de minuscules bulles appelées vésicules, et une protéine auxiliaire nommée alpha‑SNAP joue un rôle central pour que ces livraisons aboutissent. Une mutation rare d’alpha‑SNAP, connue chez une lignée de souris appelée « hyh », provoque de graves troubles de la formation du cerveau et de l’équilibre des fluides. Cette étude pose une question apparemment simple mais aux lourdes conséquences : ce changement d’une seule lettre dans alpha‑SNAP l’empêche‑t‑il de s’accrocher aux membranes cellulaires, et cela pourrait‑il être une cause majeure du dérèglement cérébral ?
Un docker cellulaire aux multiples fonctions
Alpha‑SNAP agit normalement comme une sorte de docker pour les vésicules, facilitant leur fusion avec les membranes cellulaires afin que la cargaison puisse être libérée ou recyclée. Il coopère avec un ensemble de protéines appelées SNAREs et une machine consommatrice d’énergie, NSF, pour rapprocher les membranes puis réinitialiser le système pour la tournée suivante. Au‑delà de ce rôle classique, alpha‑SNAP contribue aussi à contrôler des processus tels que l’autophagie, la mort cellulaire, l’entrée de calcium et la détection énergétique. Toutes ces fonctions dépendent, d’une manière ou d’une autre, de la capacité d’alpha‑SNAP à toucher et à s’insérer partiellement dans la surface huileuse des membranes.
Une boucle cachée et une mutation problématique
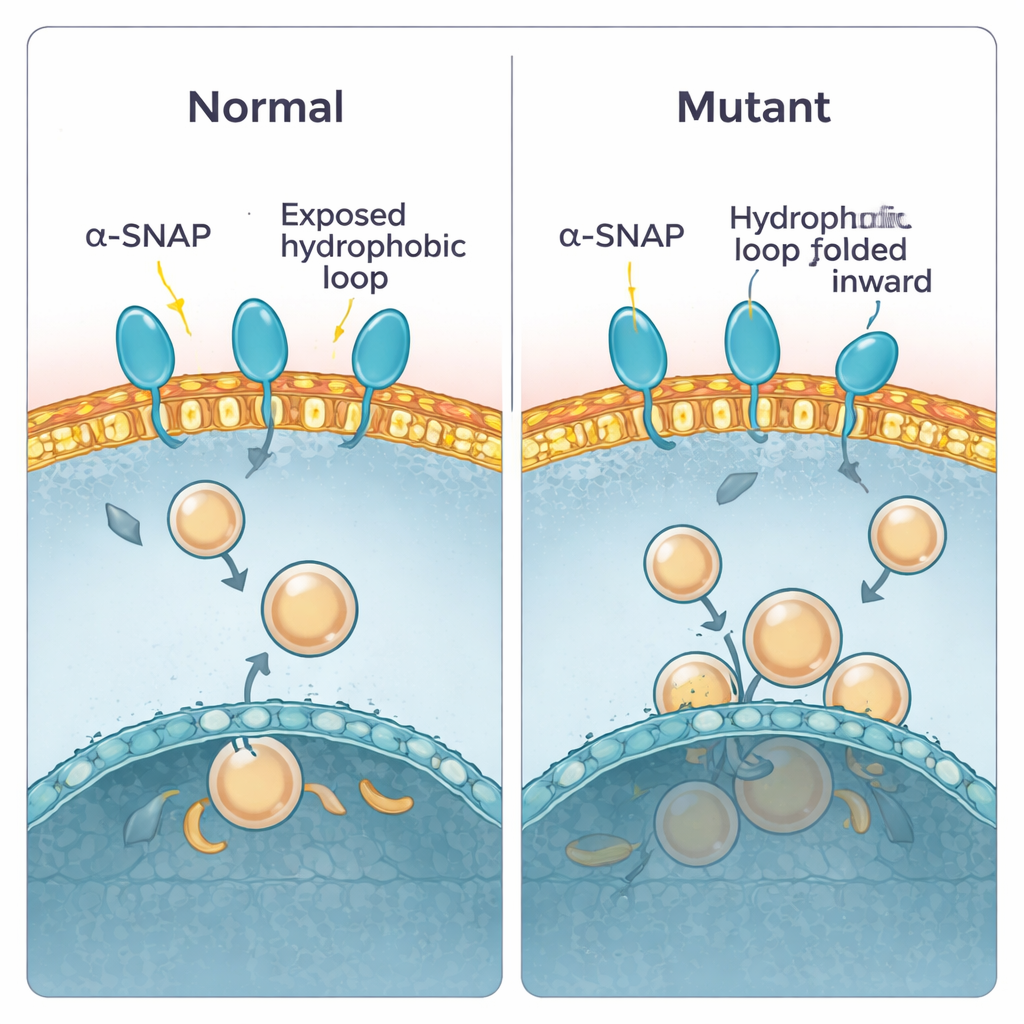
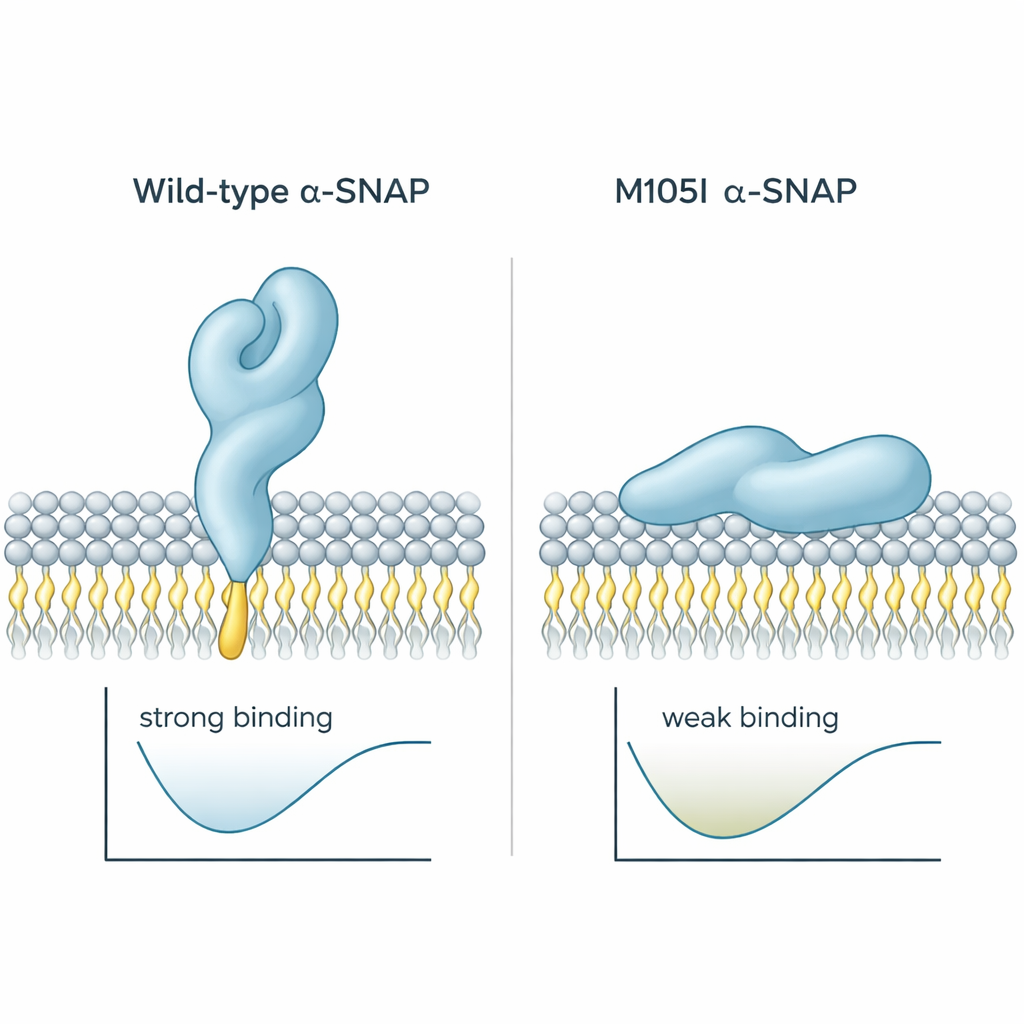
Des travaux antérieurs avaient montré qu’alpha‑SNAP utilise une courte « boucle » hydrophobe près d’une extrémité de la protéine pour s’accrocher aux membranes. Dans la protéine saine, cette boucle émerge et peut plonger dans la couche externe de la membrane. Chez la souris hyh, un seul acide aminé en position 105 est remplacé, créant la mutation M105I. Les auteurs ont utilisé des simulations informatiques pour voir comment ce changement affecte la conformation de la protéine. Ils ont constaté que la protéine mutante devient légèrement plus compacte et se tord d’une façon qui replie la boucle hydrophobe vers l’intérieur, à l’abri de l’eau et des membranes. En conséquence, la protéine mutante s’approche des membranes sous un angle plus plat et a tendance à les appuyer avec une région moins adhésive, réduisant à la fois le temps de contact et la profondeur d’insertion. Les calculs d’énergie de liaison vont dans le même sens : la protéine sauvage s’installe dans un état fortement lié et à basse énergie, tandis que la mutante privilégie des contacts plus faibles et plus superficiels.
Mettre la prédiction à l’épreuve en laboratoire
Pour vérifier ces prédictions, l’équipe a purifié l’alpha‑SNAP normale et la mutante et a testé leur comportement dans différents montages expérimentaux. D’abord, ils ont utilisé un détergent qui sépare une phase aqueuse et une phase huileuse, imitant le choix entre l’eau et la membrane. L’alpha‑SNAP normale se répartissait de façon assez équilibrée, cohérente avec une surface partiellement hydrophobe. La version mutante était moins encline à entrer dans la phase huileuse, ce qui suggère que ses parties grasses sont effectivement plus enfouies. Ensuite, ils ont laissé les protéines interagir avec des « feuilles » de membrane plasmique préparées à partir de cellules et ont imagé le nombre de sites de liaison apparus. Là encore, l’alpha‑SNAP normale ponctuait la membrane, tandis que la mutante s’y fixait beaucoup moins. Enfin, ils ont flotté des bulles membranaires artificielles (liposomes) fabriquées à partir de lipides cérébraux dans des gradients de sucre. L’alpha‑SNAP sauvage remontait avec les vésicules riches en lipides de membrane plasmique, alors que la mutante traînait derrière, se liant mal, sauf lorsque les vésicules étaient constituées d’un mélange membranaire plus interne.
Conséquences dans le cerveau en développement
Les chercheurs se sont ensuite tournés vers des cerveaux d’embryons de souris en développement, en se concentrant sur une étape où de nouveaux neurones naissent. En séparant le contenu cellulaire en pools soluble et lié aux membranes, ils ont montré que les niveaux totaux d’alpha‑SNAP étaient déjà réduits dans les cerveaux hyh, mais, plus important encore, la fraction attachée aux membranes était disproportionnellement faible comparée aux souris normales. En séparant encore différents types de membranes, ils ont constaté que la perte la plus marquée concernait la membrane plasmique, la surface externe de la cellule, tandis que les membranes internes étaient beaucoup moins affects. La microscopie racontait la même histoire : dans les tissus normaux, l’alpha‑SNAP soulignait les cellules sous la forme d’un motif en nid d’abeille correspondant à un marqueur de surface connu. Dans les cerveaux hyh, ce marquage net en bordure s’estompe pour devenir une lueur plus diffuse et interne, indiquant que la protéine mutante ne reste pas ancrée en périphérie cellulaire, là où la fusion des vésicules et la signalisation sont les plus actives.
Pourquoi cela a de l’importance pour la maladie
En somme, le travail montre que la mutation M105I fait plus que réduire simplement la quantité d’alpha‑SNAP ; elle modifie le repliement de la protéine de sorte que sa boucle d’accrochage membraneux est dissimulée. Cela rend plus difficile pour alpha‑SNAP d’agripper la membrane plasmique et d’adopter l’orientation adéquate pour organiser la machinerie de fusion. Dans un cerveau en développement, où la livraison précise de signaux et de matériaux à la surface cellulaire est essentielle, ce défaut structural subtil contribue probablement à l’hydrocéphalie, au cortex mal câblé et aux autres anomalies observées chez les souris hyh. Pour les non‑spécialistes, le message est clair : même un tout petit changement dans la conformation d’une seule protéine peut remodeler la communication cellulaire et, par conséquent, la construction du cerveau.
Citation: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Mots-clés: alpha-SNAP, liaison à la membrane, mutation protéique, développement cérébral, fusion de vésicules