Clear Sky Science · fr
La voie perforante et les afférences CA3–collatérales de Schaffer se coordonnent pour réguler l’apprentissage spatial
Pourquoi savoir s’orienter compte
Qu’il s’agisse d’une souris cherchant une plateforme cachée ou d’une personne se repérant dans une nouvelle ville, le cerveau transforme en permanence les vues, les sons et les mouvements du corps en une carte interne. Cette étude examine comment deux régions cérébrales clés, le cortex entorhinal et l’hippocampe, coopèrent pour soutenir cette capacité. En observant l’activité en direct de fibres nerveuses minuscules et en stimulant ou en silencant avec précision des voies spécifiques chez la souris, les chercheurs dévoilent comment ces zones se coordonnent pour former et stabiliser les souvenirs spatiaux — des éléments qui pourraient à terme aider à comprendre et traiter les troubles de la mémoire.
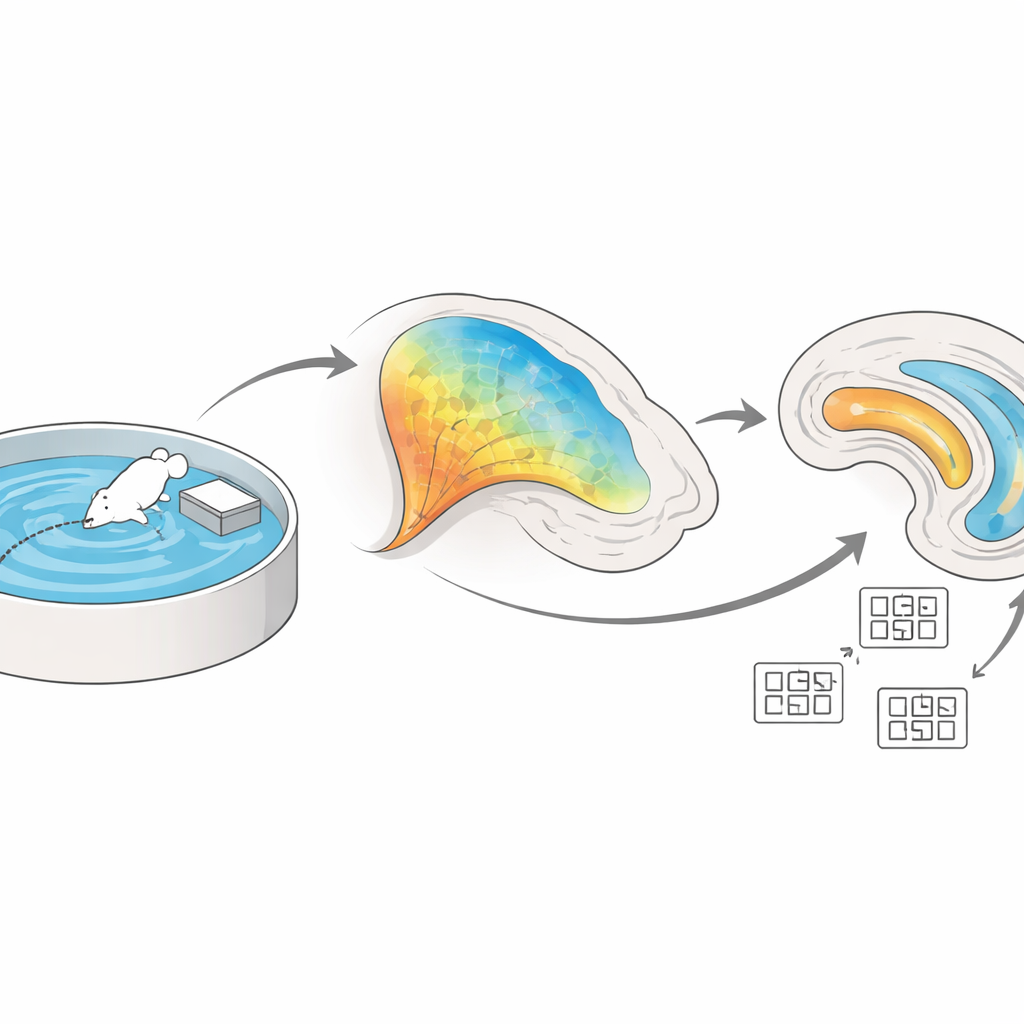
Deux pôles clés du GPS interne du cerveau
L’hippocampe et le cortex entorhinal adjacent se situent profondément dans le lobe temporal et constituent le cœur de notre système de navigation. Dans l’hippocampe, un circuit interne relie une zone appelée CA3 à une autre appelée CA1 via des fibres connues sous le nom de collatérales de Schaffer. En parallèle, le cortex entorhinal envoie un flux distinct d’informations directement vers CA1 via la voie dite perforante. Les auteurs ont cherché à déterminer comment ces deux flux d’entrée coopèrent lorsqu’un animal apprend la configuration d’un espace, et comment les modifications à leurs connexions — désignées globalement sous le terme de « plasticité » — soutiennent la construction d’une carte spatiale stable.
Observer l’apprentissage fibre par fibre
Pour suivre ce processus chez des animaux en comportement, l’équipe a utilisé la photométrie par fibre, une technique qui rend compte de l’activité nerveuse par des éclairs de lumière fluorescente. Ils ont modifié génétiquement des souris pour que les neurones CA3 projetant vers CA1 s’éclairent lorsqu’ils sont actifs, puis ont entraîné les animaux au labyrinthe aquatique de Morris, un test classique où la souris doit apprendre la position cachée d’une petite plateforme dans une piscine. Lors des premières épreuves, les fibres CA3–CA1 étaient fortement actives pendant que les animaux cherchaient ; à mesure que les souris devenaient efficaces et trouvaient la plateforme plus rapidement, cette activité diminuait progressivement. Le schéma suggère que ces connexions sont particulièrement engagées pendant que le cerveau encode d’abord la configuration de l’environnement, puis s’établissent dans une représentation plus efficiente et stable une fois la mémoire formée.
Comment l’entrée en amont renforce ou atténue l’apprentissage
Les scientifiques se sont ensuite demandé comment les signaux provenant du cortex entorhinal influencent ce circuit hippocampique. En utilisant des protéines sensibles à la lumière pour activer les neurones entorhininaux tout en enregistrant l’activité des fibres CA3–CA1, ils ont montré que stimuler l’entrée depuis le cortex entorhinal médial augmentait de façon fiable l’activité de ces connexions hippocampiques. À l’inverse, lorsque l’on a affaibli chimiogénétiquement les signaux entorhininaux arrivant dans CA1 durant l’entraînement au labyrinthe aquatique, l’activité CA3–CA1 a diminué et les souris ont appris l’emplacement de la plateforme plus lentement et avec moins de précision. Dans une série complémentaire d’expériences, les auteurs ont enregistré directement l’activité des neurones entorhininaux qui projettent vers CA1 et ont observé que leur activité augmentait au fil des jours d’entraînement, reflétant l’amélioration de la performance des animaux. Ensemble, ces résultats indiquent que des signaux entorhininaux forts et bien synchronisés sont nécessaires pour régler correctement les circuits hippocampiques en vue de la navigation.
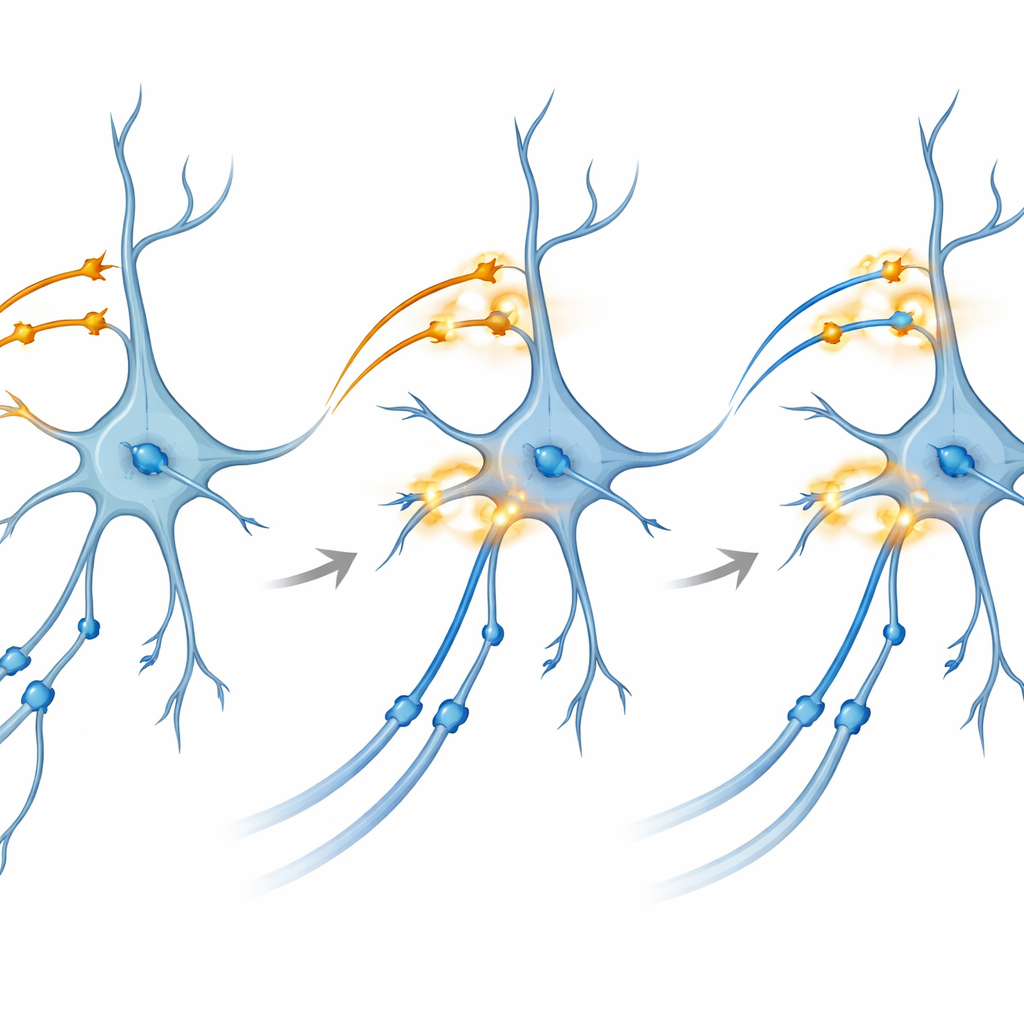
Approfondir comment les connexions se renforcent
Pour sonder le mécanisme sous-jacent, l’équipe s’est tournée vers des coupes de cerveau maintenues en vie en milieu de culture. Là, ils pouvaient contrôler séparément des protéines activées par la lumière dans CA3 et les entrées entorhinales vers CA1. De manière surprenante, une stimulation lumineuse en rafales de type thêta — des schémas qui imitent le rythme naturel de décharge — appliquée à l’une ou l’autre voie seule ne produisait pas de façon fiable une potentialisation à long terme, le renforcement durable des synapses supposé sous-tendre la mémoire. En revanche, lorsqu’ils ont délivré une rafale bichromatique soigneusement synchronisée qui co‑activait les deux voies sur CA1 en même temps, les connexions CA3–CA1 présentaient un renforcement robuste et durable. Le blocage des récepteurs NMDA ou de canaux calciques spécifiques, deux verrous moléculaires bien connus de la plasticité, empêchait cet effet, reliant le phénomène aux voies biochimiques classiques de la formation de la mémoire.
Ce que cela signifie pour la mémoire et la maladie
Dans l’ensemble, l’étude dessine le portrait de l’apprentissage spatial comme une danse coordonnée entre les signaux entorhininaux entrants et le câblage interne de l’hippocampe. Les entrées entorhinales transportent non seulement des informations sur la position et le contexte ; elles agissent aussi comme un bouton de commande puissant qui peut amplifier ou atténuer l’activité des fibres CA3–CA1 et, lorsqu’elles sont co‑activées, provoquer un renforcement à long terme de ces synapses. Pour un lecteur non spécialiste, l’idée principale est que le « GPS » du cerveau ne dépend pas d’une seule région, mais d’un partenariat où l’une pose le décor et l’autre verrouille les détails. Les perturbations de ce partenariat — qu’elles résultent du vieillissement, d’une lésion ou d’une maladie neurodégénérative — pourraient donc aider à expliquer pourquoi certaines personnes se perdent dans des lieux familiers, et cibler ces voies pourrait offrir de nouvelles pistes pour préserver ou restaurer la mémoire spatiale.
Citation: Huang, F., Temitayo Bello, S., Lau, S.H. et al. The perforant pathway and CA3-Schaffer collateral afferents coordinate to regulate spatial learning. Commun Biol 9, 364 (2026). https://doi.org/10.1038/s42003-026-09577-z
Mots-clés: mémoire spatiale, hippocampe, cortex entorhinal, plasticité synaptique, navigation