Clear Sky Science · fr
Développement de ligands de prohibitine dérivés de la capsaïcine pour moduler l’interaction Aurora kinase A/PHB2 et la mitophagie dans les cellules cancéreuses
Pourquoi une molécule de piment importe pour le cancer
Les piments doivent leur brûlure à la capsaïcine, une petite molécule qui se fixe sur des protéines de nos cellules. Cette étude explore un tournant surprenant autour de cette épice familière : les chercheurs ont repensé la capsaïcine pour créer de nouvelles molécules de type médicament qui ciblent les « centrales » des cellules cancéreuses — les mitochondries — et modulent un processus que ces cellules utilisent pour maintenir leurs usines énergétiques en bon état. Parce que les cellules cancéreuses dépendent fortement de mitochondries efficaces pour alimenter leur croissance incontrôlée, pouvoir perturber sélectivement ce système de soutien pourrait ouvrir une nouvelle voie pour des thérapies anticancéreuses.
Les centrales cellulaires et leur équipe de nettoyage interne
Les mitochondries équilibrent en permanence la fabrication de nouvelles unités et le recyclage des unités endommagées. Le volet recyclage, appelé mitophagie, fonctionne comme un système de contrôle qualité : les mitochondries usées sont marquées et démantelées, tandis que les plus saines sont conservées. De nombreuses cellules cancéreuses détournent cet équilibre, utilisant la mitophagie pour éliminer les mitochondries faibles et enrichir des « super-performantes » qui produisent de grandes quantités d’ATP, la monnaie énergétique de la cellule. Une protéine nommée Aurora kinase A (AURKA), souvent surproduite dans les tumeurs, a récemment été trouvée à l’intérieur des mitochondries où elle s’associe à une autre protéine, Prohibitin‑2 (PHB2), et à l’adaptateur de l’autophagie LC3. Ensemble, elles forment un complexe qui favorise la mitophagie et soutient une production énergétique élevée dans les cellules cancéreuses.
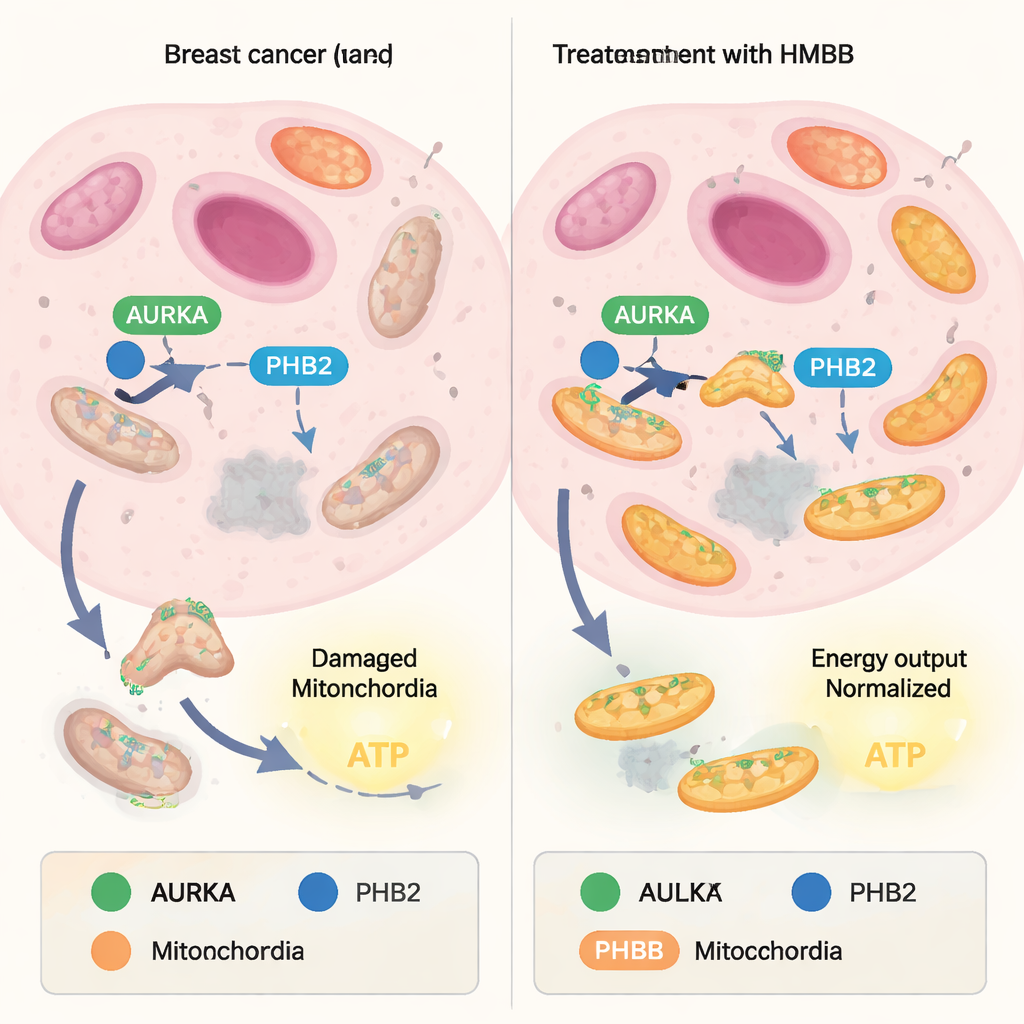
De la capsaïcine épicée aux outils moléculaires sur mesure
Des travaux antérieurs avaient montré qu’un composé naturel appelé xanthohumol peut se lier à PHB2 et perturber le complexe AURKA–PHB2–LC3, bloquant la mitophagie et réduisant la production d’ATP mitochondriale. Cependant, la structure chimique du xanthohumol n’est pas idéale pour le développement pharmaceutique. Dans cette étude, les auteurs se sont intéressés à la capsaïcine, un autre ligand naturel de PHB, et ont vérifié si elle pouvait être remodelée en outils plus pratiques. Ils ont d’abord confirmé que la capsaïcine affaiblit légèrement l’interaction entre AURKA et PHB2 dans des cellules mammaires cancéreuses vivantes, en utilisant une technique d’imagerie (FRET/FLIM) qui mesure la proximité entre deux protéines marquées. Ils ont ensuite synthétisé 16 molécules inspirées de la capsaïcine en modifiant la « queue » et la « tête » aromatique de la structure originale, et ont testé systématiquement comment chaque version affectait le partenariat AURKA–PHB2 à l’intérieur des mitochondries.
Découverte d’une « colle » moléculaire qui verrouille les protéines
Les molécules modifiées ont eu des effets très différents. Certaines, comme la capsaïcine elle-même ou un dérivé appelé composé 5, facilitaient la séparation d’AURKA et de PHB2. D’autres n’avaient presque aucun effet. Un sous-ensemble, cependant — en particulier une molécule nommée composé 13, ensuite appelée HMBB — avait l’effet inverse et renforçait significativement la liaison entre AURKA et PHB2. Des simulations de docking informatiques ont aidé à expliquer ce comportement. La capsaïcine et le composé 5 avaient tendance à s’insérer dans le site actif d’AURKA de manières qui provoquaient des conflits physiques avec PHB2, poussant les deux protéines à se séparer. En revanche, les composés 12 et 13 se logeaient dans le site actif d’AURKA tout en contactant simultanément une poche inhibitrice connue sur PHB2 sans créer de conflit. Leurs formes leur permettaient d’agir comme une « colle moléculaire », faisant le pont entre AURKA et PHB2 et stabilisant le complexe.
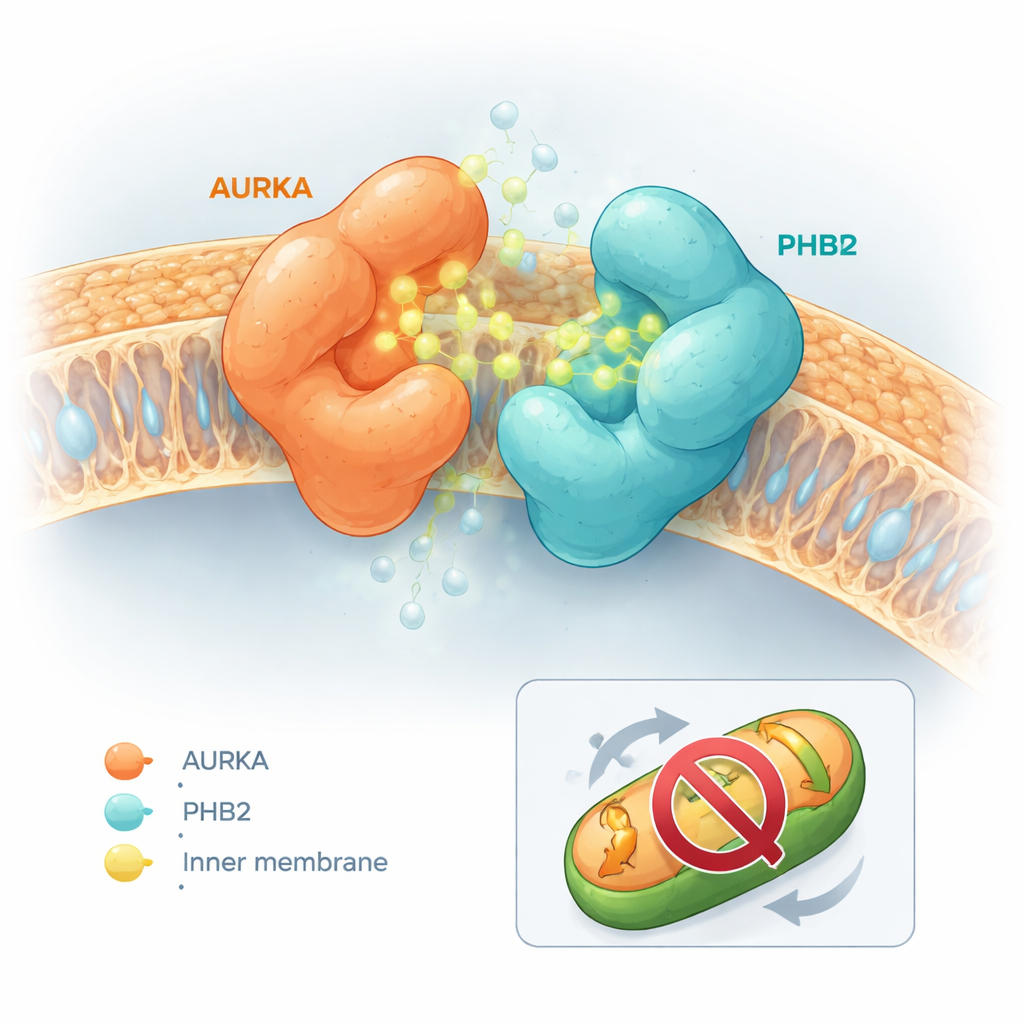
Bloquer le nettoyage mitochondrial sans éteindre le centre de contrôle de la cellule
Une question cruciale était de savoir si ce comportement de colle moléculaire désactivait simplement AURKA partout dans la cellule — ce qui exposerait à des effets indésirables larges — ou s’il était plus sélectif. En utilisant un biosenseur fluorescent distinct qui rend compte de l’activation d’AURKA au niveau des centrosomes — les structures qui organisent la machinerie de division cellulaire — l’équipe a observé que HMBB n’atténuait pas l’activité d’AURKA à ces sites. Pourtant, dans des essais mitochondriaux, HMBB a inversé la perte de masse mitochondriale normalement causée par la surexpression d’AURKA dans des cellules mammaires cancéreuses. Dans des cellules qui expriment naturellement des niveaux élevés d’AURKA, HMBB a augmenté le contenu mitochondrial, indiquant que la mitophagie induite par AURKA était bloquée. Dans des cellules à faibles niveaux d’AURKA, HMBB a eu peu d’impact, soulignant sa dépendance à la voie AURKA–PHB2.
Ce que cela pourrait signifier pour de futurs traitements du cancer
Pris ensemble, les résultats montrent que des dérivés de la capsaïcine soigneusement conçus peuvent affiner la façon dont AURKA et PHB2 interagissent dans les mitochondries. En agissant comme une colle moléculaire, HMBB et des composés apparentés verrouillent AURKA et PHB2 dans une configuration qui empêche le déroulement du programme habituel de mitophagie, sans inhiber les rôles essentiels d’AURKA ailleurs dans la cellule. Pour le lecteur non spécialiste, l’idée principale est que les auteurs ont créé des molécules prototypes qui interfèrent sélectivement avec la façon dont les cellules cancéreuses maintiennent leurs centrales énergétiques en bon état, affaiblissant potentiellement leur approvisionnement en énergie tout en épargnant les fonctions normales des cellules. Bien que ces composés soient encore à un stade précoce, en laboratoire, ils illustrent une stratégie prometteuse : utiliser de petites molécules de type médicament pour cibler des partenariats protéiques spécifiques à l’intérieur des mitochondries et, ce faisant, saper les avantages métaboliques dont dépendent de nombreuses tumeurs.
Citation: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Mots-clés: mitochondries, mitophagie, Aurora kinase A, dérivés de la capsaïcine, métabolisme du cancer