Clear Sky Science · fr
Une signature radiopathomique par apprentissage profond prédit le risque de récidive du carcinome hépatocellulaire après hépatectomie
Pourquoi cela compte pour les personnes atteintes d’un cancer du foie
Le cancer du foie fait partie des cancers les plus meurtriers dans le monde, et même lorsque les chirurgiens retirent la tumeur visible, beaucoup de patients voient la maladie réapparaître en seulement quelques années. Cette étude présente un outil d’intelligence artificielle qui combine les examens d’imagerie et les lames de microscope des tumeurs pour mieux prévoir qui est susceptible de connaître une récidive du carcinome hépatocellulaire, la forme la plus courante de cancer du foie. De telles prédictions pourraient aider les médecins à adapter le suivi et les traitements complémentaires, dans le but de prévenir la récidive et d’allonger la vie des patients.
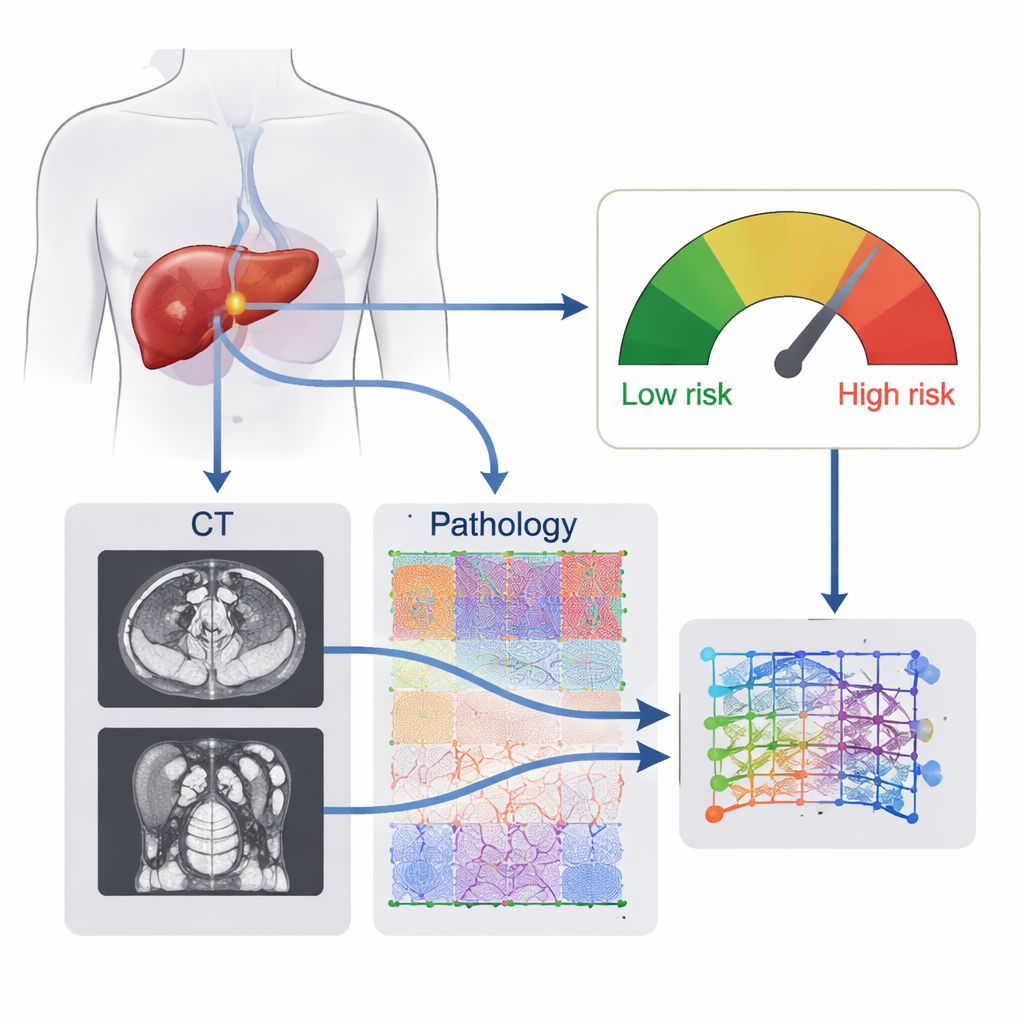
Voir la tumeur dans son ensemble, de l’extérieur et de l’intérieur
Les médecins s’appuient généralement sur les scanners (CT), les analyses sanguines et les rapports de pathologie de base pour estimer le risque de récidive après une chirurgie du foie. Chacun de ces outils examine la tumeur sous un angle différent, mais aucun ne saisit pleinement sa complexité. Les images CT montrent la forme globale de la tumeur, son irrigation sanguine et sa relation avec le foie, tandis que les lames au microscope révèlent l’apparence agressive des cellules cancéreuses et leurs interactions avec le tissu environnant. Les chercheurs ont supposé qu’un système informatique qui « regarde » les deux niveaux simultanément — images à l’échelle de l’organe et images à l’échelle cellulaire — pourrait reconnaître des motifs que l’œil humain ne perçoit pas et prédire plus précisément si le cancer va revenir.
Une empreinte numérique combinée de la tumeur
L’équipe a développé ce qu’elle appelle une signature radiopathomique par apprentissage profond (DLRP), essentiellement une empreinte numérique de la tumeur de chaque patient construite à partir de deux sources de données. D’abord, un réseau neuronal a automatiquement délimité les tumeurs sur les scans CT préopératoires et a appris des caractéristiques d’image subtiles liées à la récidive. Ensuite, un autre réseau a analysé des lames entières de tissu teintées à l’hématoxyline-éosine, les découpant en milliers de petits patchs et apprenant quels motifs microscopiques importaient le plus. Un module de fusion a alors tissé ensemble les caractéristiques CT et les caractéristiques de pathologie en un score de risque unique qui reflète le comportement de la tumeur plutôt qu’un seul trait visible.
Tester le score chez de vrais patients
Les chercheurs ont appliqué ce système à 599 personnes ayant subi une intervention pour carcinome hépatocellulaire dans quatre hôpitaux, en les répartissant en ensembles d’entraînement et de test indépendants. Sur tous les jeux de test, la signature DLRP a prédit la survie sans récidive mieux que des modèles utilisant uniquement le CT, uniquement la pathologie, des variables cliniques standard comme la taille de la tumeur et les marqueurs sanguins, ou le stade largement utilisé du Barcelona Clinic Liver Cancer. Les patients avec des scores DLRP élevés avaient une probabilité nettement plus grande de voir la tumeur réapparaître et une survie globale plus courte. Fait important, cela demeurait vrai dans de nombreux sous-groupes, y compris ceux avec des tumeurs petites versus grosses, uniques versus multiples, et avec ou sans cirrhose, ce qui suggère que le score saisit des aspects fondamentaux de l’agressivité tumorale.
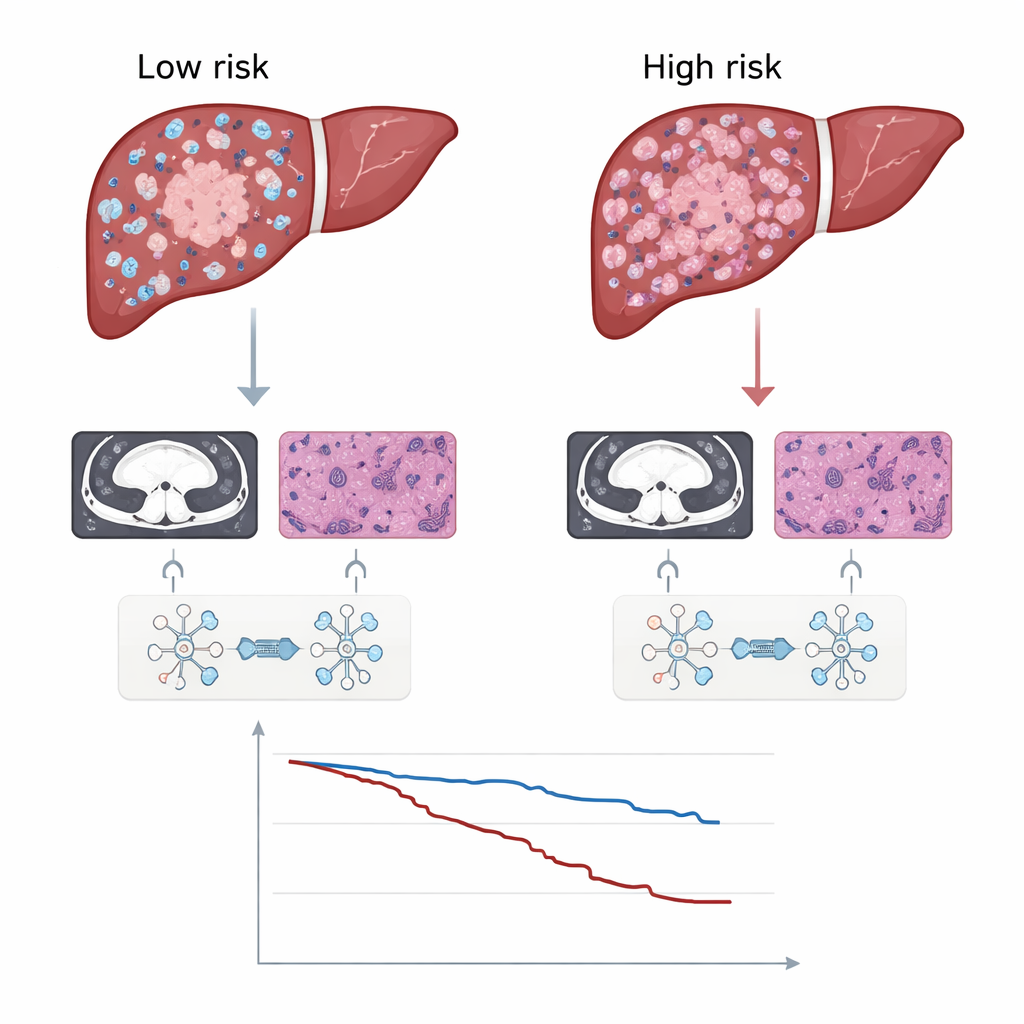
Orienter des traitements complémentaires et révéler la biologie
Au-delà de la prédiction, le score a aidé à identifier quels patients pourraient bénéficier d’une procédure supplémentaire appelée chimioembolisation artérielle postopératoire adjuvante (PA-TACE), dans laquelle une chimiothérapie mélangée à un agent de contraste huileux est injectée dans l’apport sanguin du foie. Parmi tous les patients réunis, ceux ayant reçu une PA-TACE avaient tendance à rester plus longtemps sans récidive. Mais lorsque le groupe a été divisé selon la signature DLRP, le bénéfice se concentrait presque entièrement chez les patients à haut risque ; les patients à faible risque ne montraient pas d’avantage net, ce qui suggère qu’ils pourraient éviter en toute sécurité les contraintes d’un traitement supplémentaire. L’équipe a également exploré pourquoi les tumeurs à haut risque se comportent plus mal en reliant les scores DLRP à des données génétiques issues de The Cancer Genome Atlas. Les scores élevés étaient associés à l’activation de la voie Wnt/β-caténine, connue pour favoriser la croissance tumorale et la résistance à l’immunothérapie, et à une moindre infiltration de cellules immunitaires anti-cancer, en particulier des lymphocytes T CD8, dans la tumeur.
Ce que cela signifie pour la prise en charge future du cancer du foie
Pour un non-spécialiste, la conclusion est que les ordinateurs peuvent désormais fusionner des images de type radiographique et des vues microscopiques pour produire un nombre unique qui indique la probabilité qu’un cancer du foie réapparaisse après la chirurgie. Cette étude montre qu’un tel chiffre peut surpasser les systèmes de stadification traditionnels et aider à décider qui a vraiment besoin de traitements complémentaires et d’un suivi plus intensif. Bien que l’outil doive encore être testé prospectivement dans des populations de patients plus larges, notamment ceux dont la maladie hépatique n’est pas causée par l’hépatite B, il ouvre la voie à un avenir où les plans de traitement sont façonnés par des portraits riches et multicouches de la tumeur de chaque personne plutôt que par la seule taille et le stade.
Citation: Wang, G., Chen, W., Liang, Z. et al. A deep learning radiopathomic signature predicts recurrence risk of hepatocellular carcinoma after hepatectomy. Commun Biol 9, 295 (2026). https://doi.org/10.1038/s42003-026-09571-5
Mots-clés: carcinome hépatocellulaire, récurrence du cancer du foie, apprentissage profond, imagerie médicale, microenvironnement tumoral