Clear Sky Science · fr
Réévaluation de la spécificité protéine Gα–élément de réponse dans la signalisation GPCR
Pourquoi ces petits interrupteurs cellulaires comptent pour la médecine
Nombre des médicaments actuels agissent en activant des « interrupteurs » moléculaires à la surface de nos cellules appelés récepteurs couplés aux protéines G, ou GPCR. Ces interrupteurs transmettent des messages vers l’intérieur de la cellule via des protéines d’aide appelées protéines G et aboutissent finalement à l’activation ou à la répression de gènes. Pendant des décennies, les chercheurs ont utilisé des tests simples produisant de la lumière pour identifier quelles protéines G sont engagées par un médicament ou un récepteur donné. Cette étude pose une question simple mais cruciale : ces tests nous disent‑ils vraiment ce que nous croyons — et peut‑on encore leur faire confiance lors de la conception de la prochaine génération de médicaments de précision ?
Comment les scientifiques lisent habituellement les signaux GPCR
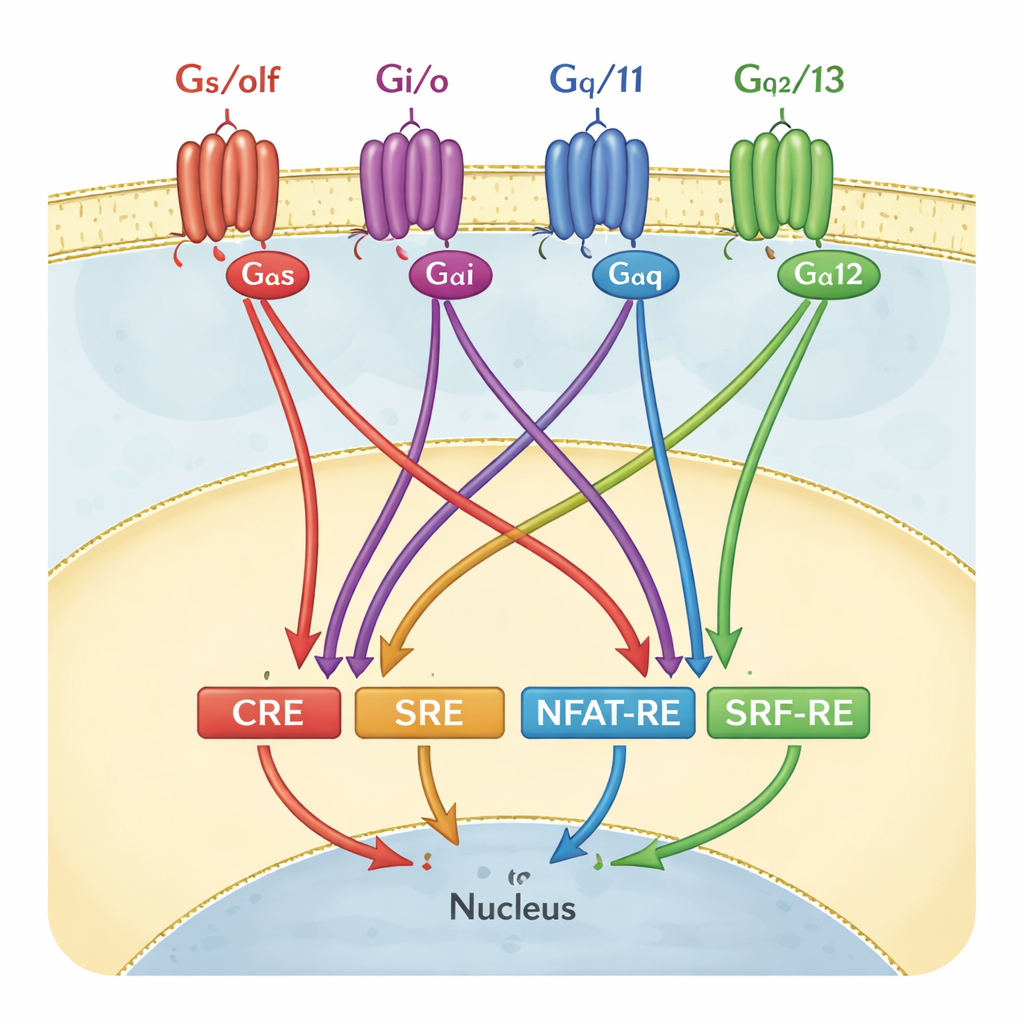
Pour suivre l’activité des GPCR, de nombreux laboratoires utilisent des tests de gènes rapporteurs. Dans ces essais, les cellules sont modifiées de sorte que lorsqu’un commutateur génétique particulier, ou « élément de réponse », est activé, les cellules émettent de la lumière. Quatre de ces éléments sont particulièrement populaires : CRE, SRE, NFAT‑RE et SRF‑RE. Chacun a longtemps été considéré comme le substitut d’une branche de la signalisation via les protéines G — par exemple CRE pour la famille Gαs/olf, ou SRF‑RE pour Gα12/13. Dans les manuels et les pipelines de criblage, ces appariements sont souvent représentés presque comme des schémas de câblage un à un : activer une protéine G spécifique et un seul rapporteur s’allume.
Mettre l’ancien schéma de câblage à l’épreuve
Les auteurs ont remis en cause ce tableau de façon systématique en utilisant des cellules humaines HEK293 dans lesquelles des familles spécifiques de protéines G — voire toutes les protéines G — ont été supprimées par édition du génome. Ils ont ensuite réintroduit des types individuels de protéines G, un par un. Dans ces cellules, ils ont exprimé neuf GPCR différents, choisis pour représenter des récepteurs signalant de manière très sélective ou via de nombreux partenaires protéine G. En mesurant l’intensité d’émission des quatre rapporteurs à travers de nombreuses concentrations de médicament, ils ont pu déterminer quelles protéines G étaient réellement nécessaires pour chaque élément de réponse et lesquelles pouvaient participer de façon indirecte.
Des voies qui se chevauchent plutôt que des canaux propres
Les résultats renversent le modèle net « un récepteur‑un rapporteur ». Si le CRE dépendait toujours principalement des protéines Gαs/olf — la voie classique d’élévation de l’AMPc — d’autres familles de protéines G pouvaient notablement influencer l’activité du CRE, mais seulement en présence de Gαs/olf. Pour les trois autres rapporteurs, SRE, NFAT‑RE et SRF‑RE, la famille Gαq/11 est apparue comme le principal moteur, même si SRE et SRF‑RE étaient traditionnellement liés à d’autres branches des protéines G. SRE et SRF‑RE se comportaient de manière particulièrement similaire, suggérant qu’ils exploitent une machinerie en aval commune plutôt que des voies distinctes et isolées. Dans de nombreux cas, des protéines G supplémentaires telles que Gα12/13 et Gαi/o fournissaient un soutien additionnel ou une activité de fond, mettant en évidence un réseau d’interférences plutôt que des canaux séparés.
Pourquoi le réseau cellulaire brouille nos mesures
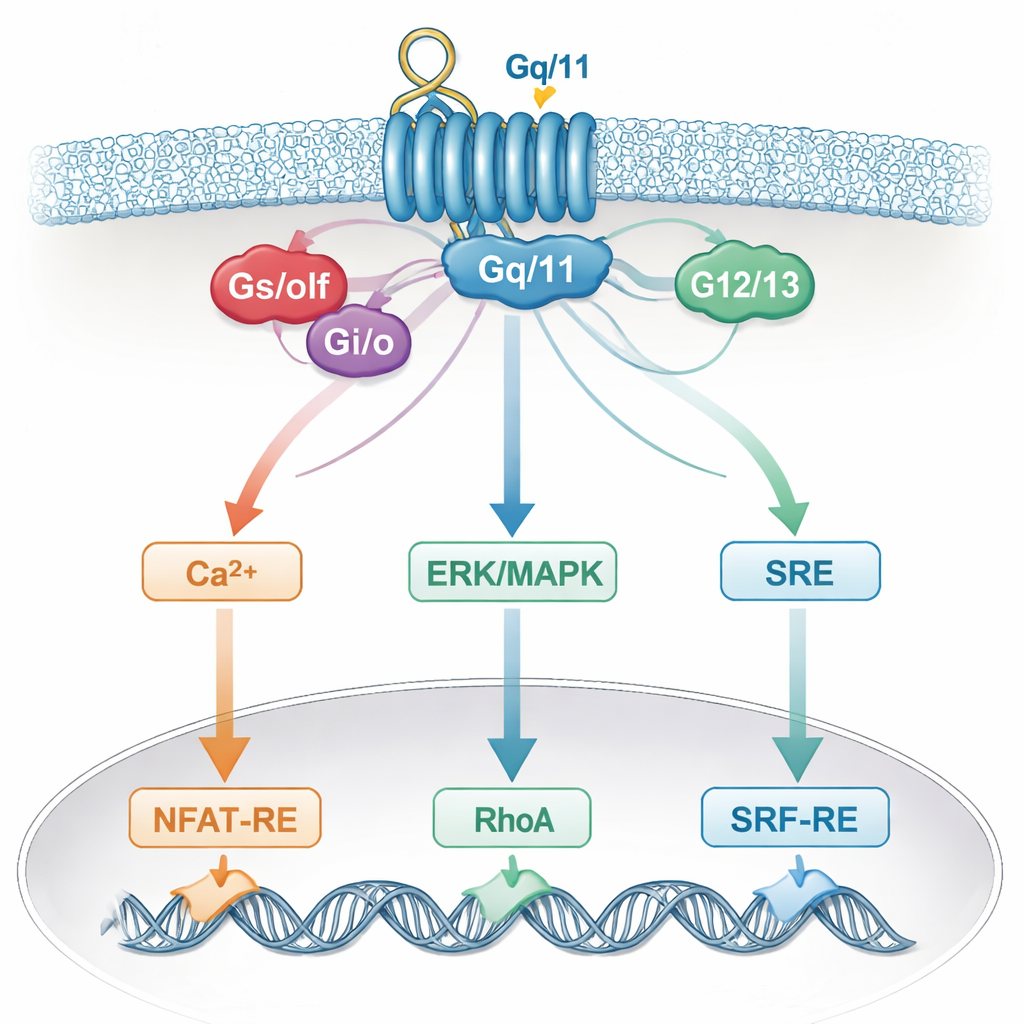
Cette spécificité floue reflète probablement la façon dont les cellules réelles intègrent les signaux. Un unique récepteur peut activer plusieurs protéines G, qui convergent ensuite sur des messagers communs comme le calcium, ERK/MAPK, RhoA ou l’AMPc, et sur des aides partagées telles que les sous‑unités Gβγ. Ces voies communes alimentent à leur tour les mêmes commutateurs géniques dans le noyau. Par conséquent, un rapporteur que l’on pensait répondre à une seule famille de protéines G « écoute » en fait plusieurs. Des facteurs spécifiques au type cellulaire et l’ensemble exact de récepteurs présents ajoutent encore de la complexité, ce qui signifie que des conclusions tirées d’un système cellulaire peuvent ne pas être valables dans un autre.
Ce que cela implique pour la découverte de médicaments
Pour les non‑spécialistes, la conclusion principale est que nombre de tests GPCR basés sur l’émission de lumière sont moins spécifiques que leur étiquette ne le suggère. Ils peuvent néanmoins indiquer qu’un récepteur est actif et, de manière approximative, quelles grandes voies sont engagées, mais ils ne constituent pas une preuve fiable qu’une famille de protéines G particulière — et uniquement cette famille — est impliquée. Les auteurs recommandent que les chercheurs et les développeurs pharmaceutiques considèrent ces rapporteurs comme des indicateurs grossiers et les associent à des méthodes plus directes qui observent les interactions protéiques en temps réel. Cela donnera une image plus fidèle de la manière dont des médicaments potentiels orientent la signalisation cellulaire et aidera à éviter des raccourcis trompeurs dans la recherche de thérapies plus sûres et plus ciblées.
Citation: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Mots-clés: Signalisation GPCR, Protéines G, tests rapporteurs, réseaux de signalisation cellulaire, découverte de médicaments