Clear Sky Science · fr
HBP1 amplifie l’activité du récepteur à la progestérone et l’expression d’IGFBP1, stimulant la décidualisation de l’endomètre
Pourquoi cela compte pour la fertilité
Quand une grossesse débute, l’embryon ne peut s’implanter dans l’utérus que si la muqueuse utérine a subi une transformation essentielle appelée décidualisation. De nombreux cas d’infertilité et d’échecs répétés de transfert d’embryon restent inexpliqués, et des preuves croissantes suggèrent que le problème se situe dans cette transformation plutôt que dans l’embryon lui‑même. Cette étude révèle un « interrupteur » moléculaire jusque‑là sous‑estimé, un facteur de transcription nommé HBP1, qui aide à préparer l’endomètre à l’implantation et pourrait offrir de nouvelles voies pour diagnostiquer et traiter les troubles d’implantation.
Un interrupteur caché dans la muqueuse utérine
La couche interne de l’utérus, l’endomètre, change rythmiquement à chaque cycle menstruel. Sous l’influence des œstrogènes il croît, et sous celle de la progestérone il mûrit pour devenir un site réceptif à l’embryon. Dans ce travail, les chercheurs se sont concentrés sur les cellules stromales endométriales humaines, les cellules structurelles qui se transforment en cellules déciduelles plus grandes et plus sécrétrices au moment de l’implantation. En exploitant des données d’expression génique existantes et en réalisant de nouvelles expériences, ils ont constaté que les niveaux de HBP1 augmentent fortement lorsque ces cellules stromales commencent à se décidualiser, ce qui suggère que HBP1 fait partie du système temporel intégré qui prépare l’utérus.
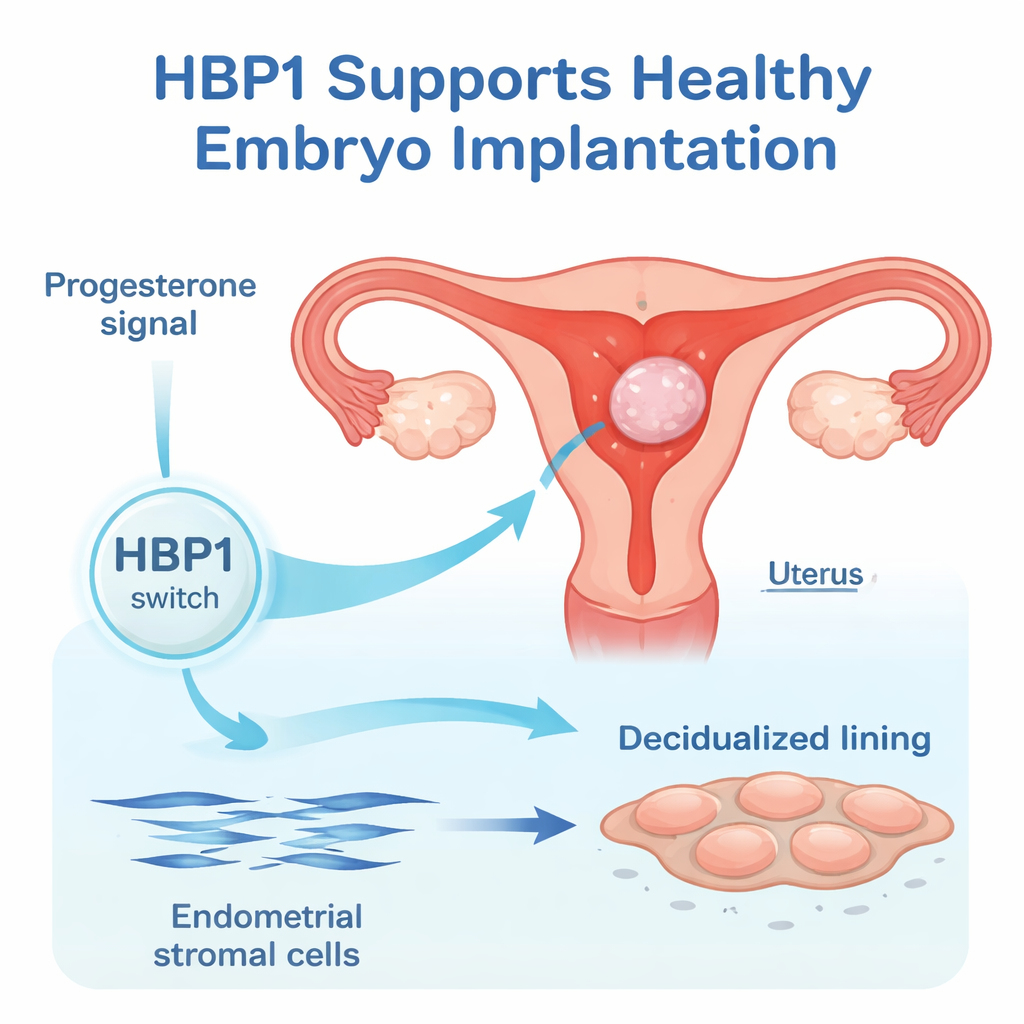
Favoriser le changement de forme et le ralentissement cellulaire
Pour déterminer si HBP1 est simplement présent ou réellement nécessaire, l’équipe a modulé son expression à la hausse et à la baisse dans des cellules stromales endométriales humaines en culture. Lorsque HBP1 était réduit, des marqueurs classiques de la décidualisation tels qu’IGFBP1, FOXO1 et la prolactine diminuaient au niveau de l’ARN et de la protéine. Les cellules n’ont pas non plus effectué le changement de forme typique — de cellules fines et fusiformes vers des cellules plus larges et polygonales — et ont continué à proliférer. À l’inverse, l’augmentation de HBP1 élevait les niveaux d’IGFBP1 et ralentissait la division cellulaire. Ces résultats montrent que HBP1 aide les cellules à sortir du mode croissance pour entrer dans l’état décidual spécialisé qui soutient le début de la grossesse.
Affiner les signaux hormonaux à l’intérieur de la cellule
La progestérone et son récepteur sont au centre de la préparation utérine, mais tous les tissus ne répondent pas de la même façon à l’hormone. Les chercheurs ont découvert que la signalisation de la progestérone augmente elle‑même les niveaux de HBP1, créant une boucle de rétroaction positive. Fait frappant, la diminution de HBP1 n’a pas modifié la quantité de récepteur de la progestérone produite par les cellules, mais elle a atténué l’activité de gènes importants répondant à la progestérone, notamment FKBP4, FKBP5, FOSL2 et le coactivateur SRC1. Par des approches à l’échelle du génome, ils ont montré que HBP1 se lie à proximité de nombreux de ces gènes et s’associe à une augmentation d’une marque histone spécifique, H3K4me3, qui signale une région d’ADN active. En substance, HBP1 ne met pas le récepteur en marche ou hors marche ; il rend les gènes cibles du récepteur plus lisibles.
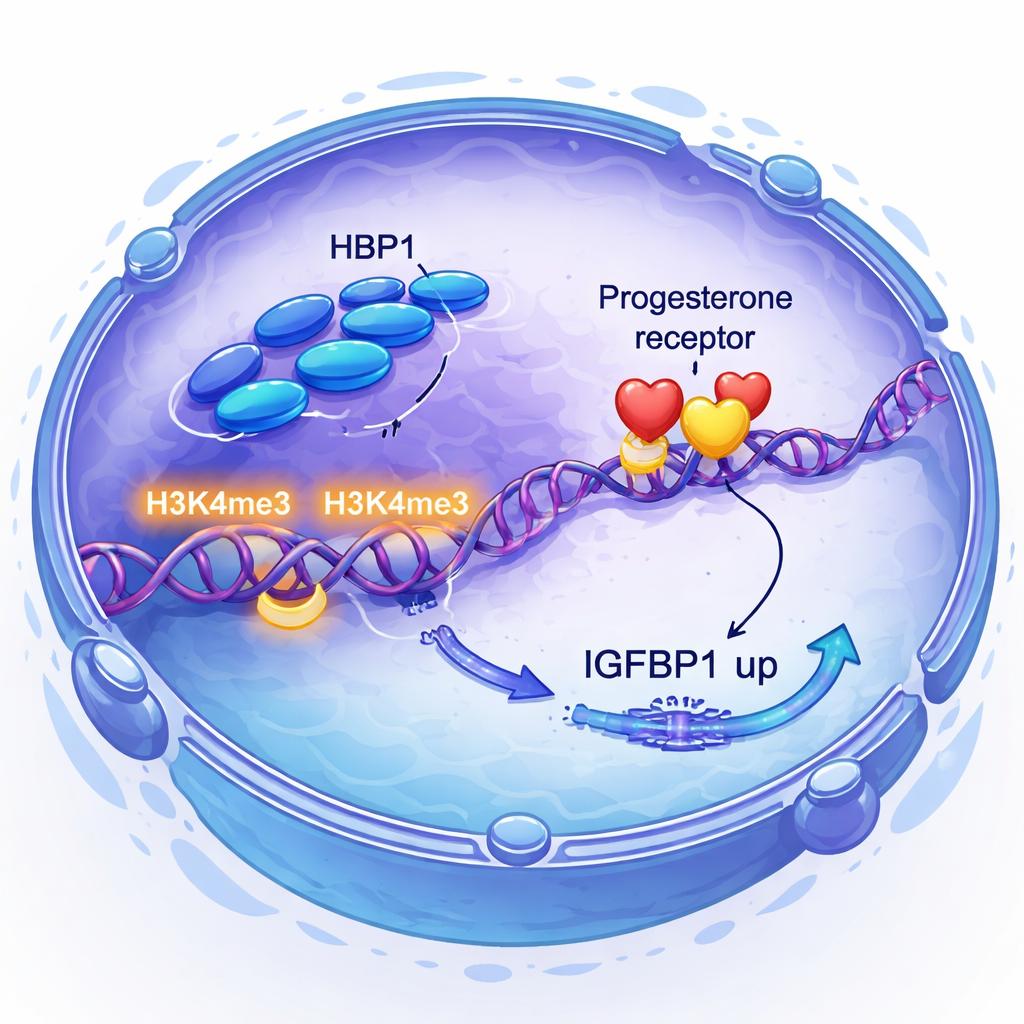
Contrôle direct d’un signal clé d’implantation
L’équipe a ensuite examiné comment HBP1 se relie à IGFBP1, une protéine utilisée depuis longtemps comme marqueur d’une décidualisation saine et connue pour influencer la communication entre l’embryon et l’utérus. En combinant le séquençage de l’ARN et l’immunoprécipitation de la chromatine suivie de séquençage, ils ont montré que HBP1 se situe directement sur la région promotrice d’IGFBP1 et y augmente H3K4me3, stimulant ainsi une plus forte production d’IGFBP1. Ils ont aussi constaté que la réduction de HBP1 activait la voie PI3K–AKT, un signal lié à la croissance qui, lorsqu’il est hyperactif, réprime IGFBP1. Le blocage de cette voie a permis de restaurer les niveaux d’IGFBP1. Ainsi, HBP1 soutient la décidualisation de deux manières : en activant directement IGFBP1 et en atténuant un signal de croissance qui aurait autrement freiné les gènes déciduaux.
Relier un défaut moléculaire à l’échec d’implantation
Enfin, les chercheurs ont analysé des échantillons endométriaux de femmes souffrant d’échecs d’implantation récurrents et les ont comparés avec des tissus de femmes fertiles pendant la phase sécrétoire médiane, prête pour l’implantation. Les femmes avec échecs répétés présentaient des niveaux nettement plus faibles de HBP1 et de ses partenaires en aval IGFBP1, FKBP5 et FOSL2, bien que les niveaux de récepteur de la progestérone soient similaires entre les groupes. Ce schéma s’accorde avec l’idée d’une « résistance à la progestérone » — l’hormone est présente, mais le tissu ne peut pas monter une réponse complète parce que des facteurs de soutien clés comme HBP1 font défaut.
Ce que cela signifie pour les patientes
Dit simplement, cette étude suggère que HBP1 agit comme un réglage maître sur le tableau de bord de l’endomètre. Lorsqu’il est correctement augmenté, il aide à faire entendre les signaux de la progestérone, encourage les cellules à cesser de se diviser et à se spécialiser, et augmente la production de molécules favorables à l’implantation comme IGFBP1. Lorsque HBP1 est trop faible, la muqueuse peut sembler normale au microscope mais fonctionner mal, empêchant les embryons de s’implanter. Comprendre et mesurer HBP1 et son réseau pourrait, à l’avenir, aider les cliniciens à identifier les femmes à risque de problèmes d’implantation et inspirer de nouveaux traitements visant à restaurer la réceptivité utérine.
Citation: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Mots-clés: décidualisation endométriale, implantation de l’embryon, signalisation de la progestérone, infertilité, HBP1