Clear Sky Science · fr
Le métabolite intestinal acide indole-3-acétique aggrave le lupus neuropsychiatrique via la voie AHR/STAT3 dans les microglies
Comment les microbes intestinaux peuvent affecter l’esprit
Les personnes atteintes de lupus, une maladie auto-immune, développent parfois des troubles sérieux de la pensée, de l’humeur et de la mémoire — une affection appelée lupus neuropsychiatrique. Ces symptômes cérébraux peuvent être invalidants, et les médecins peinent encore à en expliquer précisément les causes ou à les traiter. Cette étude explore un coupable inattendu : certaines bactéries intestinales et les produits chimiques qu’elles génèrent, susceptibles de passer de l’intestin au cerveau et d’y attiser l’inflammation.
Des microbes intestinaux aux comportements perturbés
Les chercheurs ont d’abord cherché à savoir si les microbes intestinaux de patients atteints de lupus neuropsychiatrique différaient par leurs effets de ceux de patients lupiques sans symptômes cérébraux. Ils ont transféré les bactéries fécales de chaque groupe de patients dans des souris saines préalablement débarrassées de leur propre microbiote. Les souris ayant reçu les microbes de patients atteints de lupus neuropsychiatrique ont développé davantage de comportements de type anxieux, des signes de dépression et des problèmes d’apprentissage et de mémoire que les souris ayant reçu les microbes d’autres patients lupiques. Leur cerveau présentait une activation accrue des microglies — les cellules immunitaires du cerveau — et des niveaux plus élevés de molécules inflammatoires. La barrière protectrice autour du cerveau, connue sous le nom de barrière hémato‑encéphalique, était également plus perméable chez ces animaux, suggérant que quelque chose dans le microbiote transplanté endommageait cette barrière critique.
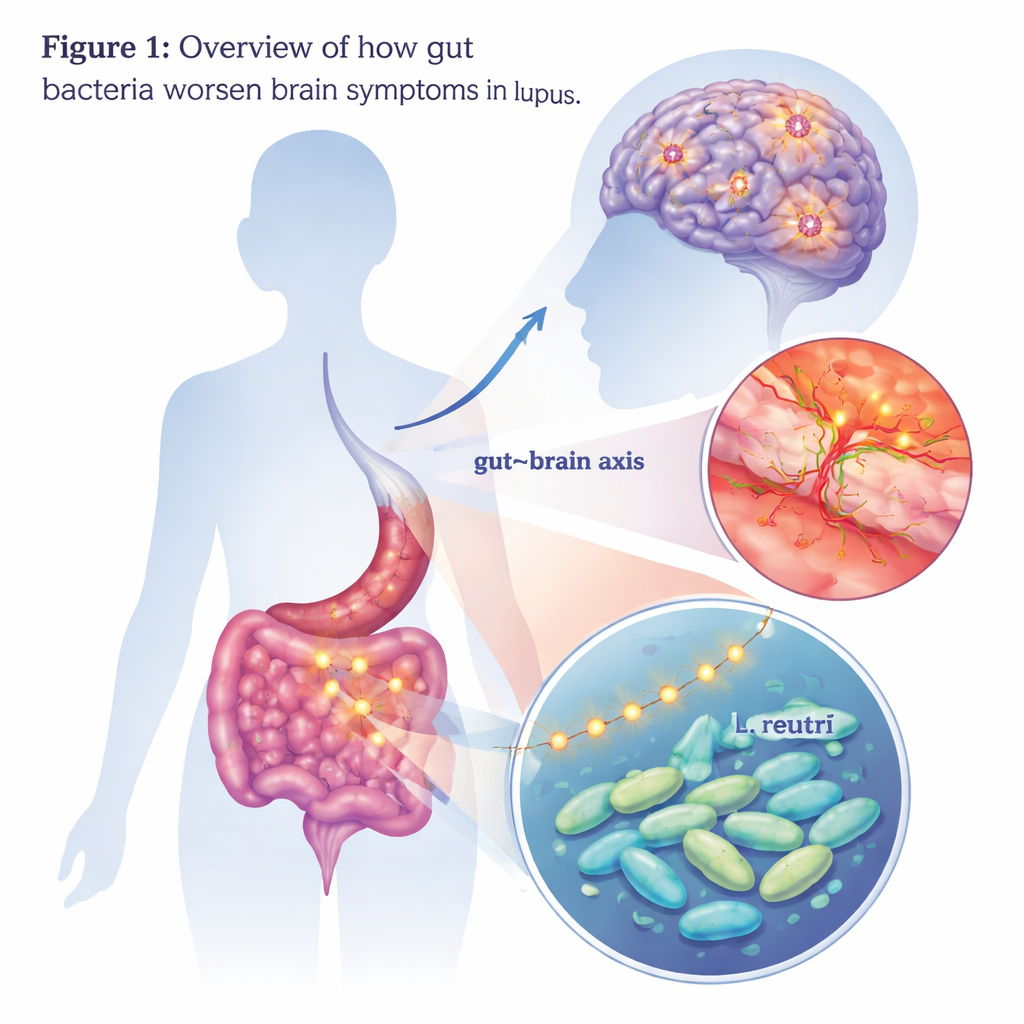
Zoom sur une seule bactérie
Pour identifier les microbes potentiellement responsables, l’équipe a comparé les communautés bactériennes intestinales des patients et des souris. Un groupe a attiré l’attention : Lactobacillus, et en particulier une espèce appelée Lactobacillus reuteri, était plus abondant chez les patients atteints de lupus neuropsychiatrique et chez les souris présentant des altérations cérébrales. Lorsque les scientifiques ont nourri des souris prédisposées au lupus avec L. reuteri seule, les animaux ont développé des comportements anxieux et dépressifs plus marqués et ont obtenu de moins bons résultats aux tests de mémoire. Leur cerveau présentait davantage de microglies activées, une perte accrue de neurones et une perturbation supplémentaire de la barrière hémato‑encéphalique. Ces résultats suggèrent que, au moins dans le contexte du lupus, cette bactérie habituellement considérée comme probiotique peut adopter un rôle plus nocif.
Une petite molécule aux grands effets
L. reuteri est connue pour produire une molécule appelée acide indole‑3‑acétique (AIA) à partir du tryptophane alimentaire. Grâce à des tests chimiques sensibles, l’équipe a détecté des niveaux plus élevés d’AIA dans les selles des patients atteints de lupus neuropsychiatrique que chez les autres patients lupiques, et a confirmé que des cultures de L. reuteri produisent beaucoup plus d’AIA que des bactéries intestinales communes comme Escherichia coli. Chez les patients atteints de lupus neuropsychiatrique, les niveaux d’AIA dans le liquide entourant le cerveau et la moelle épinière corrélaient avec des niveaux plus élevés de cytokines inflammatoires, ce qui laisse entendre que cette molécule peut atteindre le système nerveux central et y déclencher l’inflammation. Chez des souris prédisposées au lupus, l’alimentation en L. reuteri augmentait les niveaux d’AIA dans l’intestin, le sang et le cerveau. L’administration d’AIA seule à ces souris reproduisait bon nombre des mêmes changements : comportements anormaux, activation des microglies, signaux inflammatoires accrus et affaiblissement de la barrière hémato‑encéphalique et de la barrière intestinale.
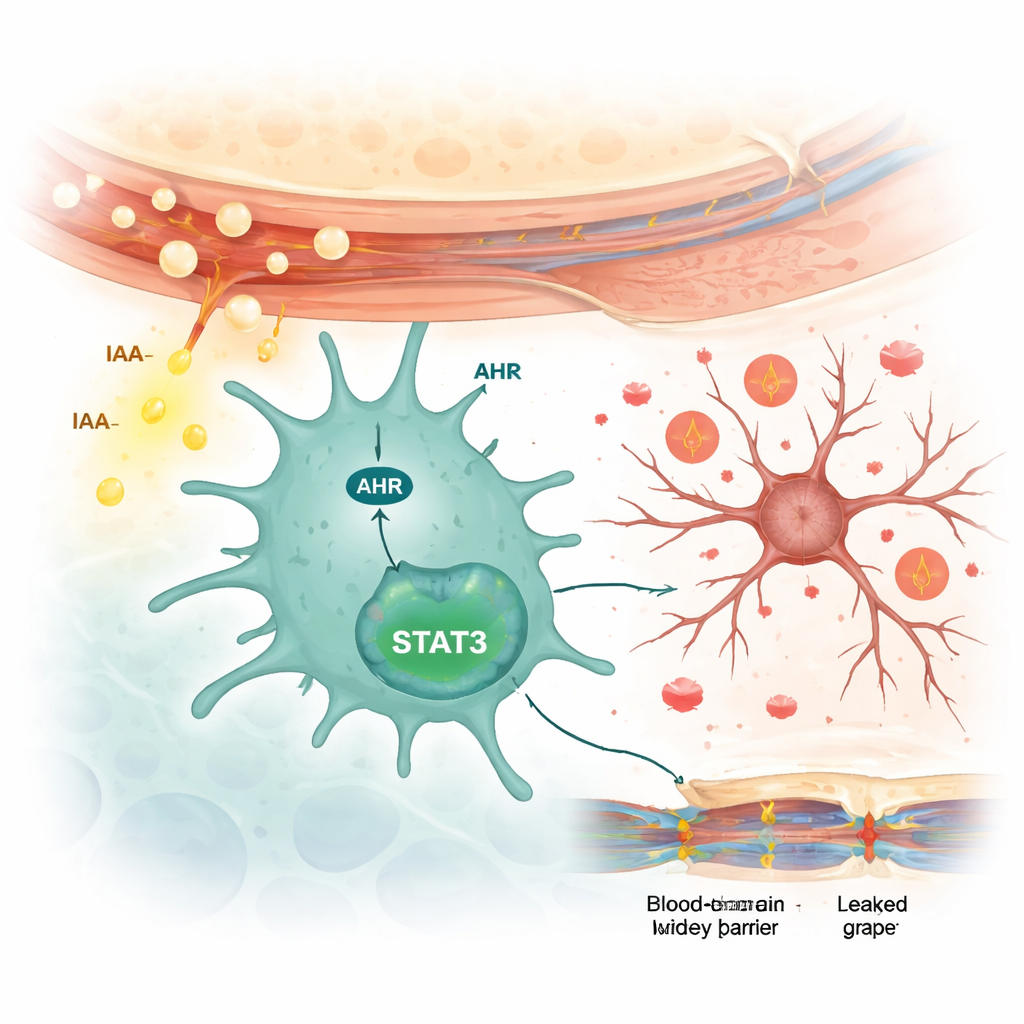
Comment les cellules immunitaires cérébrales sont activées
Les scientifiques ont ensuite examiné comment l’AIA communique avec les cellules cérébrales. Ils ont constaté que l’AIA augmentait l’activité d’une protéine capteur appelée récepteur aryl‑hydrocarbone (AHR) spécifiquement dans les microglies, et non dans les neurones ou les cellules de soutien étoilées appelées astrocytes. Dans des microglies en culture, l’AIA augmentait les niveaux d’AHR et activait une protéine de signalisation en aval nommée STAT3, qui à son tour stimulait la production de cytokines inflammatoires. Le blocage de l’AHR par un médicament empêchait l’activation de STAT3 et réduisait la libération de ces signaux inflammatoires. Lorsque des souris prédisposées au lupus ont été traitées par ce médicament bloquant l’AHR, leurs comportements anxieux et dépressifs se sont améliorés, l’activation des microglies a diminué, les molécules inflammatoires ont chuté et la barrière hémato‑encéphalique est devenue moins perméable.
Ce que cela signifie pour les patients
Globalement, l’étude décrit une chaîne d’événements reliant l’intestin au cerveau dans le lupus neuropsychiatrique. Une surabondance de L. reuteri dans l’intestin produit un excès d’AIA, qui fragilise la barrière intestinale et pénètre dans la circulation sanguine. L’AIA atteint ensuite le cerveau, où il active la signalisation AHR/STAT3 des microglies, déclenchant une inflammation qui endommage les neurones et relâche la barrière hémato‑encéphalique. Pour les patients, ces résultats suggèrent que modifier le microbiote intestinal, réduire les métabolites nuisibles comme l’AIA, ou bloquer la voie AHR/STAT3 dans les microglies pourrait un jour aider à protéger le cerveau des effets dévastateurs du lupus neuropsychiatrique.
Citation: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Mots-clés: lupus neuropsychiatrique, microbiote intestinal, Lactobacillus reuteri, inflammation des microglies, barrière hémato‑encéphalique